Clear Sky Science · it
p53: dalla comprensione della sua struttura ai progressi nel targeting terapeutico
Perché questa proteina guardiana è importante
La proteina p53 è spesso chiamata il “guardiano del genoma” perché aiuta le cellule sane a riparare i danni e impedisce alle cellule compromesse di diventare cancerose. Questo articolo di revisione spiega come funziona p53, perché fallisce così frequentemente nei tumori e come gli scienziati stanno ora imparando a colpire con farmaci ciò che per lungo tempo è stato considerato “non farmacabile”. Esamina inoltre collegamenti sorprendenti tra p53 e patologie come il morbo di Alzheimer, il diabete e le malattie cardiache, e passa in rassegna nuovi trattamenti che cercano di correggere o aggirare i guasti di p53.
L’ispettore di sicurezza interno della cellula
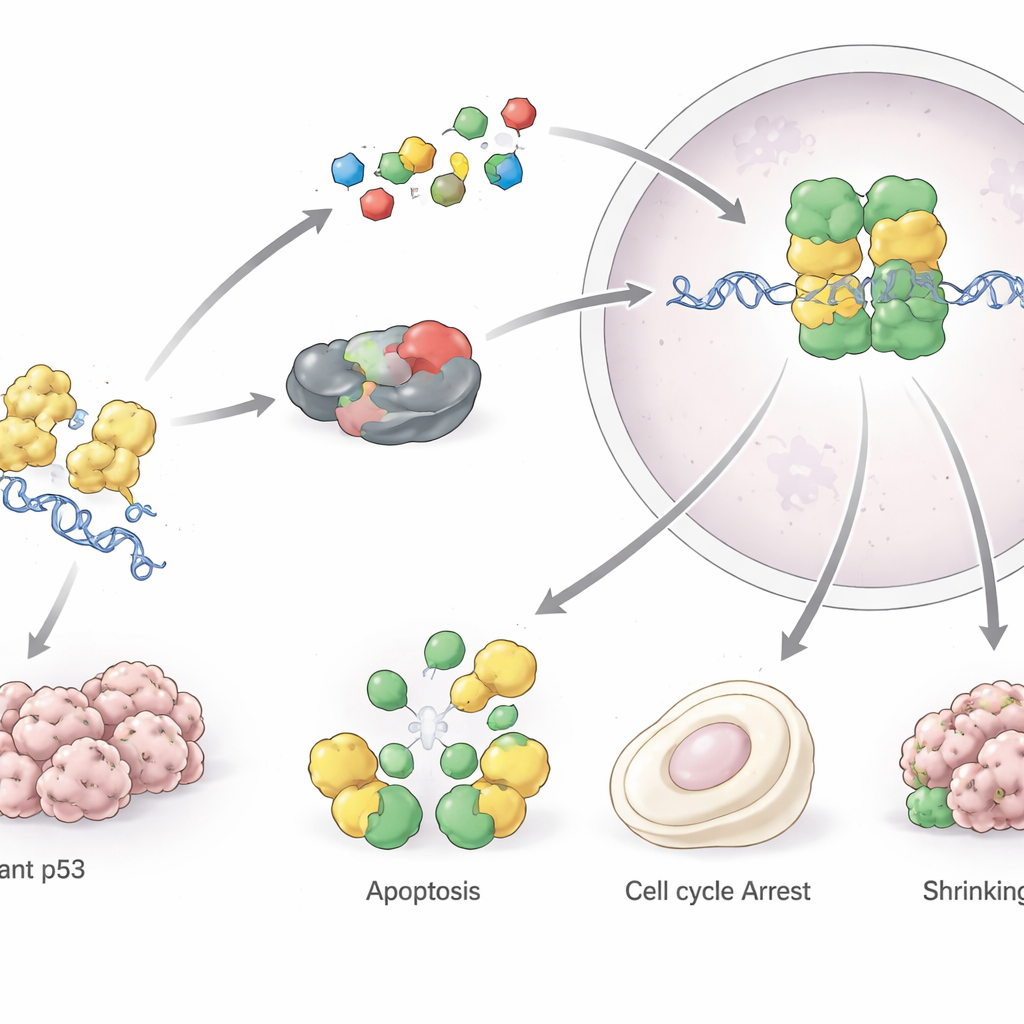
In condizioni normali, le cellule mantengono bassi i livelli di p53 tramite un sistema di riciclaggio intrinseco. Quando arriva lo stress — come danni al DNA, ipossia o segnali che favoriscono il cancro — p53 si accumula rapidamente e attiva molti geni. Questi geni arrestano la divisione cellulare, innescano la riparazione del DNA, aggiustano il metabolismo o, se il danno è troppo grave, spingono la cellula verso il ritiro permanente (senescenza) o la morte programmata (apoptosi). In questo modo p53 mantiene stabile il codice genetico e impedisce la proliferazione di cellule danneggiate. Influisce anche su forme più recenti di morte cellulare, come la ferroptosi, e modella l’ambiente immunitario intorno ai tumori, aiutando le cellule immunitarie a riconoscere e attaccare le cellule cancerose.
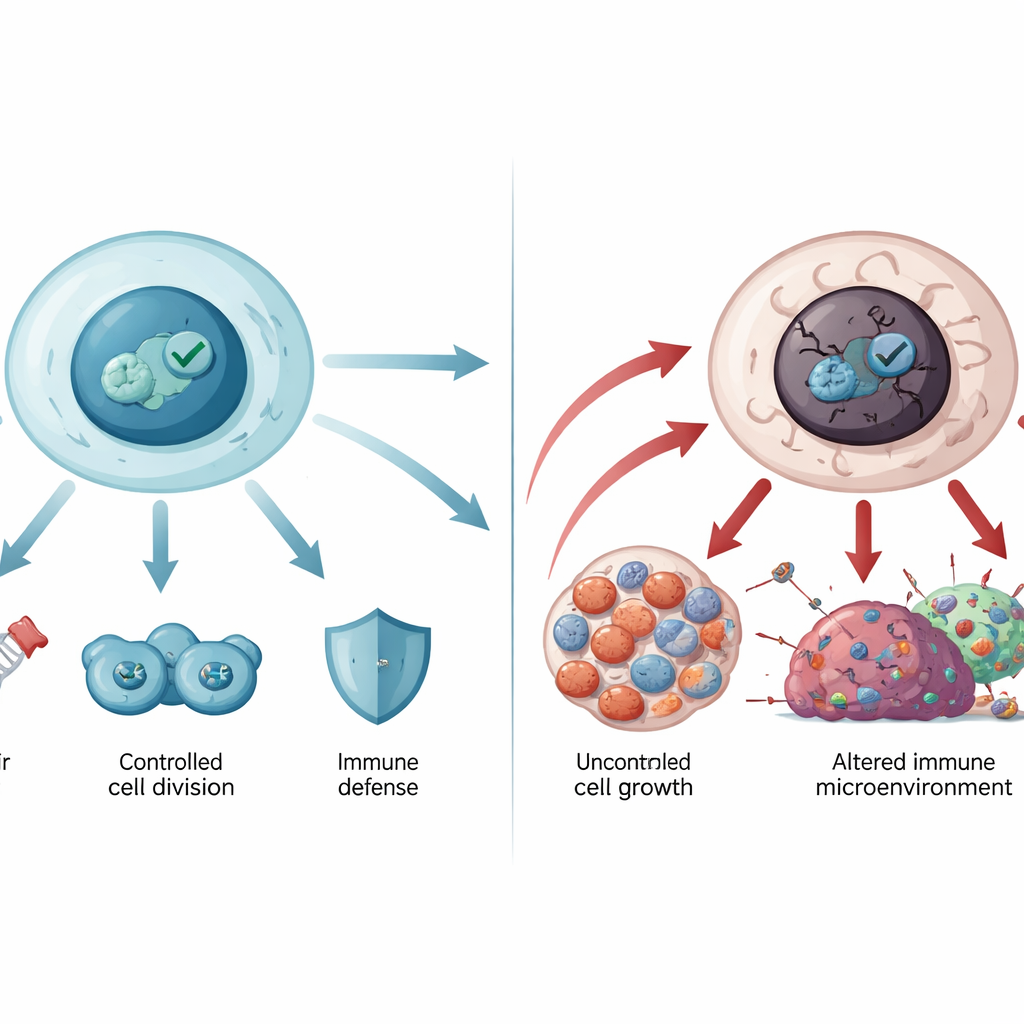
Quando il guardiano va fuori controllo
Il gene che codifica p53, TP53, è il gene più frequentemente mutato nei tumori umani. La maggior parte di queste mutazioni consiste in cambiamenti di un singolo amminoacido nella regione centrale di legame al DNA della proteina. Alcune mutazioni indeboliscono l’affinità di p53 per il DNA, mentre altre destabilizzano la sua struttura facendola così disfoldare e raggrumare in aggregati che ricordano gli amiloidi osservati nelle malattie neurodegenerative. p53 mutante non solo perde il ruolo protettivo ma può anche acquisire nuove attività promotrici del cancro: può favorire una crescita incontrollata, aiutare le cellule tumorali a resistere alla morte cellulare e alla chemioterapia, rimodellare il metabolismo per nutrire i tumori e indebolire l’immunità antitumorale. Le mutazioni germinali di TP53 sono alla base della sindrome di Li‑Fraumeni e di altri rari disturbi ereditari con alto rischio di cancro, dimostrando quanto sia cruciale questa via per la protezione nel corso della vita.
Oltre il cancro: connessioni con cervello, metabolismo e cuore
Poiché p53 controlla la morte cellulare, le risposte allo stress e l’uso di energia, la sua influenza si estende oltre il cancro. Nel cervello, un’attività anomala di p53 è stata collegata ad Alzheimer, Parkinson, Huntington, SLA e sclerosi multipla, spesso tramite interazioni con proteine associate a queste malattie e promuovendo una perdita eccessiva di neuroni vulnerabili. Nel metabolismo, p53 contribuisce a regolare l’accumulo di grasso, la glicemia e il grasso epatico; a seconda del contesto, può proteggere da obesità e diabete oppure contribuire a insulino‑resistenza e steatosi epatica. Nel cuore e nei vasi sanguigni, p53 influenza la sopravvivenza cellulare, la formazione di tessuto cicatriziale e la deposizione di placche, svolgendo ruoli complessi nell’insufficienza cardiaca, nei danni cardiaci diabetici e nell’aterosclerosi. Questi effetti così ampi significano che ogni tentativo di potenziare o bloccare p53 deve bilanciare i benefici antitumorali con potenziali danni ai tessuti normali.
Nuove strategie per colpire il “non farmacabile”
Per decenni p53 è stato considerato troppo complesso e troppo centrale per essere mirato in sicurezza con farmaci. Questa visione sta cambiando. Una strategia principale mira a “salvare” p53 mutato stabilizzandone la conformazione in modo che si comporti più come la proteina normale; esempi includono PRIMA‑1/APR‑246, triossido di arsenico e molecole progettate per specifici hotspot mutazionali come Y220C o R175H. Un altro approccio è aumentare i livelli di p53 normale nei tumori che mantengono un gene TP53 intatto bloccando i suoi regolatori negativi MDM2 e MDM4; diversi inibitori orali di queste proteine sono in sperimentazione clinica. Una terza tattica cerca di privare le cellule tumorali della loro dipendenza da p53 mutante favorendone la degradazione mediante inibitori dello shock termico e delle deacetilasi istoniche o con comuni farmaci statine. In parallelo, vaccini, cellule dendritiche ingegnerizzate e anticorpi ad elevata specificità sono in sviluppo per aiutare il sistema immunitario a riconoscere le cellule sovraccariche di p53 anomalo.
Prospettive future: dalle mappe ai farmaci
L’articolo conclude che p53 è passata dall’essere una curiosità biologica a un bersaglio terapeutico realistico, ma che richiede precisione. La diversità delle mutazioni TP53 e la natura a doppio taglio dei ruoli di p53 nei tessuti normali rendono improbabili terapie valide per tutti. Gli autori immaginano invece combinazioni di piccole molecole, immunoterapie e strumenti di editing genico guidati dalla biologia dei sistemi e dal machine learning per abbinare la strategia mirata a p53 più adatta all’architettura di ciascun tumore. Se questi sforzi avranno successo, farmaci che ripristinano o compensano la funzione di p53 potrebbero trasformare le cure non solo per molti tumori, ma potenzialmente anche per alcune malattie non neoplastiche legate a questa proteina guardiana fondamentale.
Citazione: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Parole chiave: p53, mutazioni TP53, terapia oncologica, vie di soppressione tumorale, farmaci mirati a p53