Clear Sky Science · tr
p53: yapısını anlamaktan terapötik hedeflemelerdeki gelişmelere
Bu koruyucu protein neden önemli
p53 proteini genellikle “genomun bekçisi” olarak adlandırılır; çünkü sağlıklı hücrelerin hasarı onarmasına yardımcı olur ve hasarlı hücrelerin kansere dönüşmesini engeller. Bu derleme makalesi p53’ün nasıl çalıştığını, kanserde neden bu kadar sık çöktüğünü ve uzun süre “ilaçla hedeflenemez” kabul edilen bir hedefin nasıl ilaçlanabilir hale getirildiğini açıklar. Ayrıca p53 ile Alzheimer hastalığı, diyabet ve kalp hastalığı gibi durumlar arasındaki şaşırtıcı bağlantıları inceler ve p53’ün başarısızlıklarını onarmaya veya bunların etrafından dolaşmaya çalışan yeni tedavileri gözden geçirir.
Hücrenin iç denetçisi
Normal koşullarda hücreler, yerleşik bir geri dönüşüm sistemiyle p53 düzeylerini düşük tutar. DNA hasarı, oksijen düşüklüğü veya kanseri teşvik eden sinyaller gibi stresler ortaya çıktığında p53 hızla birikir ve birçok geni etkinleştirir. Bu genler hücre bölünmesini duraklatır, DNA tamirini tetikler, metabolizmayı ayarlar veya hasar çok büyükse hücreyi kalıcı emekliliğe (senesans) ya da kontrol edilen hücre ölümüne (apoptoz) sürükler. Bu yolla p53 genetik kodu kararlı tutar ve hasarlı hücrelerin çoğalmasını önler. Ayrıca ferroptoz gibi daha yeni hücre ölümü biçimlerini etkiler ve tümör çevresindeki bağışıklık ortamını şekillendirerek bağışıklık hücrelerinin kanserli hücreleri tanımasına ve saldırmasına yardımcı olur.
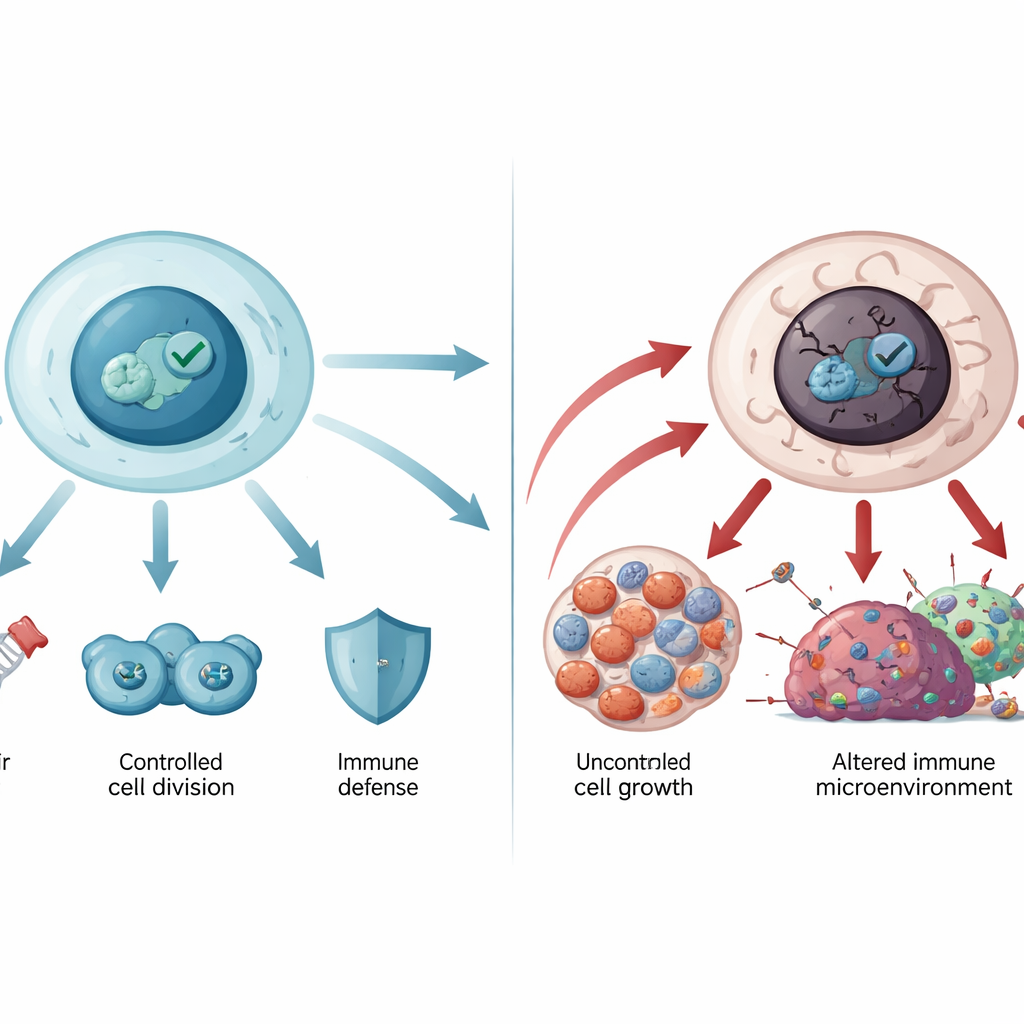
Koruyucu düştüğünde
p53’ü kodlayan gen olan TP53, insan kanserlerinde en sık mutasyona uğrayan gendir. Bu mutasyonların çoğu proteinin merkezi DNA bağlayan bölümünde tek bir aminoasit değişikliğidir. Bazı mutasyonlar p53’ün DNA’ya tutunmasını zayıflatırken, diğerleri yapısını kararsızlaştırıp açılmasına ve amiloide benzer agregatlar halinde kümeleşmesine yol açar; bu durum nörodejeneratif hastalıklarda görülenlerle benzerlik taşır. Mutant p53 yalnızca koruyucu rolünü kaybetmekle kalmaz, aynı zamanda yeni kanser‑destekleyici aktiviteler de kazanabilir: kontrolsüz büyümeyi teşvik edebilir, tümör hücrelerinin hücre ölümüne ve kemoterapiye direnç göstermesine yardımcı olabilir, tümörleri beslemek için metabolizmayı yeniden şekillendirebilir ve anti‑tümör bağışıklığı zayıflatabilir. Germline TP53 mutasyonları Li‑Fraumeni sendromu ve yüksek kanser riski taşıyan diğer nadir kalıtsal bozuklukların temelini oluşturarak bu yolun yaşam boyu koruma için ne kadar kritik olduğunu gösterir.
Kansere ek olarak: beyin, metabolizma ve kalple bağlantılar
p53 hücre ölümü, stres tepkileri ve enerji kullanımı üzerinde kontrol sağladığından etkisi kanserin ötesine uzanır. Beyinde anormal p53 aktivitesi Alzheimer, Parkinson, Huntington, ALS ve multipl skleroz ile ilişkilendirilmiştir; genellikle hastalıkla ilişkili proteinlerle etkileşimler yoluyla ve hassas nöronların aşırı kaybını teşvik ederek zarar verir. Metabolizmada p53 yağ depolanmasını, kan şekerini ve karaciğer yağını düzenlemeye yardımcı olur; bağlama bağlı olarak obezite ve diyabete karşı koruyucu olabileceği gibi insülin direnci ve yağlı karaciğere katkıda da bulunabilir. Kalp ve kan damarlarında p53 hücre hayatta kalmasını, skarlaşmayı ve plak oluşumunu etkiler; kalp yetmezliği, diyabetik kalp hasarı ve aterosklerozda karmaşık roller oynar. Bu geniş etkiler, p53’ü güçlendirme veya engelleme girişimlerinin anti‑kanser faydalarını normal dokulara zarar verme riskiyle dengelemesini gerektirir.
“İlaçlanamaz” olana yeni yollar
On yıllar boyunca p53, ilaçla güvenle hedeflenemeyecek kadar karmaşık ve merkezi olarak görüldü. Bu görüş değişiyor. Bir ana strateji, mutant p53’ü normal proteine daha çok benzeyecek şekilde stabil kılarak “kurtarmaya” yöneliktir; örnekler arasında PRIMA‑1/APR‑246, arsenik trioksit ve Y220C veya R175H gibi hotspot mutantlara özgü moleküller yer alır. Diğer bir yaklaşım, hâlâ sağlam bir TP53 geni taşıyan tümörlerde normal p53 düzeylerini artırmak için negatif düzenleyicileri MDM2 ve MDM4’ü engellemektir; bu proteinlerin birkaç oral inhibitörü klinik denemelerde bulunmaktadır. Üçüncü taktik, ısı şoku ve histon deasetilaz inhibitörleri veya yaygın kullanılan statin ilaçlarıyla mutant p53’e bağımlılığı azaltarak tümör hücrelerini bu bağımlılıktan arındırmayı denemektir. Paralel olarak, aşılar, genetik olarak tasarlanmış dendritik hücreler ve yüksek özgüllüğe sahip antikorlar, anormal p53 ile yüklü hücreleri bağışıklık sisteminin tanımasına yardımcı olmak üzere geliştirilmektedir.
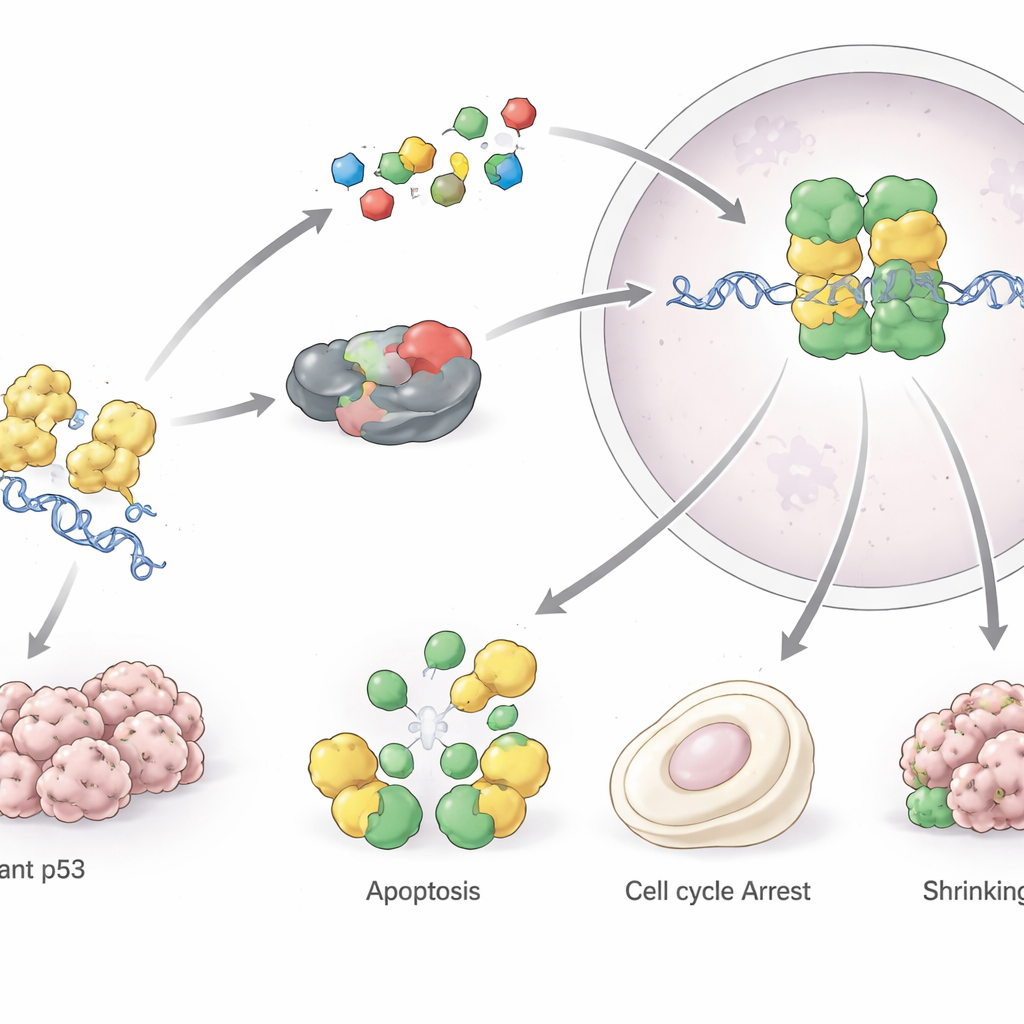
İleriye bakış: haritalardan ilaçlara
Makale, p53’ün salt biyolojik bir meraktan gerçekçi bir terapötik hedefe dönüştüğünü, ancak bunun büyük bir hassasiyet gerektirdiğini sonuçlandırır. TP53 mutasyonlarının çeşitliliği ve p53’ün normal dokulardaki çift taraflı doğası tek beden herkese uyar tedavileri olasılıksız kılar. Bunun yerine yazarlar, sistem biyolojisi ve makine öğrenmesi tarafından yönlendirilen küçük moleküller, immünoterapiler ve gen düzenleme araçlarının kombinasyonlarını hayal ediyor; böylece her tümörün devre şemasına uygun doğru p53 hedefli strateji seçilebilir. Bu çabalar başarılı olursa, p53 fonksiyonunu geri kazandıran veya telafi eden ilaçlar birçok kanserin bakımını —ve muhtemelen bu hayati koruyucu proteinle ilişkili bazı kanser dışı hastalıkları— dönüştürebilir.
Atıf: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Anahtar kelimeler: p53, TP53 mutasyonları, kanser tedavileri, tümör baskılayıcı yollar, p53 hedefli ilaçlar