Clear Sky Science · pl
p53: od poznania jego struktury do postępów w celowaniu terapeutycznym
Dlaczego ten białkowy strażnik ma znaczenie
Białko p53 bywa nazywane „strażnikiem genomu”, ponieważ pomaga zdrowym komórkom naprawiać uszkodzenia i powstrzymuje uszkodzone komórki przed przemianą w nowotwór. Ten przegląd wyjaśnia, jak działa p53, dlaczego tak często zawodzi w nowotworach i jak naukowcy uczą się leczyć coś, co długo uważano za „nieleczalne”. Omówione są także zaskakujące powiązania p53 z chorobami takimi jak choroba Alzheimera, cukrzyca czy choroby serca oraz przegląd nowych terapii, które próbują naprawić lub ominąć niedoskonałości p53.
Wewnętrzny inspektor bezpieczeństwa komórki
W normalnych warunkach komórki utrzymują niskie poziomy p53 dzięki wbudowanemu systemowi recyklingu. Gdy pojawia się stres — na przykład uszkodzenie DNA, niedobór tlenu lub sygnały sprzyjające nowotworzeniu — p53 szybko się kumuluje i włącza wiele genów. Geny te zatrzymują podział komórek, uruchamiają naprawę DNA, dostosowują metabolizm lub, jeśli uszkodzenia są zbyt rozległe, prowadzą komórkę do trwałego wycofania się (senescencja) lub kontrolowanej śmierci (apoptoza). W ten sposób p53 utrzymuje stabilność kodu genetycznego i zapobiega mnożeniu się uszkodzonych komórek. Wpływa także na nowsze formy śmierci komórkowej, takie jak ferroptoza, oraz kształtuje środowisko immunologiczne wokół guzów, pomagając komórkom układu odpornościowego rozpoznawać i atakować komórki nowotworowe.
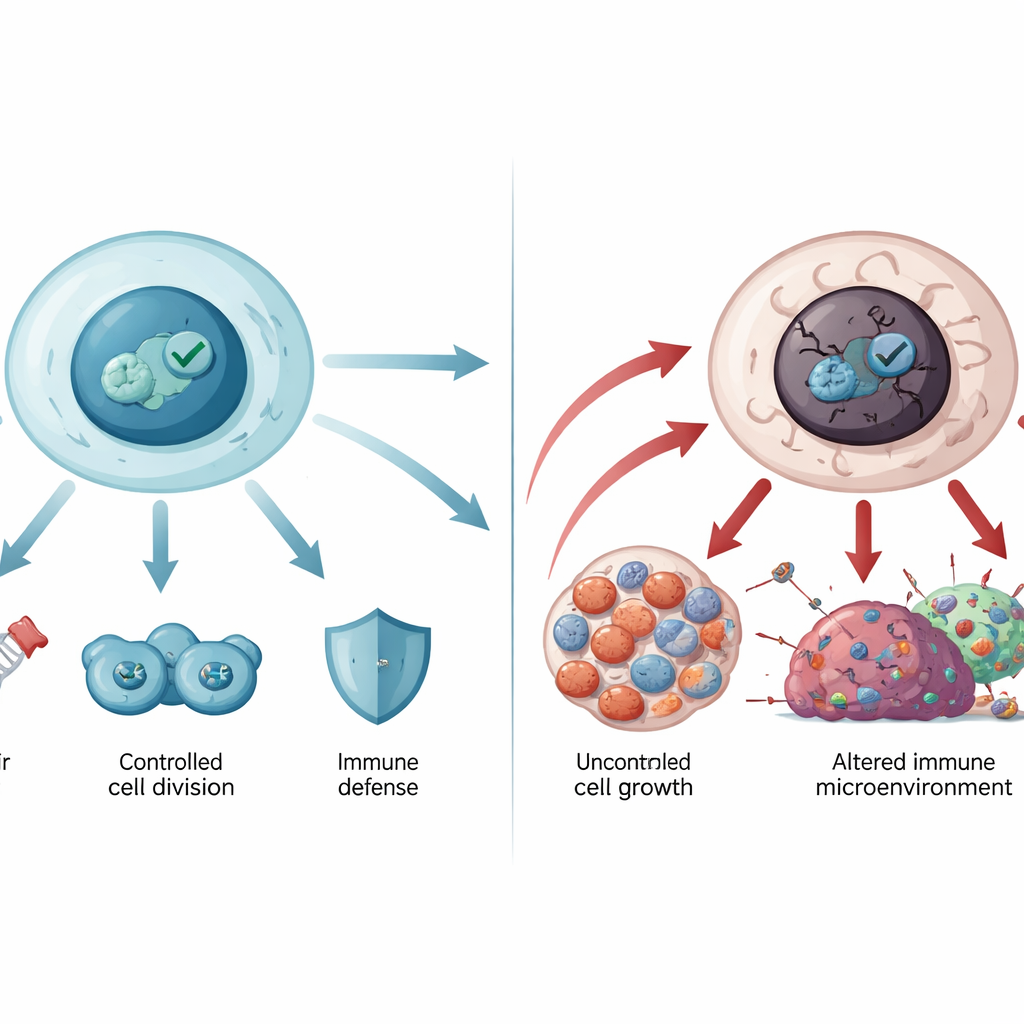
Kiedy strażnik zbuntuje się
Gen kodujący p53, TP53, jest najczęściej zmutowanym genem w nowotworach u ludzi. Większość tych mutacji to pojedyncze zmiany aminokwasowe w centralnej części białka wiążącej DNA. Niektóre mutacje osłabiają przyczepność p53 do DNA, inne destabilizują jego strukturę, powodując rozfałdowanie i agregację przypominającą amyloid, znaną z chorób neurodegeneracyjnych. Zmutowane p53 nie tylko traci rolę ochronną, lecz może też zyskiwać nowe, sprzyjające rakowi funkcje: może pobudzać niekontrolowany wzrost, pomagać komórkom nowotworowym w oporności na śmierć i chemioterapię, przekształcać metabolizm na rzecz guza oraz osłabiać odporność przeciwnowotworową. Mutacje TP53 w linii zarodkowej leżą u podstaw zespołu Li–Fraumeni i innych rzadkich chorób dziedzicznych z wysokim ryzykiem nowotworów, co pokazuje, jak kluczowa jest ta ścieżka dla ochrony przez całe życie.
Ponad rakiem: powiązania z mózgiem, metabolizmem i sercem
Ponieważ p53 kontroluje śmierć komórek, odpowiedzi na stres i wykorzystanie energii, jego wpływ wykracza poza nowotwory. W mózgu nieprawidłowa aktywność p53 wiązana jest z chorobą Alzheimera, Parkinsona, chorobą Huntingtona, stwardnieniem zanikowym bocznym (ALS) i stwardnieniem rozsianym — często poprzez interakcje z białkami związanymi z tymi chorobami i przez promowanie nadmiernej utraty wrażliwych neuronów. W metabolizmie p53 reguluje magazynowanie tłuszczu, poziom cukru we krwi i stłuszczenie wątroby; w zależności od kontekstu może chronić przed otyłością i cukrzycą lub przyczyniać się do insulinooporności i stłuszczeniowej choroby wątroby. W sercu i naczyniach p53 wpływa na przeżycie komórek, bliznowacenie i tworzenie się blaszek miażdżycowych, odgrywając złożone role w niewydolności serca, uszkodzeniu serca w cukrzycy i miażdżycy. Te szerokie efekty oznaczają, że każda próba zwiększenia lub zablokowania p53 musi wyważyć korzyści przeciwnowotworowe z potencjalnymi szkodami dla tkanek prawidłowych.
Nowe sposoby leczenia „nieleczalnego”
Przez dekady p53 uważano za zbyt złożone i zbyt istotne, by bezpiecznie celować w nie lekami. Ten pogląd się zmienia. Jedna z głównych strategii ma na celu „uratowanie” zmutowanego p53 przez stabilizację jego kształtu, aby zachowywało się bardziej jak białko prawidłowe; przykłady to PRIMA‑1/APR‑246, trójtlenek arsenu oraz cząsteczki dostosowane do konkretnych gorących punktów mutacyjnych, takich jak Y220C czy R175H. Innym podejściem jest podniesienie poziomów prawidłowego p53 w guzach, które wciąż mają nienaruszony gen TP53, poprzez blokowanie jego negatywnych regulatorów MDM2 i MDM4; kilka doustnych inhibitorów tych białek znajduje się w badaniach klinicznych. Trzecia taktyka próbuje pozbawić komórki nowotworowe zależności od zmutowanego p53, promując jego degradację za pomocą inhibitorów szoku cieplnego i deacetylaz histonowych lub powszechnie stosowanych leków statynowych. Równolegle rozwijane są szczepionki, zmodyfikowane komórki dendrytyczne i wysoce swoiste przeciwciała, które mają pomóc układowi odpornościowemu w rozpoznaniu komórek przeładowanych nieprawidłowym p53.
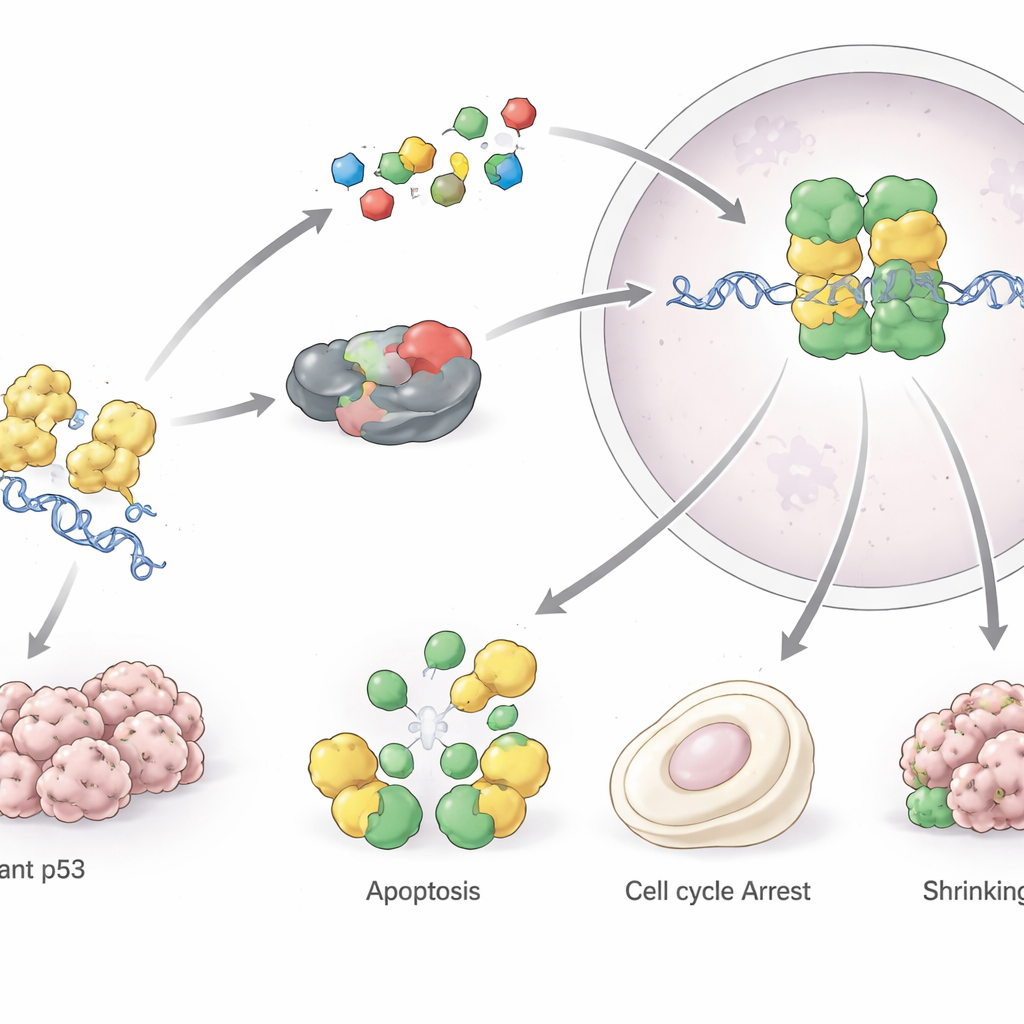
Perspektywy: od map do leków
Artykuł konkluduje, że p53 przestało być jedynie ciekawostką biologiczną i stało się realistycznym celem terapeutycznym, choć wymagającym precyzji. Różnorodność mutacji TP53 i dwustronna rola p53 w tkankach normalnych sprawiają, że uniwersalne terapie są mało prawdopodobne. Autorzy przewidują raczej kombinacje małych cząsteczek, immunoterapii i narzędzi edycji genów kierowanych przez biologię systemową i uczenie maszynowe, które dobiorą właściwą strategię ukierunkowaną na p53 do specyfiki sieci sygnałowej każdego guza. Jeśli te wysiłki się powiodą, leki przywracające lub kompensujące funkcję p53 mogą przekształcić opiekę nie tylko w wielu nowotworach, ale potencjalnie także w niektórych chorobach niezwiązanych z rakiem, powiązanych z tym kluczowym białkowym strażnikiem.
Cytowanie: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Słowa kluczowe: p53, mutacje TP53, terapie przeciwnowotworowe, szlaki supresorów nowotworów, leki ukierunkowane na p53