Clear Sky Science · ar
p53: من فهم بنيته إلى التقدّم في الاستهداف العلاجي
لماذا هذه البروتين الحامي مهم
يُطلَق على البروتين p53 غالبًا اسم «حارس الجينوم» لأنه يساعد الخلايا السليمة على إصلاح الضرر ويمنع الخلايا المتضررة من التحول إلى خلايا سرطانية. تشرح هذه المقالة الاستعراضية كيف يعمل p53، ولماذا يفشل كثيرًا في السرطان، وكيف يتعلّم العلماء الآن استهداف ما كان يُعتقد طويلاً أنه «غير قابل للعلاج» بالأدوية. وتستعرض أيضًا وصلات مفاجئة بين p53 وحالات مثل مرض ألزهايمر والسكري وأمراض القلب، وتستقصي علاجات جديدة تحاول إصلاح إخفاقات p53 أو تجاوزها.
مفتّش السلامة الداخلي للخلية
في الظروف الطبيعية، تحافظ الخلايا على مستويات منخفضة من p53 عبر نظام إعادة تدوير داخلي. عندما يتعرض الخلايا لضغط — مثل تلف الحمض النووي أو نقص الأكسجين أو إشارات تحفّز السرطان — يتراكم p53 بسرعة ويفعّل العديد من الجينات. هذه الجينات توقف انقسام الخلايا، وتطلق إصلاح الحمض النووي، وتعدّل الأيض، أو، إذا كان الضرر كبيرًا جدًا، تدفع الخلية إلى تقاعد دائم (الهرم الخلوي) أو موت مبرمج متحكم به (الاستماتة). بهذه الطريقة يحافظ p53 على ثبات الشيفرة الوراثية ويمنع تكاثر الخلايا المتضررة. كما يؤثر على أشكال أحدث من موت الخلايا، مثل الفيروسبِتوز (ferroptosis)، ويشكّل البيئة المناعية المحيطة بالأورام، مساعدًا خلايا الجهاز المناعي على التعرف على الخلايا السرطانية ومهاجمتها.
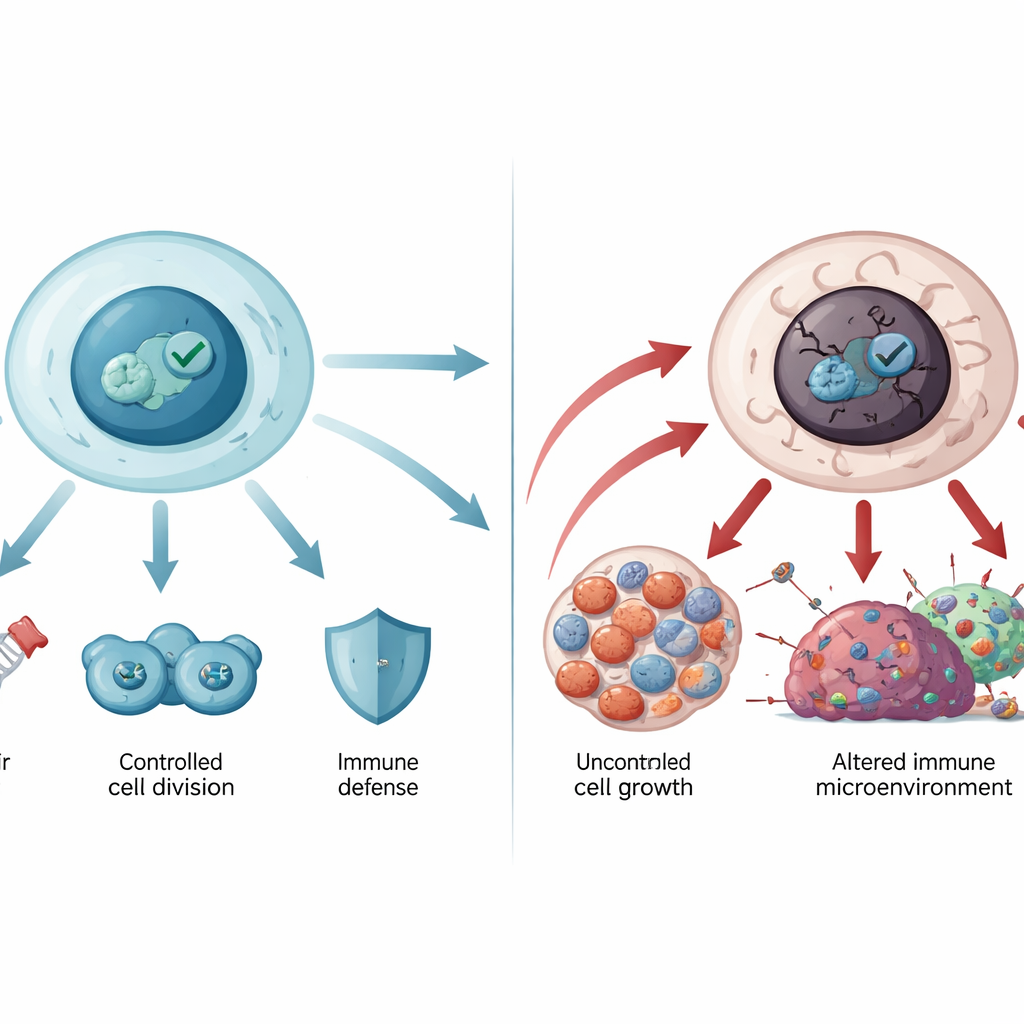
عندما ينحرف الحارس عن مساره
الجين المسؤول عن ترميز p53، TP53، هو الجين الأكثر تعرضًا للطفرات في سرطانات الإنسان. معظم هذه الطفرات هي تغييرات في حمض أميني واحد في الجزء الوسطي المسؤول عن ربط الحمض النووي في البروتين. بعض الطفرات تضعف قبضة p53 على الحمض النووي، بينما تزعزع بعضها الآخر استقراره فتنهار بنيته وتتجمع في عقيدات تشبه الأميلويد، كما يُرى في أمراض التنكّس العصبي. لا يفقد p53 المتحور دوره الوقائي فحسب، بل قد يكسب أيضًا أنشطة جديدة مشجعة للسرطان: يمكن أن يشجع النمو غير المنضبط، ويساعد خلايا الورم على مقاومة الموت والعلاج الكيميائي، ويعيد تشكيل الأيض لتغذية الأورام، ويُضعف المناعة المضادة للورم. الطفرات الخَلَقية في TP53 تقوم بدورها في متلازمة لي‑فراوميني وغيرها من الاضطرابات الوراثية النادرة ذات المخاطر العالية للسرطان، ما يبيّن مدى أهمية هذا المسار للحماية مدى الحياة.
ما وراء السرطان: روابط بالدماغ والأيض والقلب
نظرًا لأن p53 يتحكم في موت الخلايا واستجابات الضغط واستخدام الطاقة، يمتد تأثيره إلى ما هو أبعد من السرطان. في الدماغ، رُبطت نشاطات p53 غير الطبيعية بمرض ألزهايمر وباركنسون وهنتنغتون والتصلّب الجانبي الضموري والتصلّب المتعدد، غالبًا عبر تفاعلات مع بروتينات مرتبطة بالأمراض وعن طريق تعزيز فقدان مفرط للخلايا العصبية الضعيفة. في الأيض، يساعد p53 على تنظيم تخزين الدهون وسكر الدم ودهون الكبد؛ وبحسب السياق، قد يحمي من السمنة والسكري أو يساهم في مقاومة الإنسولين ومرض الكبد الدهني. في القلب والأوعية الدموية، يؤثر p53 على بقاء الخلايا والندب وتكوّن اللويحات، مؤديًا أدوارًا معقدة في فشل القلب، وإصابة القلب بالسكري، وتصلب الشرايين. تعني هذه التأثيرات الواسعة أن أي محاولة لتعزيز أو حجب p53 يجب أن توازن بين فوائد مكافحة السرطان والأضرار المحتملة للأنسجة السليمة.
طرق جديدة لعلاج «ما لا يُعالَج»
لعقود، اعتُبر p53 معقّدًا جدًا ومركزيًا للغاية بحيث لا يمكن استهدافه بأمان بأدوية. هذا التصور يتغيّر. إحدى الاستراتيجيات الرئيسية تهدف إلى «إنقاذ» p53 المتحوّر بتثبيت بنيته كي يتصرف أشبه بالبروتين الطبيعي؛ من الأمثلة PRIMA‑1/APR‑246 وثنائي أكسيد الزرنيخ وجزيئات مفصّلة لمطابقة طفريات نقاط ساخنة محددة مثل Y220C أو R175H. نهج آخر هو رفع مستويات p53 الطبيعي في الأورام التي لا تزال تحمل جين TP53 سليمًا عن طريق حجب المنظّمات السالبة MDM2 وMDM4؛ وهناك العديد من مثبطات هذين البروتينين التي تُؤخذ عن طريق الفم وتُجرب سريريًا. تكتيك ثالث يحاول نزع اعتماد خلايا الورم على p53 المتحوّر بتشجيع تحلّله عبر مثبطات الصدمة الحراريّة ومثبطات ديأسيتلة الهستونات أو أدوية الستاتين الشائعة الاستخدام. بالتوازي، تُطوَّر لقاحات وخلايا شجيرية مهندسة وأجسام مضادة شديدة التحديد لمساعدة الجهاز المناعي على التعرّف على الخلايا المحمَّلة بـ p53异常.
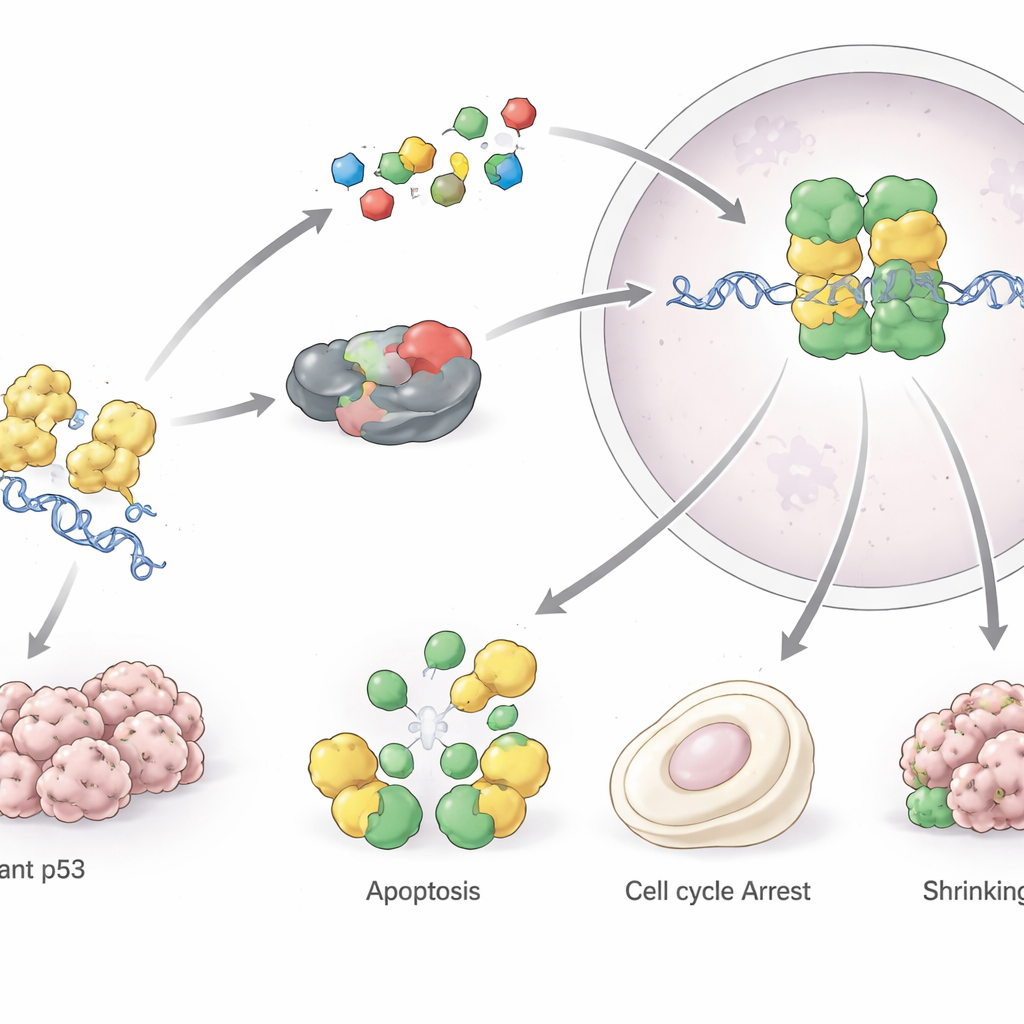
نظرة مستقبلية: من الخرائط إلى الأدوية
تخلص المقالة إلى أن p53 انتقل من كونه فضولًا بيولوجيًا محضًا إلى هدف علاجي واقعي، لكنه يتطلب دقّة. تنوّع طفرات TP53 وطبيعة أدوار p53 ذات الحدين في الأنسجة الطبيعية يجعل العلاجات الشاملة غير مرجّحة. بدلًا من ذلك، يتصور المؤلفون تركيبات من جزيئات صغيرة ومناعاتية وأدوات تحرير جيني موجّهة بواسطة علم الأنظمة والتعلّم الآلي لملاءمة الاستراتيجية المناسبة لكل سلك خلوي للورم. إذا نجحت هذه الجهود، فالبدائل أو المستعيدات لوظيفة p53 قد تغيّر مسار العلاج ليس فقط للعديد من السرطانات، بل وربما لبعض الأمراض غير السرطانية المرتبطة بهذا البروتين الحامي المحوري.
الاستشهاد: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
الكلمات المفتاحية: p53, طفرات TP53, علاجات السرطان, مسارات كابتة الأورام, أدوية مستهدفة لـ p53