Clear Sky Science · nl
p53: van inzicht in zijn structuur tot vooruitgang in therapeutische targeting
Waarom dit waakzame eiwit er toe doet
Het eiwit p53 wordt vaak de “bewaker van het genoom” genoemd omdat het gezonde cellen helpt beschadigingen te herstellen en beschadigde cellen verhindert kanker te worden. Dit overzichtsartikel legt uit hoe p53 werkt, waarom het zo vaak faalt bij kanker, en hoe wetenschappers nu leren geneesmiddelen te ontwikkelen tegen iets dat lange tijd als “onbenaderbaar” gold. Het belicht ook verrassende verbanden tussen p53 en aandoeningen zoals de ziekte van Alzheimer, diabetes en hartziekten, en biedt een overzicht van nieuwe behandelingen die proberen p53‑fouten te herstellen of te omzeilen.
De interne veiligheidsinspecteur van de cel
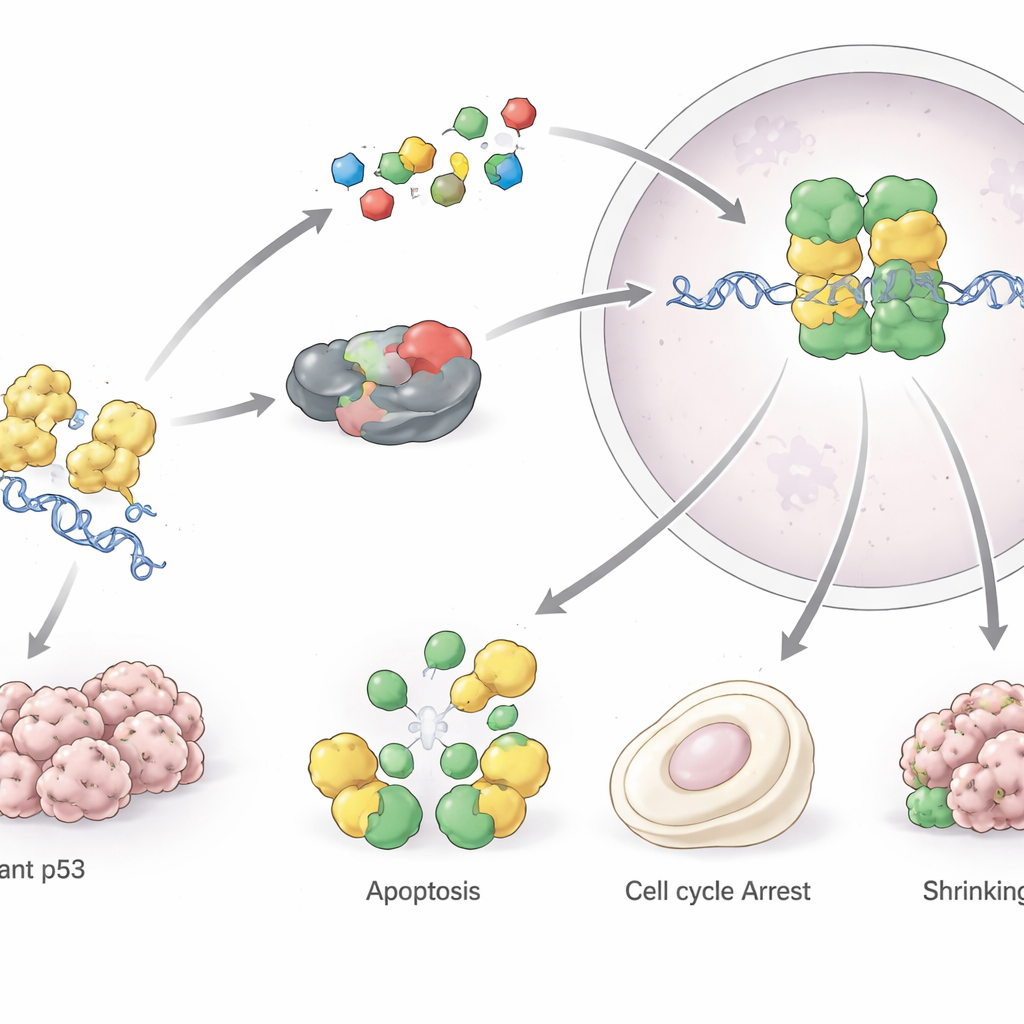
Onder normale omstandigheden houden cellen p53‑niveaus laag via een ingebouwd afbraaksysteem. Wanneer stress optreedt—zoals DNA‑schade, lage zuurstof of kankerverhogende signalen—hoopt p53 zich snel op en schakelt vele genen in. Deze genen remmen celdeling, zetten DNA‑herstel in gang, passen het metabolisme aan of, als de schade te groot is, sturen de cel naar permanente pensionering (senescentie) of gecontroleerde celdood (apoptose). Op deze manier houdt p53 de genetische code stabiel en voorkomt het dat beschadigde cellen zich voortplanten. Het beïnvloedt ook nieuwere vormen van celdood, zoals ferroptose, en vormt de immuunomgeving rond tumoren, waardoor immuuncellen kankercellen beter kunnen herkennen en aanvallen.
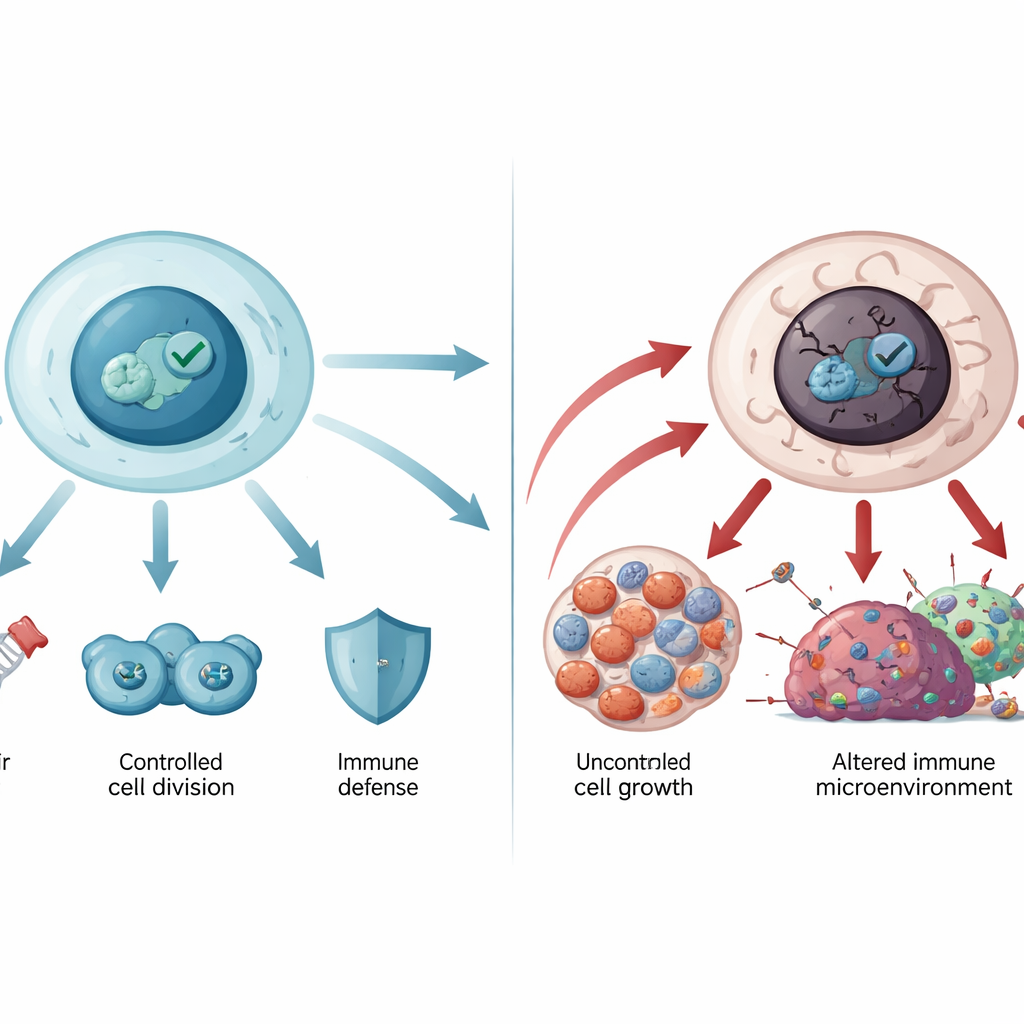
Wanneer de bewaker ontspoort
Het gen dat p53 codeert, TP53, is het meest frequent gemuteerde gen in menselijke kankers. De meeste van deze mutaties zijn veranderingen van één aminozuur in het centrale DNA‑bindende deel van het eiwit. Sommige mutaties verzwakken p53’s binding aan DNA, terwijl andere zijn structuur destabiliseren zodat het ontvouwt en samenklontert in aggregaten die lijken op amyloïde, zoals bij neurodegeneratieve ziekten. Gemuteerd p53 verliest niet alleen zijn beschermende rol, maar kan ook nieuwe kankerbevorderende functies krijgen: het kan ongeremde groei stimuleren, tumorcellen helpen te weerstaan aan celdood en chemotherapie, het metabolisme hervormen om tumoren te voeden en de anti‑tumorimmuniteit verzwakken. Germinale TP53‑mutaties liggen ten grondslag aan het Li‑Fraumeni‑syndroom en andere zeldzame erfelijke aandoeningen met hoog kanker‑risico, wat laat zien hoe cruciaal deze route is voor levenslange bescherming.
Voorbij kanker: verbanden met brein, metabolisme en hart
Aangezien p53 celdood, stressreacties en energiegebruik reguleert, reikt zijn invloed verder dan alleen kanker. In de hersenen is abnormale p53‑activiteit in verband gebracht met Alzheimer, Parkinson, Huntington, ALS en multiple sclerose, vaak via interacties met ziektegerelateerde eiwitten en door het bevorderen van overmatige verlies van kwetsbare neuronen. In het metabolisme helpt p53 vetopslag, bloedsuiker en levervet te reguleren; afhankelijk van de context kan het beschermen tegen obesitas en diabetes of bijdragen aan insulineresistentie en leververvetting. In hart en bloedvaten beïnvloedt p53 celsurvival, littekenvorming en plaquevorming, en speelt het complexe rollen bij hartfalen, diabetische hartschade en atherosclerose. Deze veelomvattende effecten betekenen dat elke poging om p53 te versterken of te remmen een afweging vereist tussen antikankereffecten en mogelijk schade aan normale weefsels.
Nieuwe manieren om het “onbenaderbare” te targeten
Decennialang werd p53 gezien als te complex en te centraal om veilig met geneesmiddelen te richten. Dat beeld verandert. Een belangrijke strategie is het “redden” van gemuteerd p53 door zijn vouwing te stabiliseren zodat het meer als het normale eiwit functioneert; voorbeelden zijn PRIMA‑1/APR‑246, arseentrioxide en moleculen toegespitst op specifieke hotspot‑mutaties zoals Y220C of R175H. Een andere benadering is om de niveaus van normaal p53 in tumoren die nog een intact TP53‑gen hebben, te verhogen door zijn negatieve regulatoren MDM2 en MDM4 te blokkeren; verschillende orale remmers van deze eiwitten zitten in klinische onderzoeken. Een derde tactiek probeert tumorcellen te ontdoen van hun afhankelijkheid van gemuteerd p53 door de afbraak ervan te bevorderen met behulp van heat‑shock en histon‑deacetylaseremmers of veelgebruikte statines. Parallel daaraan worden vaccins, gemodificeerde dendritische cellen en zeer specifieke antilichamen ontwikkeld om het immuunsysteem te helpen cellen met overtollig abnormaal p53 te herkennen.
Vooruitkijken: van kaarten naar geneesmiddelen
Het artikel besluit dat p53 is verschoven van een puur biologische curiositeit naar een realistisch therapeutisch doel, maar één dat precisie vereist. De diversiteit aan TP53‑mutaties en de dubbelzinnige aard van p53’s rollen in normale weefsels maken uniforme behandelingen onwaarschijnlijk. In plaats daarvan voorzien de auteurs combinaties van kleine moleculen, immunotherapieën en genbewerkingsinstrumenten, aangestuurd door systeembiologie en machine learning, om de juiste p53‑gerichte strategie op het bedradingstype van elke tumor af te stemmen. Slagen deze inspanningen, dan zouden geneesmiddelen die p53‑functie herstellen of compenseren de zorg kunnen transformeren, niet alleen voor veel kankers, maar mogelijk ook voor sommige niet‑kankerziekten die met dit sleutel‑bewakereiwit zijn verbonden.
Bronvermelding: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Trefwoorden: p53, TP53-mutaties, kankertherapieën, tumorsuppressorroutes, p53-gerichte geneesmiddelen