Clear Sky Science · sv
p53: från förståelsen av dess struktur till framsteg inom terapeutisk riktning
Varför detta väktarprotein betyder så mycket
Proteinet p53 kallas ofta för ”genomets väktare” eftersom det hjälper friska celler att reparera skador och hindrar skadade celler från att bli cancerösa. Den här översiktsartikeln förklarar hur p53 fungerar, varför det så ofta sviktar vid cancer, och hur forskare nu lär sig att påverka något som länge ansetts vara ”obehandlingsbart”. Den belyser också överraskande kopplingar mellan p53 och tillstånd som Alzheimers sjukdom, diabetes och hjärtsjukdom, och ger en översikt över nya behandlingar som försöker åtgärda eller kringgå p53:s fel.
Cellens interna säkerhetsinspektör
Under normala förhållanden hålls p53-nivåerna låga genom ett inbyggt återvinningssystem. När stress inträffar — såsom DNA-skada, låg syretillgång eller cancertumörerande signaler — ackumuleras p53 snabbt och aktiverar många gener. Dessa gener stannar celldelningen, utlöser DNA-reparation, justerar metabolismen eller, om skadan är för stor, driver cellen in i permanent pensionering (senescens) eller kontrollerad celldöd (apoptos). På så sätt håller p53 den genetiska koden stabil och förhindrar att skadade celler förökar sig. Det påverkar även nyare former av celldöd som ferroptos och formar immummiljön runt tumörer, vilket hjälper immunceller att känna igen och angripa cancerösa celler.
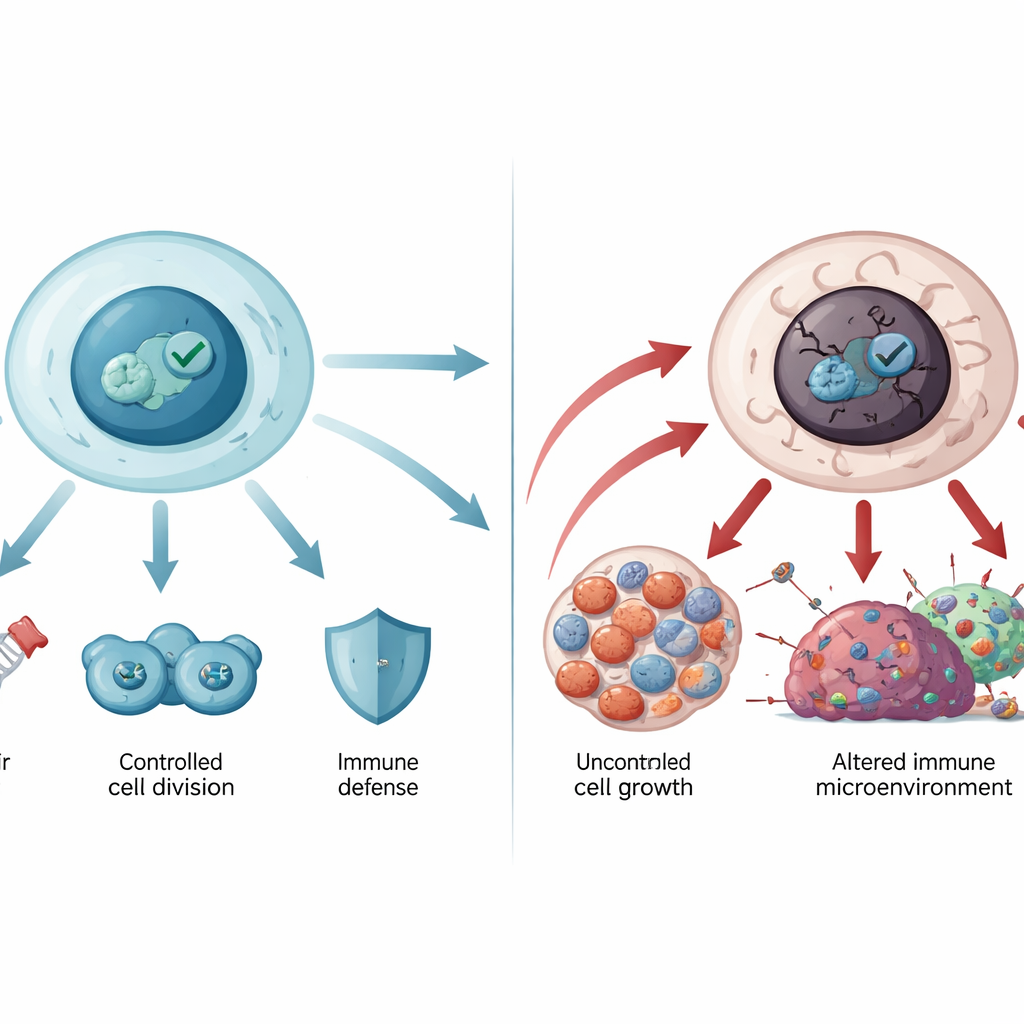
När väktaren går fel
Genen som kodar för p53, TP53, är den mest frekvent muterade genen i mänskliga cancerformer. De flesta av dessa mutationer är enstaka aminosyreförändringar i proteinets centrala DNA-bindande del. Vissa mutationer försvagar p53:s bindning till DNA, medan andra destabiliserar dess struktur så att det veckas upp och klumpar ihop sig i aggregat som liknar amyloid, liknande vad som ses i neurodegenerativa sjukdomar. Mutant p53 förlorar inte bara sin skyddande roll utan kan även vinna nya cancerfrämjande funktioner: det kan uppmuntra okontrollerad tillväxt, hjälpa tumörceller att motstå celldöd och kemoterapi, omforma metabolismen för att mata tumörer och försvaga antitumörimmuniteten. Germline-mutationer i TP53 ligger bakom Li–Fraumeni-syndromet och andra sällsynta ärftliga störningar med hög cancerrisk, vilket visar hur avgörande denna väg är för livslångt skydd.
Bortom cancer: kopplingar till hjärnan, metabolism och hjärta
Eftersom p53 styr celldöd, stressreaktioner och energianvändning sträcker sig dess inflytande bortom cancer. I hjärnan har onormal p53-aktivitet kopplats till Alzheimers, Parkinsons, Huntingtons sjukdom, ALS och multipel skleros, ofta genom interaktioner med sjukdomsrelaterade proteiner och genom att främja överdriven förlust av sårbara neuroner. I ämnesomsättningen hjälper p53 till att reglera fettlagring, blodsocker och leverfett; beroende på sammanhang kan det antingen skydda mot fetma och diabetes eller bidra till insulinresistens och fettlever. I hjärtat och blodkärlen påverkar p53 cellsöverlevnad, ärrbildning och plackbildning och har komplexa roller i hjärtsvikt, diabetisk hjärtskada och ateroskleros. Dessa vittgående effekter innebär att varje försök att öka eller blockera p53 måste väga anticancerfördelar mot potentiell skada på normala vävnader.
Nya sätt att rikta den ”obehandlingsbara”
I årtionden sågs p53 som för komplext och för centralt för att säkert rikta med läkemedel. Den synen förändras. En huvudstrategi syftar till att ”rädda” muterat p53 genom att stabilisera dess form så att det beter sig mer som det normala proteinet; exempel inkluderar PRIMA‑1/APR‑246, arseniktrioxid och molekyler anpassade till specifika hotspot‑mutanter såsom Y220C eller R175H. En annan strategi är att höja nivåerna av normalt p53 i tumörer som fortfarande har en intakt TP53-gen genom att blockera dess negativa regulatorer MDM2 och MDM4; flera orala hämmare av dessa proteiner befinner sig i kliniska prövningar. En tredje taktik försöker beröva tumörceller deras beroende av muterat p53 genom att uppmuntra dess nedbrytning med hjälp av värmechock‑ och histon‑deacetylashämmare eller vanligt använda statiner. Parallellt utvecklas vacciner, genmodifierade dendritiska celler och mycket specifika antikroppar för att hjälpa immunsystemet känna igen celler som är överbelastade med onormalt p53.
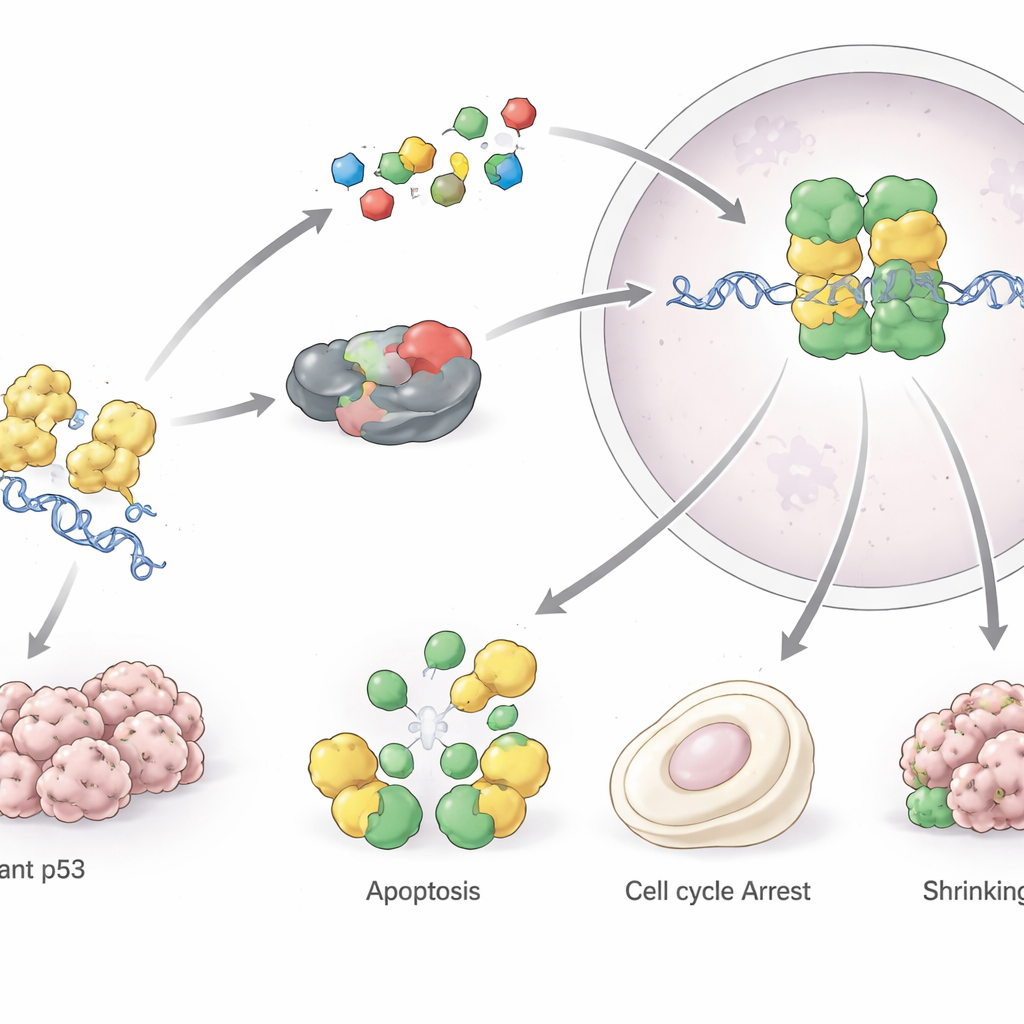
Framåt: från kartor till läkemedel
Artikeln slår fast att p53 har gått från att vara en rent biologisk kuriositet till ett realistiskt terapeutiskt mål, men ett som kräver precision. Mångfalden av TP53‑mutationer och p53:s tvåeggade roller i normala vävnader gör en universallösning osannolik. Istället ser författarna kombinationer av småmolekyler, immunterapier och genredigeringsverktyg vägledda av systembiologi och maskininlärning för att matcha rätt p53‑inriktade strategi med varje tumörs nätverk. Om dessa ansträngningar lyckas kan läkemedel som återställer eller kompenserar för p53‑funktion förvandla vården inte bara för många cancerformer utan potentiellt också för vissa icke‑cancerrelaterade sjukdomar kopplade till detta centrala väktarprotein.
Citering: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Nyckelord: p53, TP53-mutationen, cancerterapier, tumörsuppressorvägar, p53-riktade läkemedel