Clear Sky Science · pt
p53: da compreensão de sua estrutura aos avanços em diretrizes terapêuticas
Por que essa proteína guardiã importa
A proteína p53 é frequentemente chamada de “guardião do genoma” porque ajuda células saudáveis a reparar danos e impede que células danificadas se tornem cancerosas. Esta revisão explica como p53 funciona, por que ele falha com tanta frequência no câncer e como os cientistas vêm aprendendo a desenvolver fármacos para algo que por muito tempo foi considerado “intratável”. O texto também explora ligações inesperadas entre p53 e condições como doença de Alzheimer, diabetes e doenças cardíacas, além de revisar novos tratamentos que tentam consertar ou contornar as falhas de p53.
O inspetor de segurança interno da célula
Em condições normais, as células mantêm níveis baixos de p53 por meio de um sistema de reciclagem interno. Quando surge estresse — como dano ao DNA, baixa oferta de oxigênio ou sinais promotores de câncer — p53 se acumula rapidamente e ativa muitos genes. Esses genes suspendem a divisão celular, disparam a reparação do DNA, ajustam o metabolismo ou, se o dano for excessivo, conduzem a célula a uma aposentadoria permanente (senescência) ou à morte controlada (apoptose). Dessa forma, p53 mantém o código genético estável e evita que células danificadas se multipliquem. Ele também influencia formas mais recentes de morte celular, como ferroptose, e molda o ambiente imune ao redor dos tumores, ajudando células imunes a reconhecer e atacar células cancerosas.
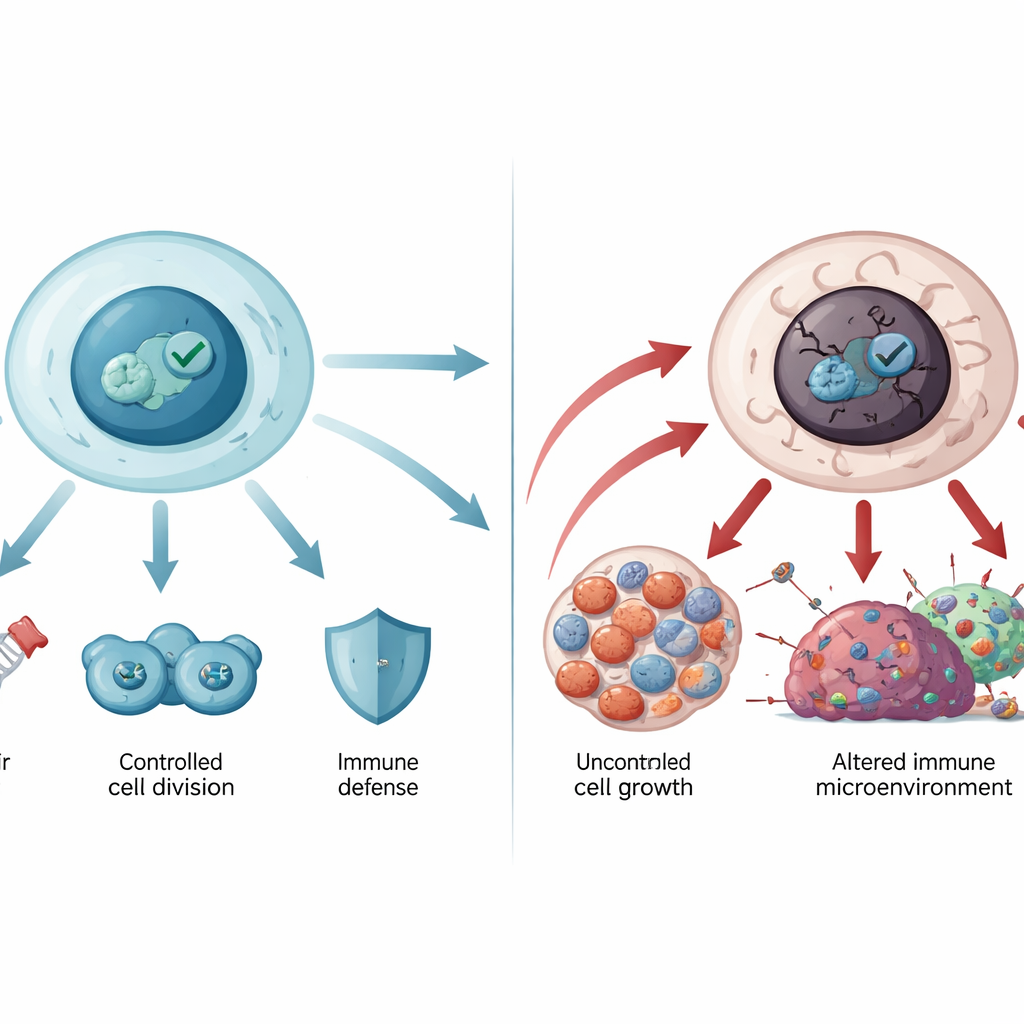
Quando o guardião sai do controle
O gene que codifica p53, TP53, é o mais frequentemente mutado nos cânceres humanos. A maioria dessas mutações são trocas de um único aminoácido na região central de ligação ao DNA da proteína. Algumas mutações enfraquecem a capacidade de p53 de se ligar ao DNA, enquanto outras desestabilizam sua estrutura, fazendo‑o desenrolar e agregar‑se em aglomerados semelhantes a amiloides, como os observados em doenças neurodegenerativas. O p53 mutante não apenas perde sua função protetora, como também pode adquirir novas atividades promotoras de câncer: pode incentivar crescimento descontrolado, ajudar células tumorais a resistir à morte e à quimioterapia, remodelar o metabolismo para nutrir tumores e enfraquecer a imunidade antitumoral. Mutações germinativas em TP53 estão na base da síndrome de Li‑Fraumeni e de outros transtornos hereditários raros com alto risco de câncer, evidenciando o quão crucial essa via é para a proteção ao longo da vida.
Além do câncer: conexões com cérebro, metabolismo e coração
Como p53 controla morte celular, respostas ao estresse e uso de energia, sua influência vai além do câncer. No cérebro, atividade anormal de p53 tem sido associada à doença de Alzheimer, Parkinson, Huntington, ELA e esclerose múltipla, frequentemente por meio de interações com proteínas relacionadas às doenças e por promover perda excessiva de neurônios vulneráveis. No metabolismo, p53 ajuda a regular armazenamento de gordura, glicemia e gordura hepática; dependendo do contexto, pode tanto proteger contra obesidade e diabetes quanto contribuir para resistência à insulina e doença hepática gordurosa. No coração e nos vasos, p53 afeta sobrevivência celular, cicatrização e formação de placas, desempenhando papéis complexos em insuficiência cardíaca, dano cardíaco diabético e aterosclerose. Esses efeitos amplos significam que qualquer tentativa de estimular ou bloquear p53 precisa equilibrar benefícios anticâncer com possíveis danos a tecidos normais.
Novas maneiras de atacar o “intratável”
Durante décadas, p53 foi visto como demasiado complexo e central para ser um alvo seguro de fármacos. Essa visão está mudando. Uma estratégia importante busca “resgatar” p53 mutante estabilizando sua conformação para que se comporte mais como a proteína normal; exemplos incluem PRIMA‑1/APR‑246, trióxido de arsênio e moléculas desenhadas para mutantes hotspot específicos, como Y220C ou R175H. Outra abordagem é elevar os níveis de p53 normal em tumores que ainda têm o gene TP53 intacto, bloqueando seus reguladores negativos MDM2 e MDM4; vários inibidores orais dessas proteínas estão em ensaios clínicos. Uma terceira tática tenta eliminar a dependência das células tumorais do p53 mutante incentivando sua degradação com inibidores de choque térmico e de histona‑desacetilase ou com estatinas de uso corrente. Em paralelo, vacinas, células dendríticas geneticamente modificadas e anticorpos altamente específicos estão sendo desenvolvidos para ajudar o sistema imune a reconhecer células sobrecarregadas por p53 anormal.
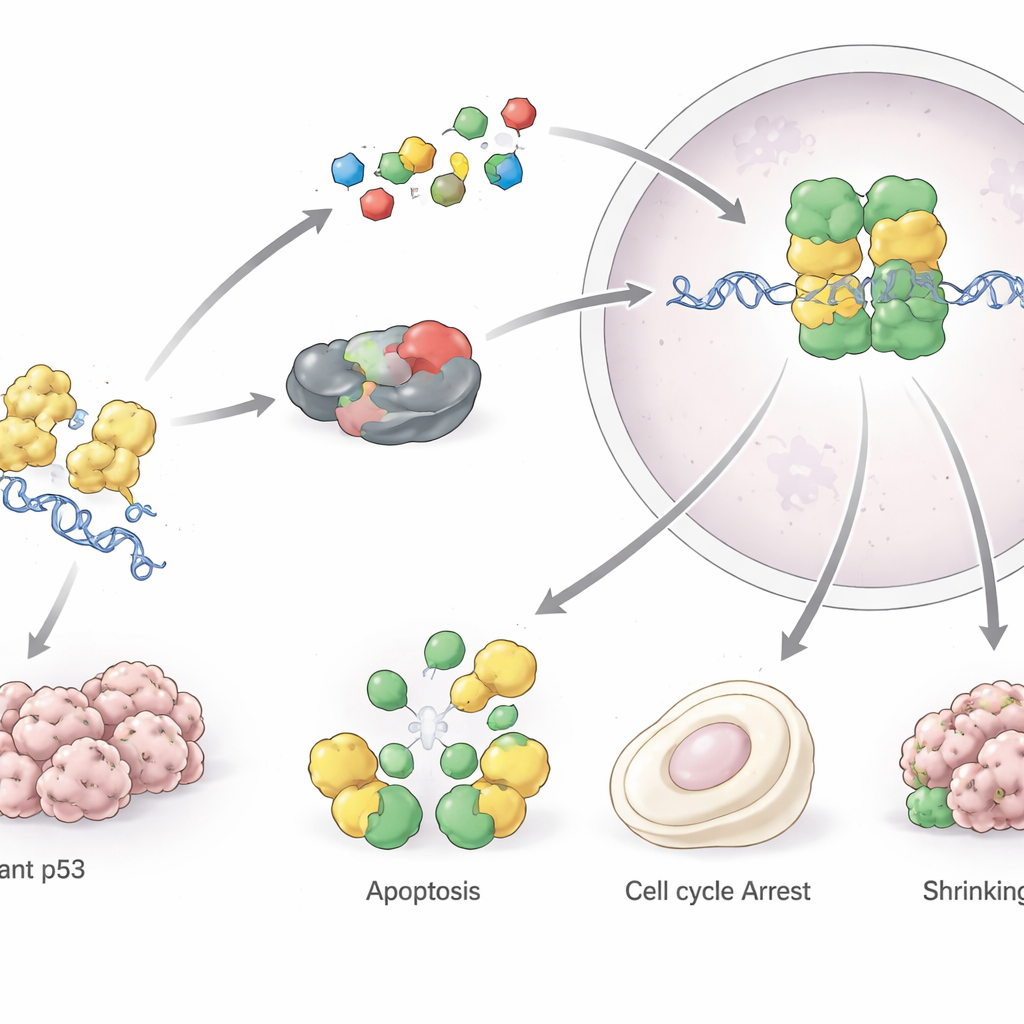
Olhando adiante: de mapas a medicamentos
O artigo conclui que p53 deixou de ser apenas uma curiosidade biológica para se tornar um alvo terapêutico realista, porém que exige precisão. A diversidade de mutações em TP53 e a natureza de dois gumes das funções de p53 em tecidos normais tornam improvável um tratamento único para todos. Em vez disso, os autores imaginam combinações de pequenas moléculas, imunoterapias e ferramentas de edição gênica orientadas por biologia de sistemas e aprendizado de máquina para combinar a estratégia direcionada a p53 certa com a arquitetura de cada tumor. Se esses esforços forem bem‑sucedidos, fármacos que restaurem ou compensem a função de p53 poderão transformar o tratamento não apenas de muitos cânceres, mas potencialmente de algumas doenças não cancerosas ligadas a essa proteína guardiã pivotal.
Citação: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Palavras-chave: p53, mutações TP53, terapêuticas contra o câncer, vias supressoras de tumor, fármacos direcionados a p53