Clear Sky Science · es
p53: desde la comprensión de su estructura hasta los avances en su direccionamiento terapéutico
Por qué importa esta proteína guardiana
La proteína p53 suele llamarse el “guardián del genoma” porque ayuda a las células sanas a reparar daños y evita que las células dañadas se vuelvan cancerosas. Este artículo de revisión explica cómo funciona p53, por qué falla tan a menudo en el cáncer y cómo los científicos están aprendiendo a dirigir con fármacos lo que durante mucho tiempo se consideró “indruggable” (difícil de abordar farmacológicamente). También explora vínculos sorprendentes entre p53 y enfermedades como el Alzheimer, la diabetes y las cardiopatías, y repasa nuevos tratamientos que intentan corregir o sortear las fallas de p53.
El inspector de seguridad interno de la célula
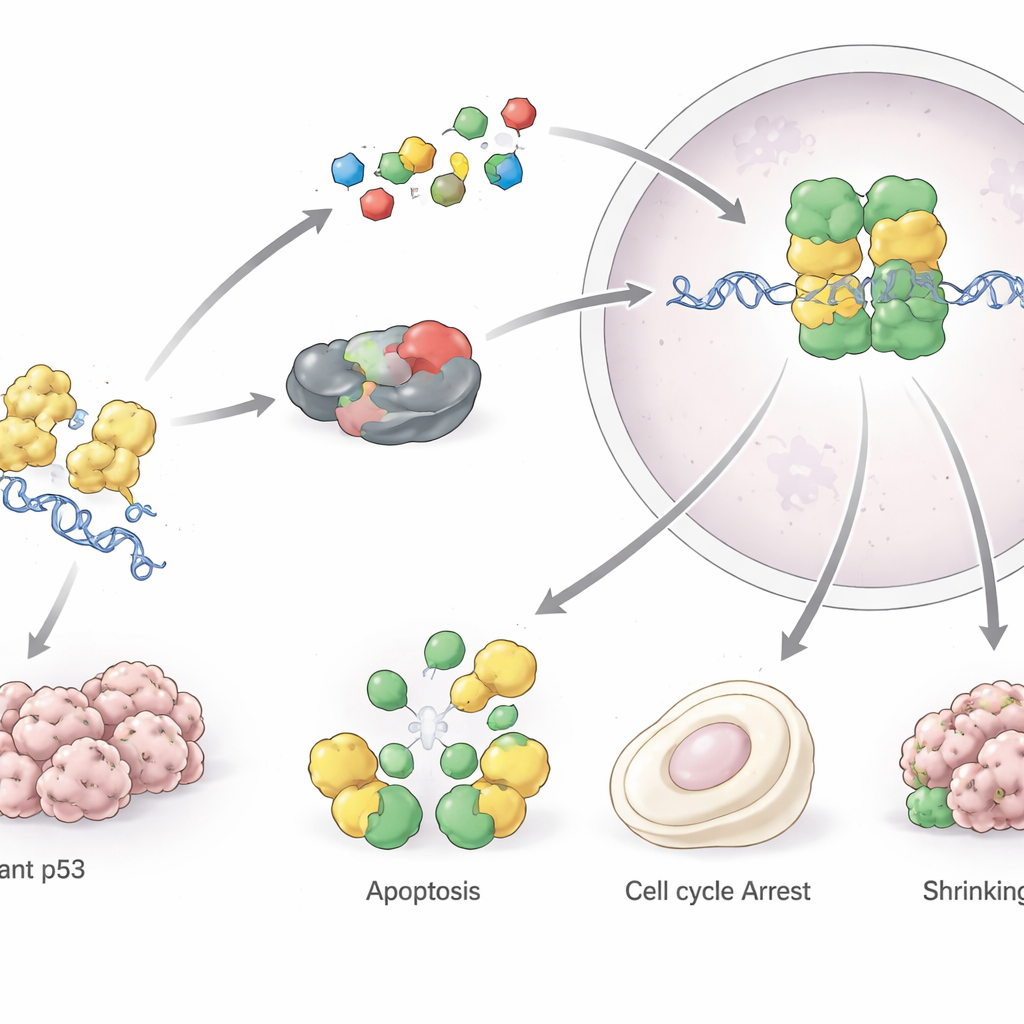
En condiciones normales, las células mantienen bajos los niveles de p53 mediante un sistema de reciclaje incorporado. Cuando aparece el estrés—como daño en el ADN, falta de oxígeno o señales que favorecen el cáncer—p53 se acumula rápidamente y activa numerosos genes. Estos genes detienen la división celular, desencadenan la reparación del ADN, ajustan el metabolismo o, si el daño es demasiado grande, llevan a la célula a una jubilación permanente (senescencia) o a la muerte controlada (apoptosis). De este modo, p53 mantiene estable el código genético y evita que las células dañadas se multipliquen. También influye en formas más recientes de muerte celular, como la ferroptosis, y modula el entorno inmune alrededor de los tumores, ayudando a las células inmunitarias a reconocer y atacar las células cancerosas.
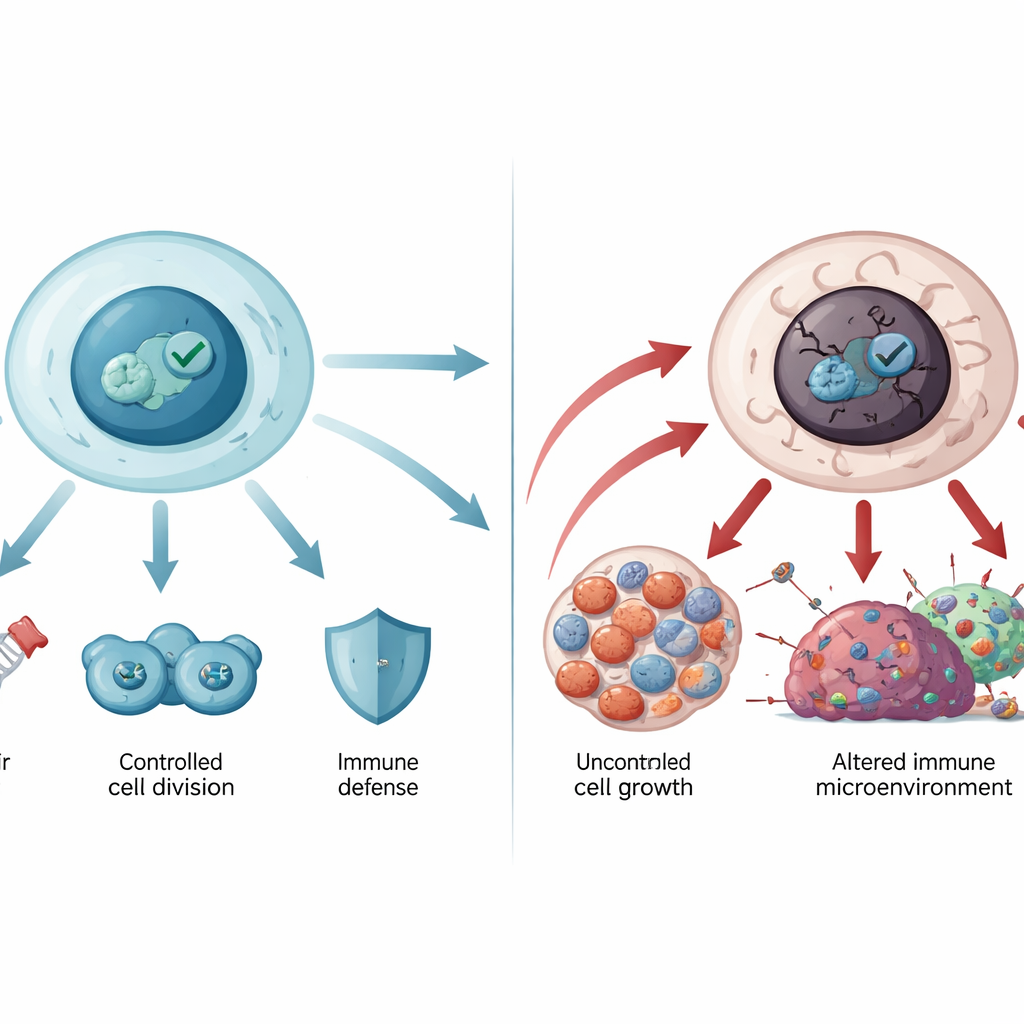
Cuando el guardián se vuelve rebelde
El gen que codifica p53, TP53, es el gen con mayor frecuencia de mutación en los cánceres humanos. La mayoría de estas mutaciones son cambios de un solo aminoácido en la región central de unión al ADN de la proteína. Algunas mutaciones debilitan la unión de p53 al ADN, mientras que otras desestabilizan su estructura para que se desplace y forme agregados parecidos a amiloides, como se observa en enfermedades neurodegenerativas. p53 mutante no sólo pierde su papel protector, sino que además puede adquirir nuevas actividades que promueven el cáncer: puede fomentar el crecimiento descontrolado, ayudar a las células tumorales a resistir la muerte celular y la quimioterapia, reconfigurar el metabolismo para alimentar los tumores y debilitar la inmunidad antitumoral. Las mutaciones germinales de TP53 subyacen al síndrome de Li‑Fraumeni y otros trastornos hereditarios raros con alto riesgo de cáncer, lo que muestra lo crucial que es esta vía para la protección a lo largo de la vida.
Más allá del cáncer: vínculos con el cerebro, el metabolismo y el corazón
Como p53 controla la muerte celular, las respuestas al estrés y el uso de energía, su influencia se extiende más allá del cáncer. En el cerebro, la actividad anómala de p53 se ha vinculado al Alzheimer, el Parkinson, la enfermedad de Huntington, la ELA y la esclerosis múltiple, a menudo mediante interacciones con proteínas relacionadas con estas enfermedades y promoviendo la pérdida excesiva de neuronas vulnerables. En el metabolismo, p53 ayuda a regular el almacenamiento de grasa, el azúcar en sangre y la grasa hepática; dependiendo del contexto, puede proteger frente a la obesidad y la diabetes o contribuir a la resistencia a la insulina y la esteatosis hepática. En el corazón y los vasos sanguíneos, p53 afecta la supervivencia celular, la cicatrización y la formación de placas, desempeñando papeles complejos en la insuficiencia cardíaca, el daño cardíaco diabético y la aterosclerosis. Estos efectos de amplio alcance implican que cualquier intento de potenciar o bloquear p53 debe equilibrar los beneficios antitumorales con el posible daño a tejidos normales.
Nuevas formas de dirigir a lo “indruggable”
Durante décadas, p53 se consideró demasiado complejo y demasiado central como para abordarlo de forma segura con fármacos. Esa visión está cambiando. Una estrategia principal pretende “rescatar” p53 mutante estabilizando su conformación para que se comporte más como la proteína normal; ejemplos incluyen PRIMA‑1/APR‑246, trióxido de arsénico y moléculas diseñadas para mutantes puntuales específicos como Y220C o R175H. Otro enfoque es elevar los niveles de p53 normal en tumores que aún conservan un gen TP53 intacto bloqueando sus reguladores negativos MDM2 y MDM4; varios inhibidores orales de estas proteínas están en ensayos clínicos. Una tercera táctica intenta despojar a las células tumorales de su dependencia de p53 mutante fomentando su degradación mediante inhibidores de chaperonas de choque térmico y de histona‑desacetilasas o con estatinas de uso común. En paralelo, se desarrollan vacunas, células dendríticas modificadas y anticuerpos muy específicos para ayudar al sistema inmune a reconocer células sobrecargadas de p53 anómalo.
Mirando hacia adelante: de los mapas a los fármacos
El artículo concluye que p53 ha pasado de ser una curiosidad puramente biológica a un objetivo terapéutico realista, pero que exige precisión. La diversidad de mutaciones en TP53 y la naturaleza ambivalente de los roles de p53 en tejidos normales hacen que los tratamientos universales sean improbables. En su lugar, los autores imaginan combinaciones de pequeñas moléculas, inmunoterapias y herramientas de edición génica guiadas por biología de sistemas y aprendizaje automático para adaptar la estrategia dirigida a p53 a la red particular de cada tumor. Si estos esfuerzos tienen éxito, los fármacos que restauren o compensen la función de p53 podrían transformar la atención no solo de muchos cánceres, sino potencialmente de algunas enfermedades no oncológicas vinculadas a esta proteína guardiana pivotal.
Cita: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Palabras clave: p53, mutaciones TP53, terapéutica del cáncer, vías supresoras de tumores, fármacos dirigidos a p53