Clear Sky Science · he
p53: מהבנת המבנה שלו ועד התקדמות בטיפול הממוקד
למה החלבון השומר חשוב
החלבון p53 נקרא לעתים קרובות "שומר הגנום" כיוון שהוא מסייע לתאים בריאים לתקן נזק ומונע מתאים פגועים להפוך לממאירים. מאמר סקירה זה מסביר כיצד p53 פועל, מדוע הוא נכשל כל כך לעתים קרובות בסרטן, וכיצד מדענים לומדים כעת לפתח תרופות נגד מטרה שנחשבה זמן רב כ"לא ניתנת לטיפול". הוא גם חוקר קשרים מפתיעים בין p53 ומחלות כמו אלצהיימר, סוכרת ומחלות לב, ובוחן טיפולים חדשים שמנסים לתקן או לעקוף את כשלונות p53.
בוחן הבטיחות הפנימי של התא
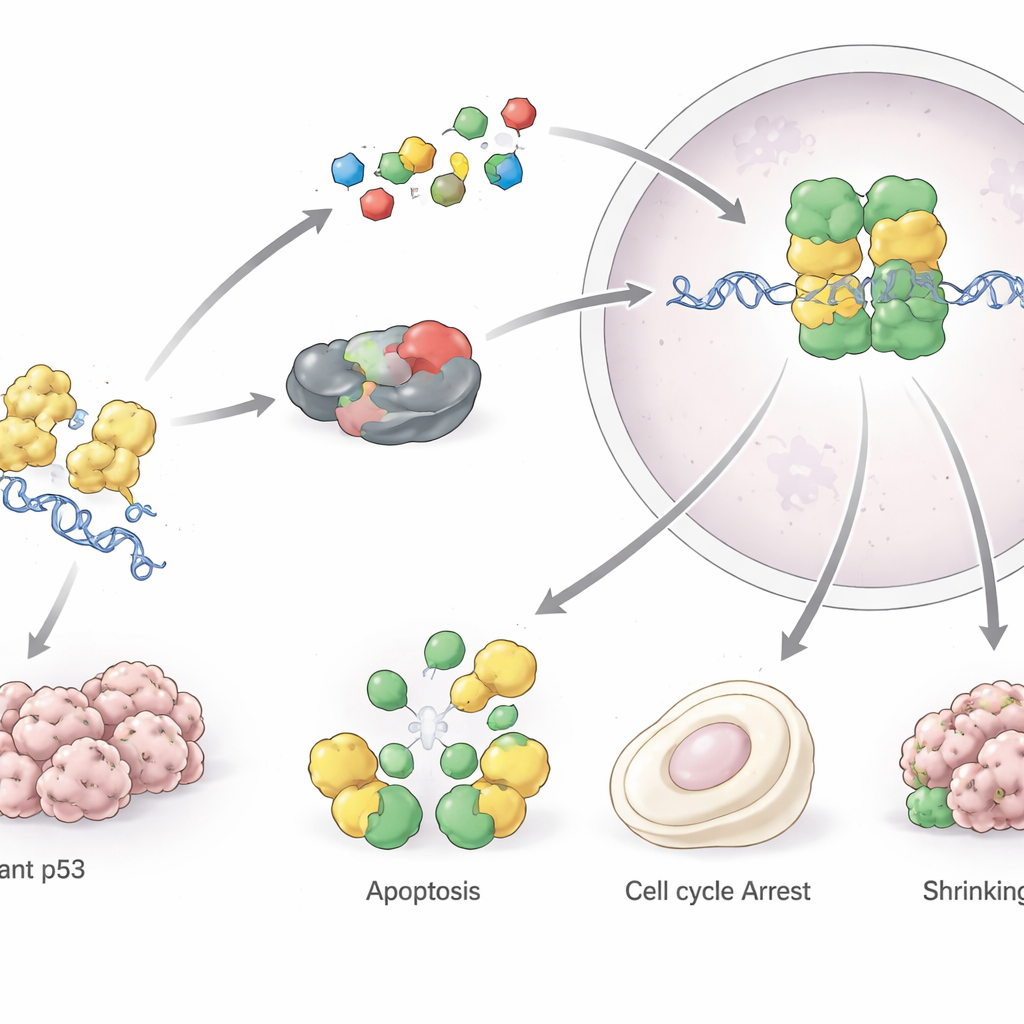
בתנאים רגילים, התאים שומרים על רמות נמוכות של p53 באמצעות מערכת מיחזור פנימית. כאשר מופיע לחץ — כמו נזק ל‑DNA, חוסר חמצן או אותות המעודדים סרטן — p53 מצטבר במהירות ומפעיל שפע של גנים. גנים אלה עוצרים את חלוקת התא, מעוררים תיקון DNA, מתאימים את המטבוליזם או, אם הנזק חמור מדי, דוחפים את התא לפנסיה קבועה (סנֵסֶנְס) או למוות מבוקר (א폽טוזיס). בכך p53 שומר על יציבות הקוד הגנטי ומונע ריבוי של תאים פגועים. הוא גם משפיע על צורות חדשות של מוות תאי, כמו פרוטאופטוזיס מסוג ferroptosis, ומעצב את סביבה החיסונית סביב הגידולים, מסייע לתאי החיסון לזהות ולתקוף תאים ממאירים.
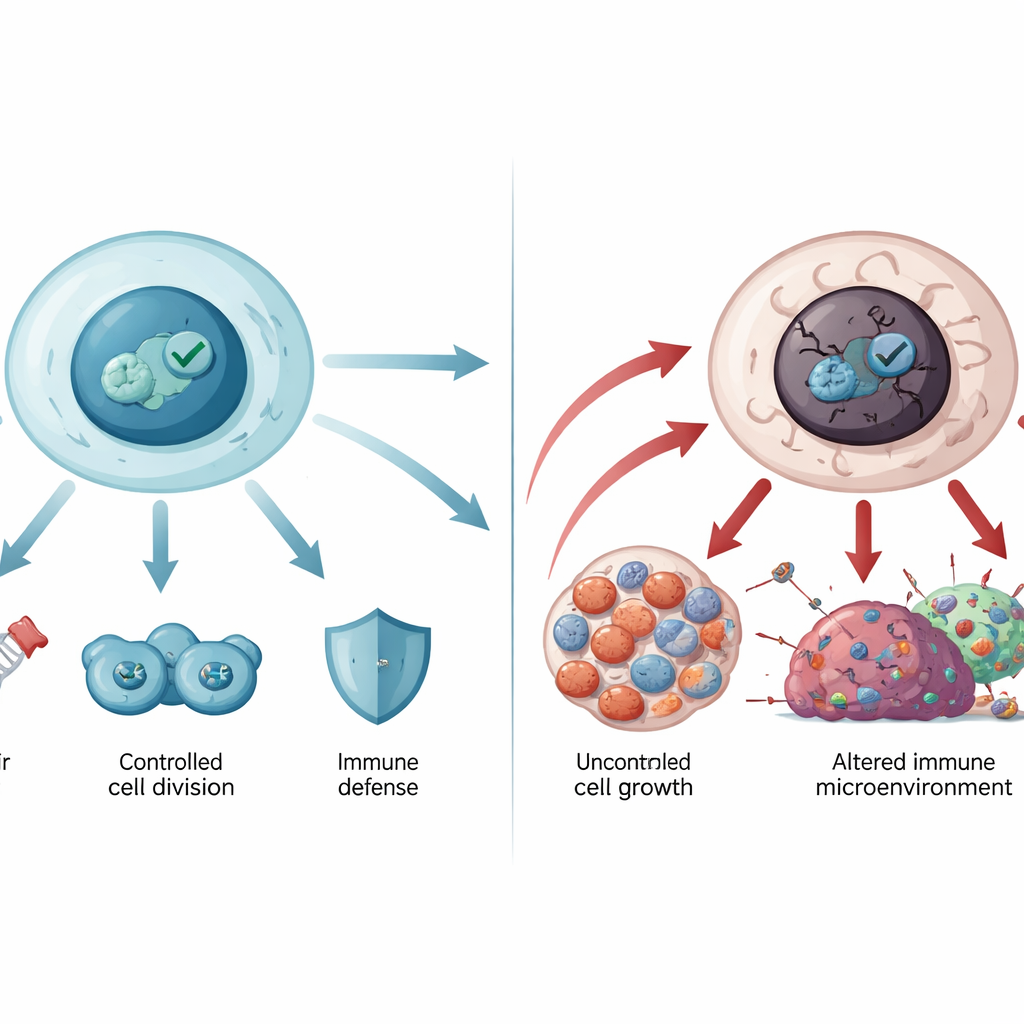
כשהשומר משתבש
הגן המקודד ל‑p53, TP53, הוא הגן המוטנטי השכיח ביותר בסרטן האנושי. רוב המוטציות הללו הן החלפות של חומצת אמינו יחידה בחלק המרכזי של החלבון האחראי לקשירת DNA. חלק מהמוטציות מחלישות את אחיזת p53 ל‑DNA, בעוד שאחרות מייצבות את המבנה באופן לקוי כך שהוא מתפרק ומצטבר באגרגטים הדומים לאמילואיד, כפי שנראה במחלות ניווניות עצביות. p53 המוטנטי לא רק מאבד את תפקידו המגן אלא עלול גם לרכוש פעילויות המעודדות סרטן: הוא יכול לעודד גדילה ללא בקרה, לסייע לתאי הגידול לעמוד בפני מוות תאי וכימותרפיה, לעצב מחדש את המטבוליזם כדי להאכיל את הגידולים ולהחליש את החיסון נגד גידולים. מוטציות זרעיות ב‑TP53 עומדות בבסיס תסמונת לי‑פרמני ומחלות תורשתיות נדירות נוספות עם סיכון גבוה לסרטן, מה שמדגים כמה חשוב מסלול זה להגנה ארוכת־חיים.
מעבר לסרטן: קשרים למוח, מטבוליזם ולב
מכיוון ש‑p53 שולט במוות תאי, בתגובות ללחץ ובשימוש באנרגיה, השפעתו חורגת מעבר לסרטן. במוח, פעילות p53 בלתי תקינה נקשרת לאלצהיימר, פרקינסון, הנטינגטון, ALS ולטרשת נפוצה, לעתים דרך אינטראקציות עם חלבונים הקשורים למחלות ולעידוד איבוד יתר של נוירונים רגישים. במטבוליזם, p53 מסייע בוויסות אחסון השומן, רמות סוכר בדם ושומן כבד; בהתאם להקשר, הוא יכול להגן מפני השמנה וסוכרת או לתרום לעמידות לאינסולין ולכבד שומני. בלב וכלי הדם, p53 משפיע על הישרדות תאים, צלקת והיווצרות פלאקים, ומשחק תפקידים מורכבים בכשל לב, נזק לבבי סוכרת ולטרשת עורקים. השפעות נרחבות אלה פירושן שכל ניסיון להגביר או לחסום את p53 חייב לאזן בין יתרונות אנטי‑סרטן לבין נזק אפשרי לרקמות בריאות.
דרכים חדשות לטפל ב"שלא ניתנת לטיפול"
בעשורים רבים נחשבה p53 למטרה מורכבת מדי ולרב מרכזית כדי לכוון אותה בבטחה בעזרת תרופות. תפיסה זו משתנה. אסטרטגיה מרכזית שואפת "להציל" p53 המוטנטי על‑ידי ייצוב צורתו כך שיתנהג יותר כמו החלבון התקין; דוגמאות לכך כוללות את PRIMA‑1/APR‑246, תכשיר תלת־ארסניק ועצמים המותאמים למוטנטים חמים ספציפיים כגון Y220C או R175H. גישה נוספת היא להעלות את רמות ה‑p53 התקין בגידולים שעדיין מחזיקים בגן TP53 שלם על‑ידי חסימת הרגולטורים השליליים שלו MDM2 ו‑MDM4; כמה מעכבים אורליים של חלבונים אלה נמצאים בניסויים קליניים. טקטיקה שלישית מנסה לשלול מתאי הגידול את התלות ב‑p53 המוטנטי על‑ידי עידוד פירקו באמצעות מעכבי חום‑הלם ומעכבי דה‑אצטילציה של היסטונים או תרופות סטטינים נפוצות. במקביל, מפותחים חיסונים, תאי דנדריט מהונדסים ונוגדנים ספציפיים מאוד כדי לעזור למערכת החיסון לזהות תאים המצטברים ב‑p53 חריג.
מבט קדימה: ממפות לתרופות
המאמר מסכם כי p53 עבר מעניין ביולוגי טהור למטרה טיפולית ריאליסטית, אך כזו שדורשת דיוק. המגוון של מוטציות TP53 והטבע הדו‑חרב של תפקודי p53 ברקמות תקינות הופכים פתרונות אחידים לסבירים פחות. במקום זאת, המחברים מדמיינים שילובים של מולקולות קטנות, אימונו‑תרפיות וכלי עריכת גנים שמונחים על‑ידי ביולוגיה מערכות ולמידת מכונה כדי להתאים את האסטרטגיה הממוקדת p53 לחיווט הספציפי של כל גידול. אם מאמצים אלה יצליחו, תרופות המשקמות או מפצות על תפקוד p53 עשויות לשנות את הטיפול לא רק עבור סוגים רבים של סרטן, אלא אף עבור חלק מהמחלות הלא‑סרטניות המקושרות לחלבון השומר המרכזי הזה.
ציטוט: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
מילות מפתח: p53, מוטציות TP53, תרופות נגד סרטן, מסלולי מדכאי גידולים, תרופות ממוקדות p53