Clear Sky Science · fr
p53 : de la compréhension de sa structure aux avancées du ciblage thérapeutique
Pourquoi cette protéine gardienne est importante
La protéine p53 est souvent qualifiée de « gardienne du génome » car elle aide les cellules saines à réparer les dommages et empêche les cellules endommagées de devenir cancéreuses. Cet article de synthèse explique le fonctionnement de p53, pourquoi elle fait si souvent défaut dans le cancer et comment les scientifiques apprennent aujourd’hui à cibler pharmacologiquement ce qui était longtemps considéré comme « inatteignable ». Il explore aussi des liens surprenants entre p53 et des affections telles que la maladie d’Alzheimer, le diabète et les maladies cardiaques, et passe en revue de nouveaux traitements qui tentent de réparer ou de contourner les défaillances de p53.
L’inspecteur de sécurité interne de la cellule
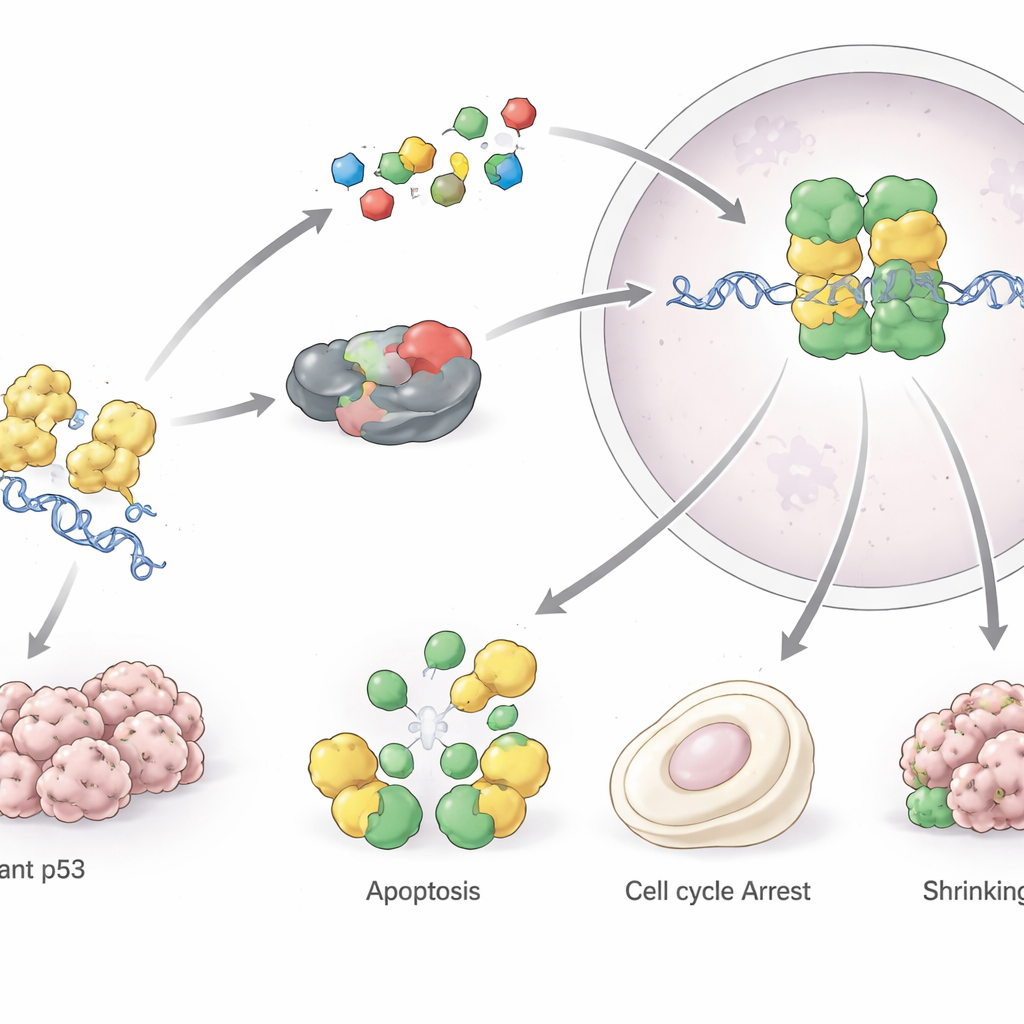
Dans des conditions normales, les cellules maintiennent de faibles niveaux de p53 grâce à un système d’élimination intégré. Lorsqu’un stress survient — comme une lésion de l’ADN, un faible apport en oxygène ou des signaux favorisant le cancer — p53 s’accumule rapidement et active de nombreux gènes. Ces gènes arrêtent la division cellulaire, déclenchent la réparation de l’ADN, ajustent le métabolisme ou, si les dommages sont trop importants, conduisent la cellule à une retraite permanente (sénescence) ou à une mort contrôlée (apoptose). De cette façon, p53 préserve la stabilité du code génétique et empêche la prolifération de cellules endommagées. Elle influence également des formes plus récentes de mort cellulaire, comme la ferroptose, et module l’environnement immunitaire des tumeurs, aidant les cellules immunitaires à reconnaître et attaquer les cellules cancéreuses.
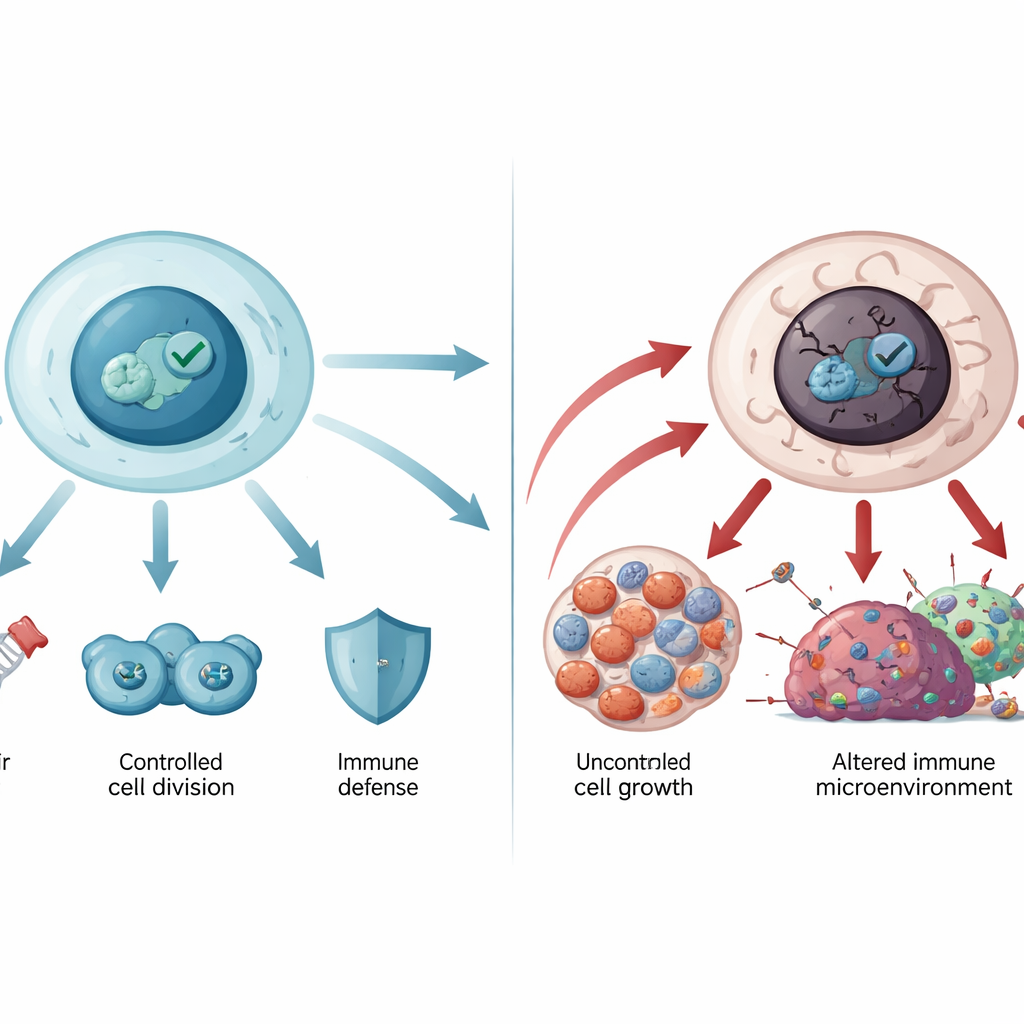
Quand la gardienne déraille
Le gène codant pour p53, TP53, est le gène le plus fréquemment muté dans les cancers humains. La plupart de ces mutations sont des substitutions d’acides aminés dans la région centrale de liaison à l’ADN de la protéine. Certaines mutations affaiblissent l’attachement de p53 à l’ADN, tandis que d’autres déstabilisent sa structure de sorte qu’elle se déroule et s’agrège en amas semblables à des amyloïdes, comme observé dans des maladies neurodégénératives. La p53 mutante ne se contente pas de perdre son rôle protecteur : elle peut aussi acquérir de nouvelles activités favorisant le cancer : elle peut encourager une croissance incontrôlée, aider les cellules tumorales à résister à la mort cellulaire et à la chimiothérapie, remodeler le métabolisme pour nourrir les tumeurs et affaiblir l’immunité anti‑tumorale. Les mutations germinales de TP53 sont à l’origine du syndrome de Li‑Fraumeni et d’autres troubles héréditaires rares à haut risque cancéreux, montrant combien cette voie est cruciale pour la protection tout au long de la vie.
Au‑delà du cancer : liens avec le cerveau, le métabolisme et le cœur
Parce que p53 contrôle la mort cellulaire, les réponses au stress et l’utilisation d’énergie, son influence dépasse le cadre du cancer. Dans le cerveau, une activité anormale de p53 a été associée à la maladie d’Alzheimer, à la maladie de Parkinson, à la maladie de Huntington, à la SLA et à la sclérose en plaques, souvent via des interactions avec des protéines liées à ces maladies et en favorisant la perte excessive de neurones vulnérables. En matière de métabolisme, p53 contribue à réguler le stockage des graisses, la glycémie et la stéatose hépatique ; selon le contexte, elle peut protéger contre l’obésité et le diabète ou, au contraire, contribuer à la résistance à l’insuline et à la maladie du foie gras. Dans le cœur et les vaisseaux, p53 influence la survie cellulaire, la cicatrisation et la formation de plaque, jouant des rôles complexes dans l’insuffisance cardiaque, les lésions cardiaques liées au diabète et l’athérosclérose. Ces effets étendus signifient que toute tentative d’augmenter ou de bloquer p53 doit équilibrer les bénéfices anticancéreux avec les risques potentiels pour les tissus normaux.
Nouvelles façons de cibler « l’intraitable »
Pendant des décennies, p53 a été considérée comme trop complexe et trop centrale pour être ciblée en toute sécurité par des médicaments. Cette vision évolue. Une stratégie majeure vise à « sauver » la p53 mutante en stabilisant sa conformation pour qu’elle se comporte davantage comme la protéine normale ; des exemples incluent PRIMA‑1/APR‑246, le trioxyde d’arsenic et des molécules adaptées à des mutants points chauds spécifiques tels que Y220C ou R175H. Une autre approche consiste à augmenter les niveaux de p53 normale dans les tumeurs qui conservent un gène TP53 intact en bloquant ses régulateurs négatifs MDM2 et MDM4 ; plusieurs inhibiteurs oraux de ces protéines sont en essais cliniques. Une troisième tactique cherche à priver les cellules tumorales de leur dépendance à la p53 mutante en favorisant sa dégradation à l’aide d’inhibiteurs de la réponse au choc thermique et des histone‑désacétylases ou d’agents couramment utilisés comme les statines. Parallèlement, des vaccins, des cellules dendritiques ingénierées et des anticorps très spécifiques sont développés pour aider le système immunitaire à reconnaître les cellules surchargées de p53 anormale.
Perspectives : des cartes aux médicaments
L’article conclut que p53 est passée d’une curiosité purement biologique à une cible thérapeutique réaliste, mais qui exige de la précision. La diversité des mutations TP53 et le double tranchant des rôles de p53 dans les tissus normaux rendent peu probables des traitements universels. Au contraire, les auteurs envisagent des combinaisons de petites molécules, d’immunothérapies et d’outils d’édition génétique guidées par la biologie des systèmes et l’apprentissage automatique pour adapter la bonne stratégie ciblant p53 au câblage propre à chaque tumeur. Si ces efforts réussissent, des médicaments qui restaurent ou compensent la fonction de p53 pourraient transformer la prise en charge non seulement de nombreux cancers, mais potentiellement aussi de certaines maladies non cancéreuses liées à cette protéine gardienne centrale.
Citation: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Mots-clés: p53, mutations TP53, thérapeutiques contre le cancer, voies suppresseurs de tumeurs, médicaments ciblant p53