Clear Sky Science · de
p53: vom Verständnis seiner Struktur bis zu Fortschritten bei therapeutischen Zielsetzungen
Warum dieses Wächterprotein wichtig ist
Das Protein p53 wird oft als „Wächter des Genoms“ bezeichnet, weil es gesunden Zellen hilft, Schäden zu reparieren, und verhindert, dass geschädigte Zellen krebsartig werden. Dieser Übersichtsartikel erklärt, wie p53 funktioniert, warum es bei Krebs so häufig versagt und wie Forscher zunehmend lernen, das lange als „nicht ansprechbar“ geltende Protein pharmakologisch anzugehen. Er beleuchtet außerdem überraschende Verbindungen zwischen p53 und Erkrankungen wie Alzheimer, Diabetes und Herzkrankheiten und sichtet neue Therapien, die versuchen, p53‑Fehler zu beheben oder zu umgehen.
Der interne Sicherheitsinspektor der Zelle
Unter normalen Bedingungen halten Zellen den p53‑Spiegel durch ein eingebautes Recycling‑System niedrig. Wenn Stress auftritt – etwa DNA‑Schäden, Sauerstoffmangel oder krebsfördernde Signale – sammelt sich p53 rasch an und schaltet zahlreiche Gene an. Diese Gene bremsen die Zellteilung, lösen DNA‑Reparatur aus, passen den Stoffwechsel an oder treiben die Zelle bei zu großer Schädigung in dauerhaften Ruhestand (Seneszenz) oder kontrollierten Zelltod (Apoptose). Auf diese Weise erhält p53 den genetischen Code stabil und verhindert die Vermehrung beschädigter Zellen. Es beeinflusst auch neuere Formen des Zelltods wie Ferroptose und prägt das Immunumfeld um Tumoren, sodass Immunzellen Krebszellen erkennen und angreifen können.
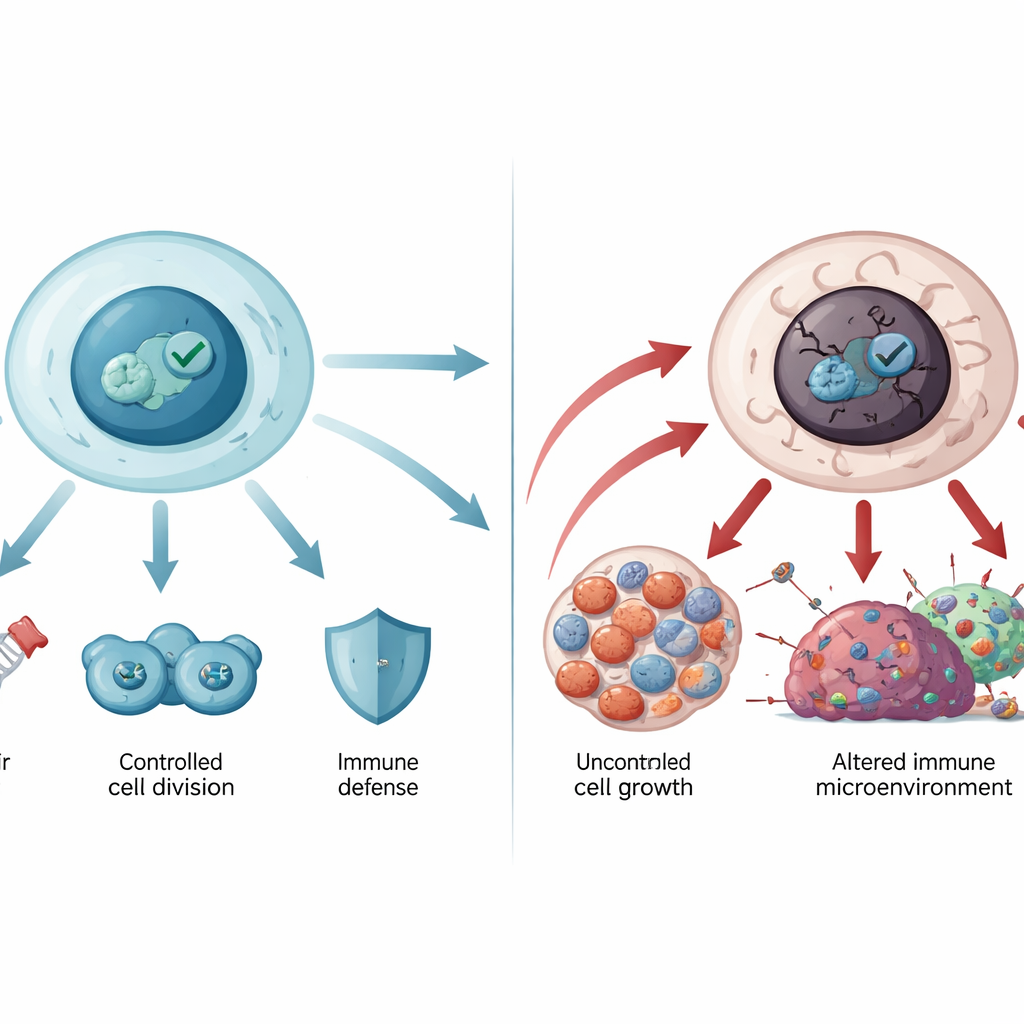
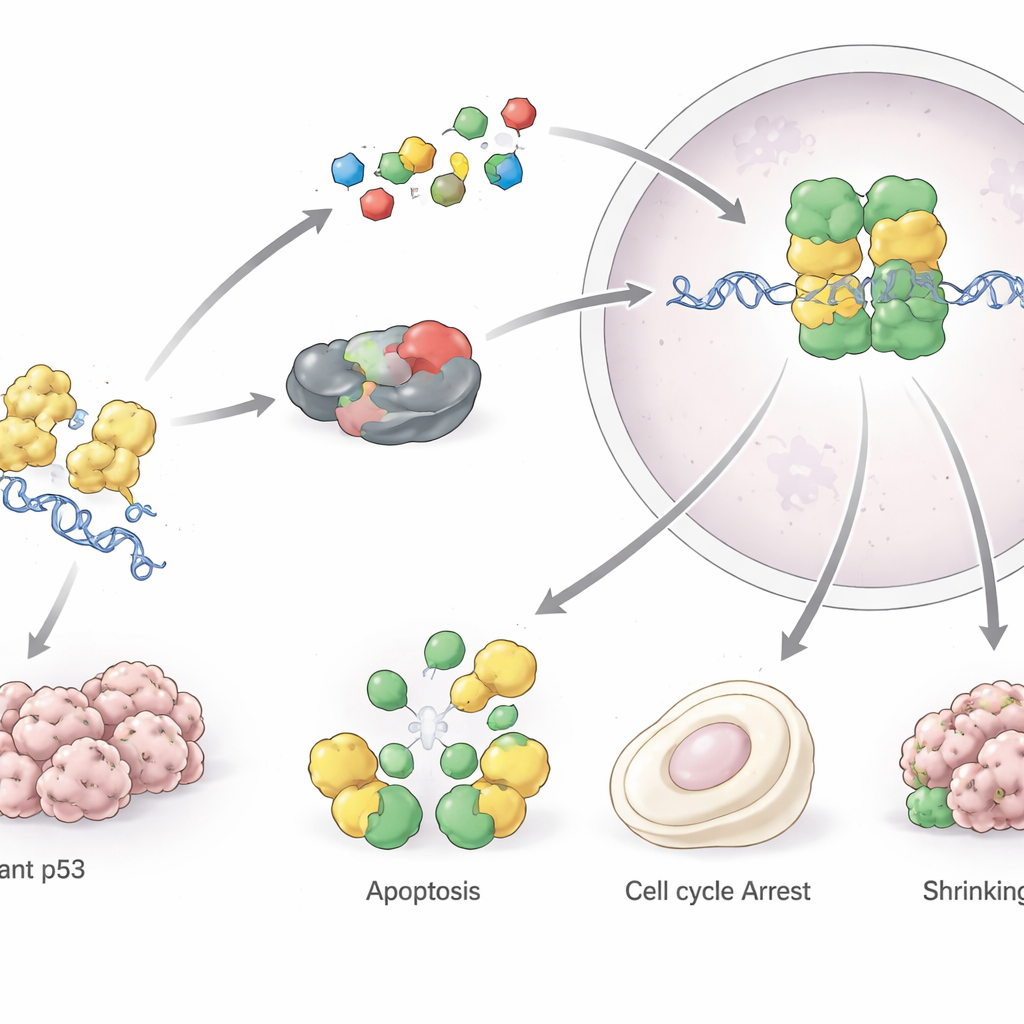
Wenn der Wächter entgleist
Das Gen, das p53 kodiert, TP53, ist das am häufigsten mutierte Gen bei menschlichen Krebserkrankungen. Die meisten dieser Mutationen sind Einzelaminosäure‑Auswechslungen im zentralen DNA‑Bindungsbereich des Proteins. Einige Mutationen schwächen p53s Bindung an DNA, andere destabilisieren seine Struktur, sodass es sich entfaltet und zu Aggregaten verklumpt, die Amyloid ähneln, wie man sie bei neurodegenerativen Erkrankungen sieht. Mutiertes p53 verliert nicht nur seine Schutzfunktion, sondern kann auch neue krebsfördernde Aktivitäten gewinnen: Es kann ungehemmtes Wachstum fördern, Tumorzellen gegen Zelltod und Chemotherapie resistenter machen, den Stoffwechsel so umbauen, dass Tumoren besser versorgt werden, und die antitumorale Immunantwort schwächen. Keimbahnmutationen in TP53 liegen dem Li‑Fraumeni‑Syndrom und anderen seltenen vererbten Erkrankungen mit hohem Krebsrisiko zugrunde und zeigen, wie entscheidend dieser Weg für den lebenslangen Schutz ist.
Jenseits von Krebs: Verbindungen zu Gehirn, Stoffwechsel und Herz
Da p53 Zelltod, Stressantworten und Energiehaushalt steuert, reicht sein Einfluss über den Krebs hinaus. Im Gehirn wurde abweichende p53‑Aktivität mit Alzheimer, Parkinson, Huntington, ALS und Multipler Sklerose in Verbindung gebracht, oft durch Wechselwirkungen mit krankheitsassoziierten Proteinen und durch Förderung übermäßigen Verlusts empfindlicher Neurone. Im Stoffwechsel reguliert p53 Fettablagerung, Blutzucker und Leberfett; je nach Kontext kann es vor Adipositas und Diabetes schützen oder zu Insulinresistenz und Fettleber beitragen. Im Herzen und in den Blutgefäßen beeinflusst p53 Überleben von Zellen, Narbenbildung und Plaquebildung und spielt komplexe Rollen bei Herzinsuffizienz, diabetischer Herzerkrankung und Atherosklerose. Diese weitreichenden Effekte bedeuten, dass jeder Versuch, p53 zu stärken oder zu blockieren, Antikrebs‑Vorteile gegen potenzielle Schäden in normalen Geweben abwägen muss.
Neue Wege, das „Unansprechbare“ zu bearbeiten
Jahrzehntelang galt p53 als zu komplex und zentral, um sicher mit Medikamenten angegangen zu werden. Diese Sicht ändert sich. Eine wichtige Strategie zielt darauf ab, mutiertes p53 zu „retten“, indem seine Faltung stabilisiert wird, sodass es sich mehr wie das normale Protein verhält; Beispiele sind PRIMA‑1/APR‑246, Arsentrioxid und Moleküle, die auf spezifische Hotspot‑Mutanten wie Y220C oder R175H zugeschnitten sind. Ein anderer Ansatz versucht, die Menge des normalen p53 in Tumoren mit intaktem TP53‑Gen zu erhöhen, indem seine negativen Regulatoren MDM2 und MDM4 blockiert werden; mehrere orale Inhibitoren dieser Proteine befinden sich in klinischen Studien. Eine dritte Taktik will Tumorzellen ihrer Abhängigkeit von mutiertem p53 berauben, indem dessen Abbau gefördert wird – etwa durch Hitzeschock‑ und Histon‑Deacetylase‑Inhibitoren oder gebräuchliche Statine. Parallel dazu werden Impfstoffe, gentechnisch veränderte dendritische Zellen und hochspezifische Antikörper entwickelt, um das Immunsystem dabei zu unterstützen, Zellen mit pathologisch erhöhtem p53‑Gehalt zu erkennen.
Blick nach vorn: von Karten zu Medikamenten
Der Artikel schließt mit der Feststellung, dass p53 sich von einer rein biologischen Kuriosität zu einem realistischen therapeutischen Ziel entwickelt hat, das jedoch Präzision verlangt. Die Vielfalt der TP53‑Mutationen und die zweischneidige Natur von p53‑Funktionen in normalen Geweben machen Einheitslösungen unwahrscheinlich. Stattdessen sehen die Autoren Kombinationen aus kleinen Molekülen, Immuntherapien und Gen‑Editierwerkzeugen vor, geleitet von Systembiologie und maschinellem Lernen, um die richtige p53‑gerichtete Strategie an die jeweilige Tumor‑Verdrahtung anzupassen. Gelingt dies, könnten Medikamente, die p53‑Funktion wiederherstellen oder kompensieren, die Behandlung nicht nur vieler Krebserkrankungen, sondern möglicherweise auch einiger nicht‑onkologischer Erkrankungen, die mit diesem zentralen Wächterprotein verknüpft sind, grundlegend verändern.
Zitation: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Schlüsselwörter: p53, TP53-Mutationen, Krebstherapeutika, tumorsuppressorische Signalwege, p53‑gerichtete Arzneimittel