Clear Sky Science · ru
p53: от понимания его структуры до прогресса в терапевтическом целеполагании
Почему этот белок‑страж важен
Белок p53 часто называют «стражем генома», потому что он помогает здоровым клеткам ремонтировать повреждения и препятствует превращению повреждённых клеток в раковые. В этом обзорном обзоре объясняется, как действует p53, почему он так часто выходит из строя при раке и как учёные теперь учатся разрабатывать препараты против того, что долгое время считалось «недрогируемым». Также рассматриваются неожиданные связи между p53 и такими состояниями, как болезнь Альцгеймера, диабет и болезни сердца, и обобщаются новые подходы к лечению, которые пытаются исправить или обойти сбои p53.
Внутренний инспектор безопасности клетки
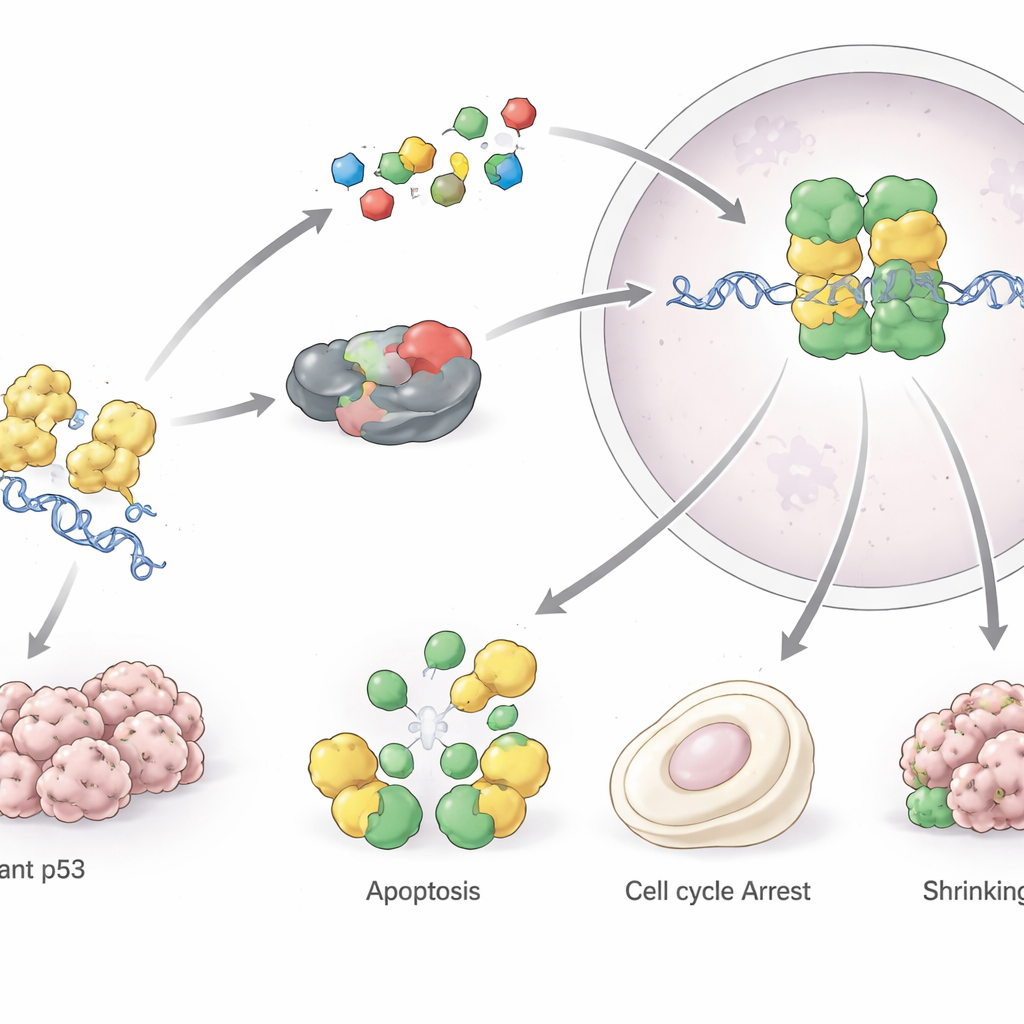
При нормальных условиях клетки держат уровни p53 низкими с помощью встроенной системы утилизации. Когда возникает стресс — например повреждение ДНК, низкий уровень кислорода или сигналы, способствующие канцерогенезу — p53 быстро накапливается и включает множества генов. Эти гены останавливают деление клетки, запускают репарацию ДНК, корректируют метаболизм или, если повреждение слишком велико, переводят клетку в состояние постоянного выхода из цикла (сенесценция) или в контролируемую гибель (апоптоз). Таким образом p53 поддерживает стабильность генетического кода и предотвращает размножение повреждённых клеток. Он также влияет на новые формы смерти клеток, такие как ферроптоз, и формирует иммунную среду вокруг опухолей, помогая иммунным клеткам распознавать и атаковать раковые клетки.
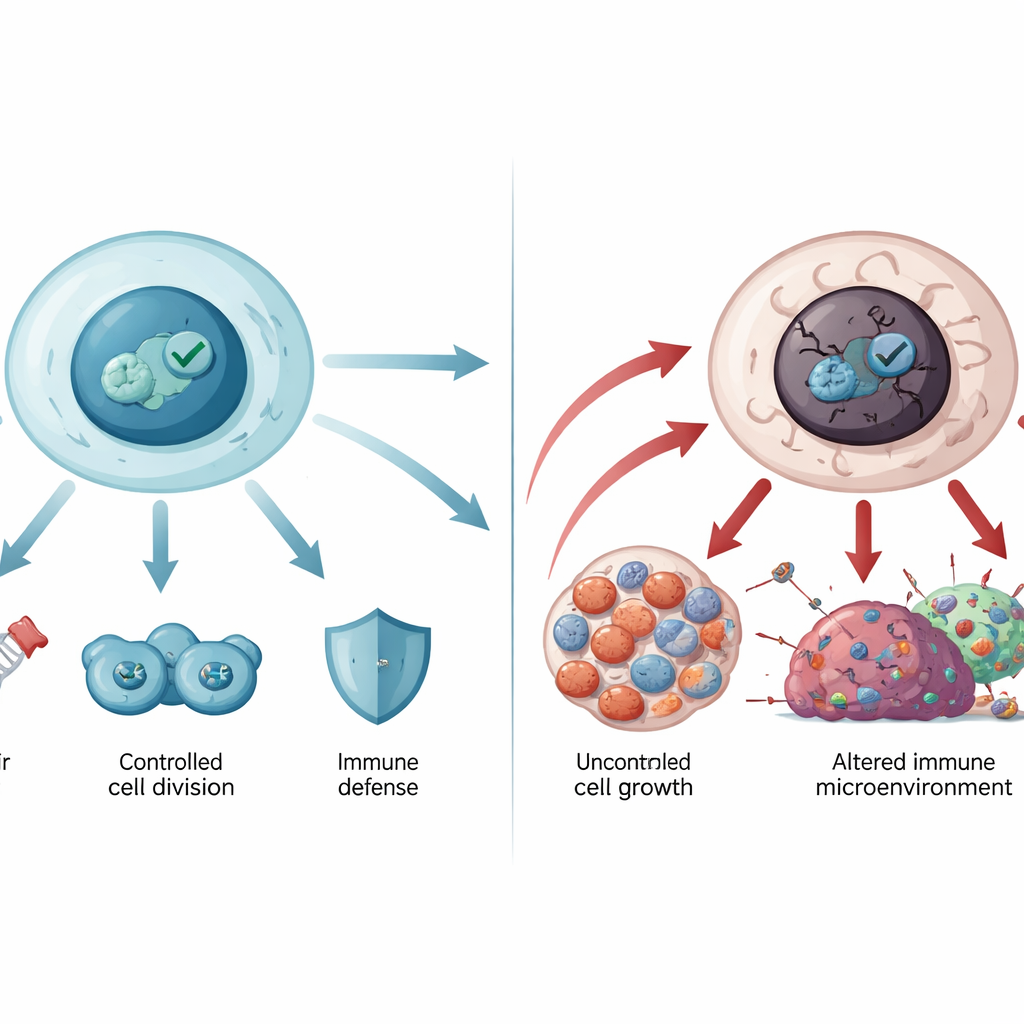
Когда страж сбивается с пути
Ген, кодирующий p53 — TP53 — является самым часто мутирующим геном в человеческих раках. Большинство этих мутаций представляют собой замены одного аминокислотного остатка в центральной ДНК‑связывающей области белка. Некоторые мутации ослабляют способность p53 связываться с ДНК, другие дестабилизируют его структуру, вызывая разворачивание и агрегацию, сходную с амилоидной, как при нейродегенеративных болезнях. Мутантный p53 не только теряет защитную функцию, но может приобретать новые протуморогенные свойства: стимулировать неконтролируемый рост, помогать опухолевым клеткам противостоять гибели и химиотерапии, перестраивать метаболизм в пользу питания опухоли и ослаблять антиопухолевый иммунитет. Герминативные мутации TP53 лежат в основе синдрома Ли‑Фраумени и других редких наследственных состояний с высоким риском рака, что подчёркивает критическую роль этого пути в пожизненной защите.
Вне рака: связи с мозгом, метаболизмом и сердцем
Поскольку p53 контролирует гибель клеток, стрессовые ответы и использование энергии, его влияние выходит за рамки рака. В мозге аномальная активность p53 связывают с болезнью Альцгеймера, болезнью Паркинсона, болезнью Хантингтона, БАС и рассеянным склерозом, часто через взаимодействие с белками, связанными с этими заболеваниями, и через продвижение избыточной потери уязвимых нейронов. В сфере метаболизма p53 участвует в регуляции накопления жира, уровня сахара в крови и жирового перерождения печени; в зависимости от контекста он может защищать от ожирения и диабета или, наоборот, способствовать инсулинорезистентности и жировому гепатозу. В сердце и сосудах p53 влияет на выживание клеток, образование рубцовой ткани и формирование атеросклеротических бляшек, играя сложные роли в сердечной недостаточности, диабетическом повреждении сердца и атеросклерозе. Эти широкие эффекты означают, что любые попытки усилить или блокировать p53 должны уравновешивать противораковые выгоды с потенциальным вредом для нормальных тканей.
Новые способы «лекарствовать» «нелекаруемое»
Долгие годы p53 считали слишком сложным и центральным, чтобы безопасно нацеливать его препаратами. Это представление меняется. Одна из основных стратегий стремится «спасти» мутантный p53, стабилизируя его конформацию, чтобы он вел себя как нормальный белок; примеры включают PRIMA‑1/APR‑246, трёхокись мышьяка и молекулы, специфичные для определённых «горячих» мутантов, таких как Y220C или R175H. Другой подход повышает уровни нормального p53 в опухолях с интактным геномом TP53, блокируя его негативные регуляторы MDM2 и MDM4; несколько пероральных ингибиторов этих белков находятся в клинических испытаниях. Третья тактика пытается лишить опухолевые клетки зависимости от мутантного p53, стимулируя его деградацию с помощью ингибиторoв шоковых белков и гистондеацетилаз или широко применяемых статинов. Параллельно разрабатываются вакцины, генетически модифицированные дендритные клетки и высокоспецифичные антитела, которые помогают иммунной системе распознавать клетки с избытком аномального p53.
Взгляд вперёд: от карт к лекарствам
В статье делается вывод, что p53 перестал быть лишь биологической диковинкой и стал реалистичной терапевтической мишенью, но требующей точного подхода. Разнообразие мутаций TP53 и двусторонняя роль p53 в нормальных тканях делают маловероятными универсальные решения. Авторы ожидают комбинаций малых молекул, иммунотерапий и инструментов редактирования генов, подкреплённых системной биологией и машинным обучением, чтобы сопоставлять правильную стратегию, нацеленную на p53, с молекулярной схемой каждой опухоли. Если эти усилия увенчаются успехом, препараты, восстанавливающие или компенсирующие функцию p53, могут преобразить лечение не только многих видов рака, но и некоторых неонкологических заболеваний, связанных с этим ключевым белком‑стражем.
Цитирование: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
Ключевые слова: p53, мутации TP53, противораковая терапия, пути супрессии опухолей, препараты, нацеленные на p53