Clear Sky Science · zh
缺氧诱导的 XBP1s–MYDGF 轴通过 UBQLN1 介导的 LCN2 稳定抑制胃癌中的铁死亡
为什么切断肿瘤的铁源很重要
胃癌是全球最致命的癌症之一,部分原因在于肿瘤细胞能在胃壁深处的低氧(缺氧)环境中出色地生存。许多新药试图通过触发一种由铁驱动的细胞死亡形式——铁死亡——来杀死癌细胞。本研究提出了对未来患者至关重要的问题:缺氧的胃肿瘤如何躲过这种依赖铁的死亡,能否阻断其逃避途径?
氧气不足肿瘤中的隐藏救援线路
研究人员利用人类胃组织的大型单细胞 RNA 测序数据,对从正常上皮到进展为胃癌的细胞逐个绘制基因活动图谱。他们发现,恶性上皮细胞显著上调一种名为髓源性生长因子(MYDGF)的分泌蛋白,远高于邻近的健康细胞。MYDGF 高表达的癌细胞还显示出内质网内蛋白处理与降解系统的显著特征,提示 MYDGF 可能与肿瘤细胞如何调控关键蛋白的生死有关。
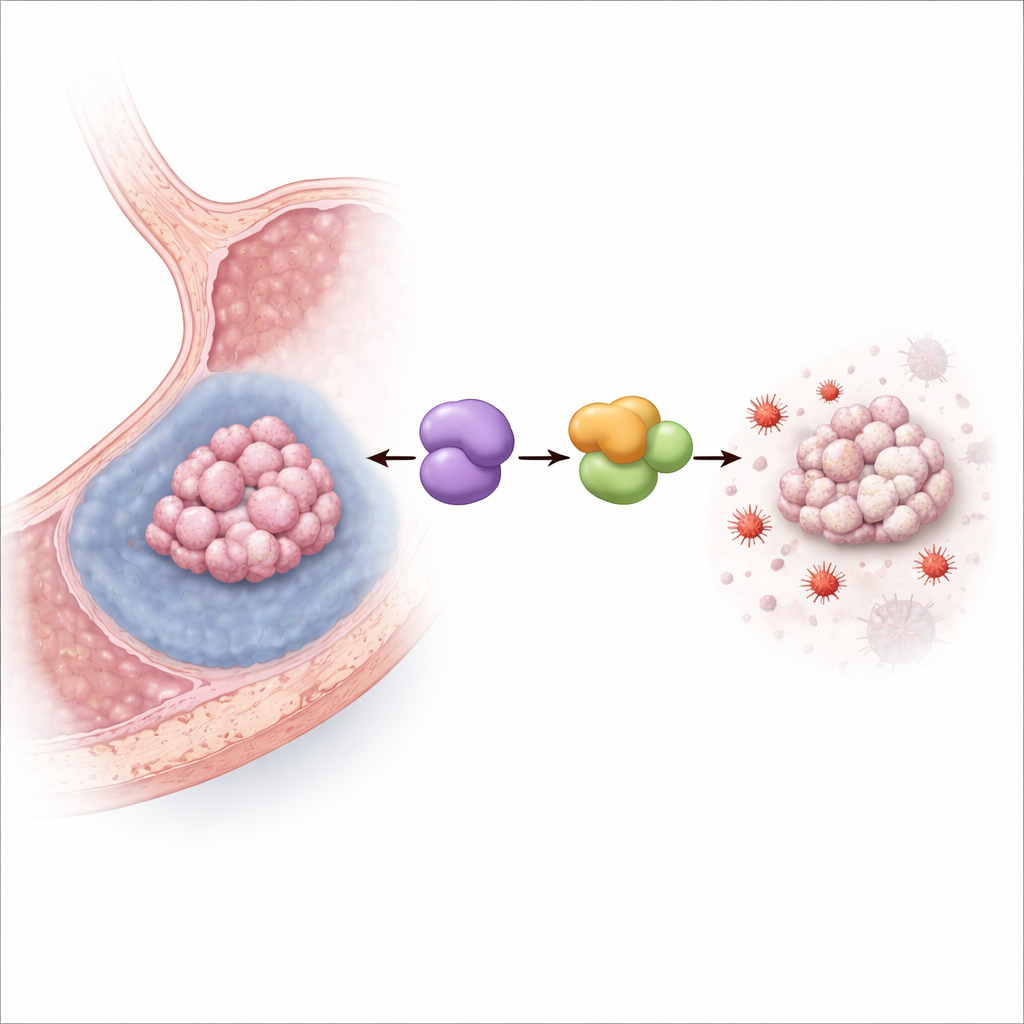
关闭铁驱动的细胞死亡
团队随后在模拟实体肿瘤饥饿性低氧环境的条件下培养人胃癌细胞。低氧使 MYDGF 水平上升,并如预期地降低了细胞存活率。实验性降低 MYDGF 后,缺氧对细胞的致死性大幅增强,尤其通过铁死亡途径:脂质损伤和铁驱动氧化应激的标志物激增,线粒体出现损伤性缩小形态,而一种强效的铁死亡抑制剂在很大程度上拯救了细胞。在带有胃癌移植瘤的小鼠中,增强 MYDGF 减弱了促铁死亡药物的肿瘤缩小效果,而阻断一个名为 LCN2 的伴侣蛋白则产生相反效果,证实该通路在体内肿瘤中也起作用。
癌细胞如何保护其结合铁的守护者
进一步研究表明,结合铁的蛋白 LCN2 是关键下游执行者。在缺氧下,LCN2 的蛋白水平下降,而其基因表达并未相应减少,表明是通过活跃的蛋白降解而非生成减少造成的。研究显示,LCN2 通常被泛素标记并通过一种称为内质网相关降解(ER‑associated degradation, ERAD)的质量控制途径送入细胞的蛋白“碎纸机”——蛋白酶体。转运适配子 UBQLN1 将泛素化的 LCN2 递送到降解装置。MYDGF 则充当保镖:它在 UBQLN1 的特定对接区与之结合,排挤 LCN2,阻止其被交给蛋白酶体。因此,LCN2 蛋白被稳定下来,持续结合反应性铁,抑制驱动铁死亡的脂质过氧化反应。
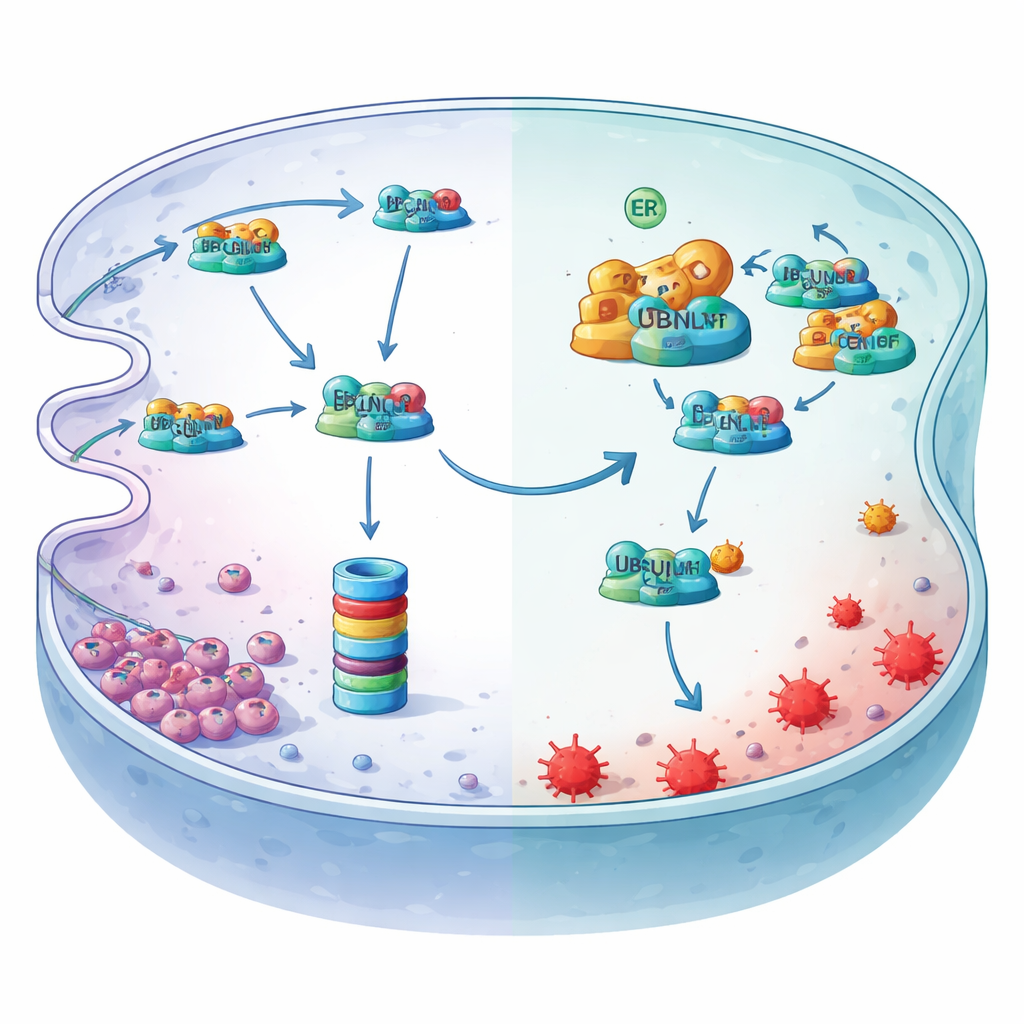
缺氧在上游翻转主开关
研究还揭示了缺氧如何开启这条保护轴。低氧使内质网承受应激并激活转录因子的剪接异构体 XBP1s。通过扫描 MYDGF 基因的调控区并结合染色质结合与报告基因实验,研究人员证明 XBP1s 在特定位点结合并直接上调 MYDGF 的产生。当降低 XBP1s 时,MYDGF 水平下降,LCN2 水平随之降低,铁死亡相关标志上升——这些效应可被恢复 MYDGF 或 LCN2 所逆转。综合这些实验,勾画出一条线性防护链:缺氧激活 XBP1s,XBP1s 提升 MYDGF,MYDGF 阻断 UBQLN1 介导的 LCN2 降解,从而使 LCN2 吸收铁并保护胃癌细胞免受铁死亡。
围剿顽固胃肿瘤的新思路
对非专业读者来说,结论是:缺氧的胃肿瘤建立了一条内部“应急通道”,使一个结合铁的保护蛋白存活足够长的时间以避免一种很有前景的新型细胞死亡方式。通过详尽描绘 XBP1s–MYDGF–UBQLN1–LCN2 这条链路,研究解释了为什么某些肿瘤区域可能对基于铁死亡的治疗产生抵抗,并指出了可以解除该防御的具体策略——例如阻断 MYDGF、XBP1s 或 UBQLN1 的相互作用界面。如果这些干预能安全地转化到临床,可能会使未来的促铁死亡药物在最耐药、氧气最匮乏的胃癌区域发挥更好疗效。
引用: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
关键词: 胃癌, 缺氧, 铁死亡, 蛋白降解, 铁代谢