Clear Sky Science · ar
محور XBP1s-MYDGF المحفز بنقص الأكسجة يثبط الفيروبتوسيس عبر استقرار LCN2 بوساطة UBQLN1 في سرطان المعدة
لماذا يهم تجويع الأورام من الحديد
يُعد سرطان المعدة من أخطر أنواع السرطان في العالم، جزئياً لأن خلايا الورم تصبح بارعة في البقاء على قيد الحياة في جيوب منخفضة الأكسجين، أو ناقصة الأكسجة، داخل جدار المعدة. تستهدف العديد من الأدوية الجديدة قتل الخلايا السرطانية عن طريق تحفيز شكل من أشكال الموت الخلوي المدفوع بالحديد يُسمى الفيروبتوسيس. تطرح هذه الدراسة سؤالًا حاسمًا للمرضى في المستقبل: كيف تتجنب أورام المعدة ناقصة الأكسجة هذا النوع المعتمد على الحديد من الموت، وهل يمكن حجب طريق الهروب هذا؟
خط إنقاذ خفي داخل الأورام الفقيرة بالأكسجين
باستخدام مجموعات بيانات واسعة للتسلسل الحلزوني الوحيد للحمض النووي الريبي من نسيج المعدة البشري، رسم الباحثون نشاط الجينات خلية بخلية عبر الانتقال من الطبقة الطبيعية إلى سرطان المعدة المتقدم. وجدوا أن الخلايا الظهارية الخبيثة تُفعّل بروتينًا مُفرَزًا باسم عامل نمو مشتق من النخاع (MYDGF) بقوة أكبر بكثير من الخلايا السليمة المجاورة. كما أظهرت خلايا السرطان ذات التعبير العالي عن MYDGF إشارات قوية لأنظمة التعامل مع البروتين والتخلص منه داخل الشبكة الإندوبلازمية، ما يوحي بأن MYDGF قد يكون مرتبطًا بكيفية إدارة خلايا الورم لبقاء ومصير بروتينات رئيسية.
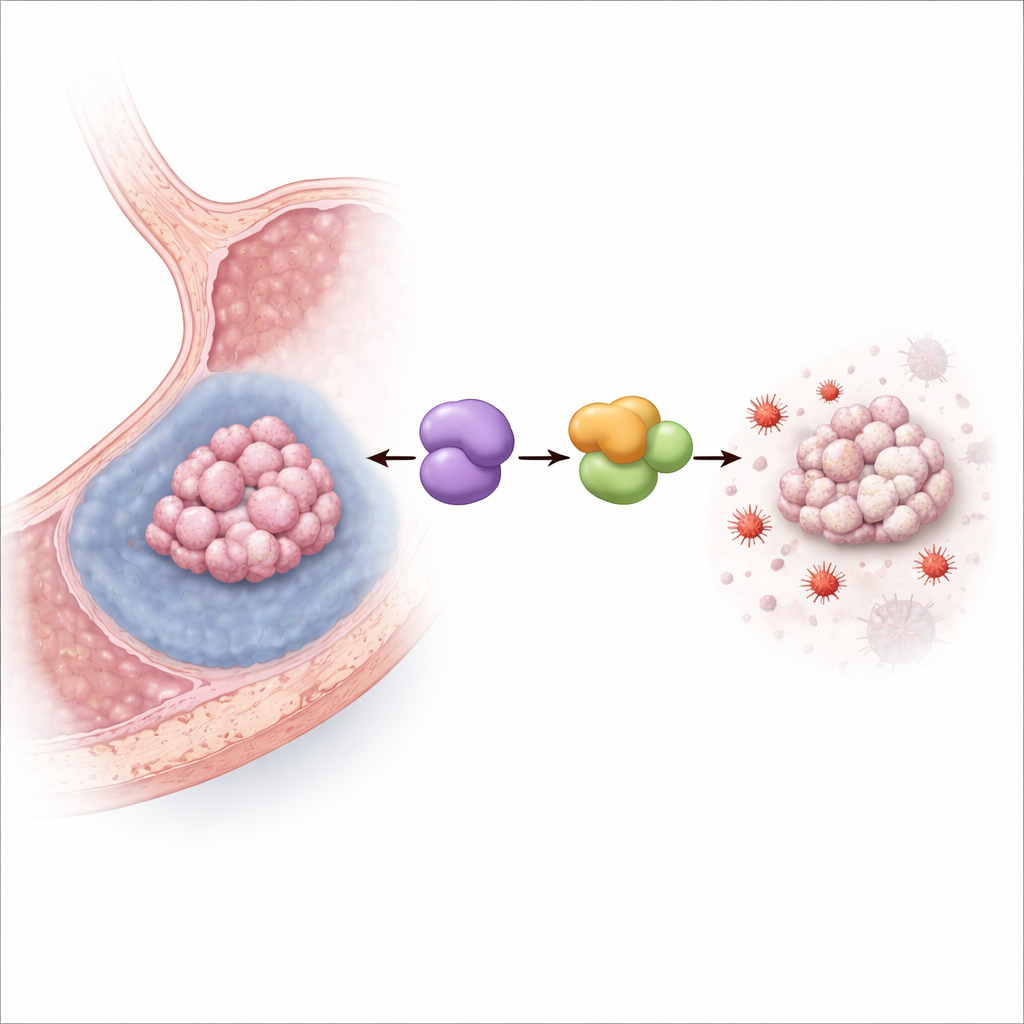
إيقاف الموت الخلوي المدفوع بالحديد
ثم نمَتْ الفريق خلايا سرطان المعدة البشرية تحت ظروف ناقصة الأكسجة التي تحاكي داخل الأورام الصلبة المجوّعة. أدت قلة الأكسجين إلى رفع مستويات MYDGF ومع انخفاض متوقع في بقاء الخلايا. عندما تم تقليل MYDGF تجريبيًا، أصبحت ناقصة الأكسجة أكثر فتكًا بكثير، لا سيما عبر الفيروبتوسيس: ارتفعت علامات تلف الدهون والإجهاد التأكسدي المدفوع بالحديد، واتخذت الميتوكوندريا مظهرًا تالفًا ومقشرًا، وأنقذت مُثبّت قوي للفيروبتوسيس الخلايا إلى حد كبير. في فئران تحمل طعومات لسرطان المعدة، قلل تعزيز MYDGF التأثير المتقلص للورم الناتج عن دواء يحفز الفيروبتوسيس، بينما أدى حجب بروتين شريك يسمى LCN2 إلى العكس، مؤكّدًا أن هذا المسار يعمل في الأورام الحية.
كيف تحمي الخلايا السرطانية حارسها الراصد للحديد
بالغوص أعمق، حدّد المؤلفون LCN2، وهو بروتين مرتبط بالحديد، كلاعب حاسم لاحقًا في المسار. تحت ناقصة الأكسجة، انخفضت مستويات بروتين LCN2 رغم أن نشاط جينّه لم ينخفض، ما يشير إلى تدمير نشط بدلًا من إنتاج أقل. أظهروا أن LCN2 يُعلَّم عادة باليوبيكويتين ويُدخل إلى مخرطة البروتينات الخلوية، البروتيازوم، عبر مسار مراقبة الجودة للشبكة الإندوبلازمية يُعرف باسم التحلل المرتبط بالشبكة الإندوبلازمية (ER‑associated degradation). ناقل يُسمى UBQLN1 يوصل LCN2 الموسوم باليوبيكويتين إلى هذه الآلية التفكيكية. يدخل MYDGF كحارس: يرتبط بـ UBQLN1 عند مجال ربط محدد، فيزاحم LCN2 ويمنع تسليمه إلى البروتيازوم. كنتيجة لذلك، يستقر بروتين LCN2، ويستمر في ربط الحديد التفاعلي، ويقلل من البيروكسدة الدهنية التي تقود الفيروبتوسيس.
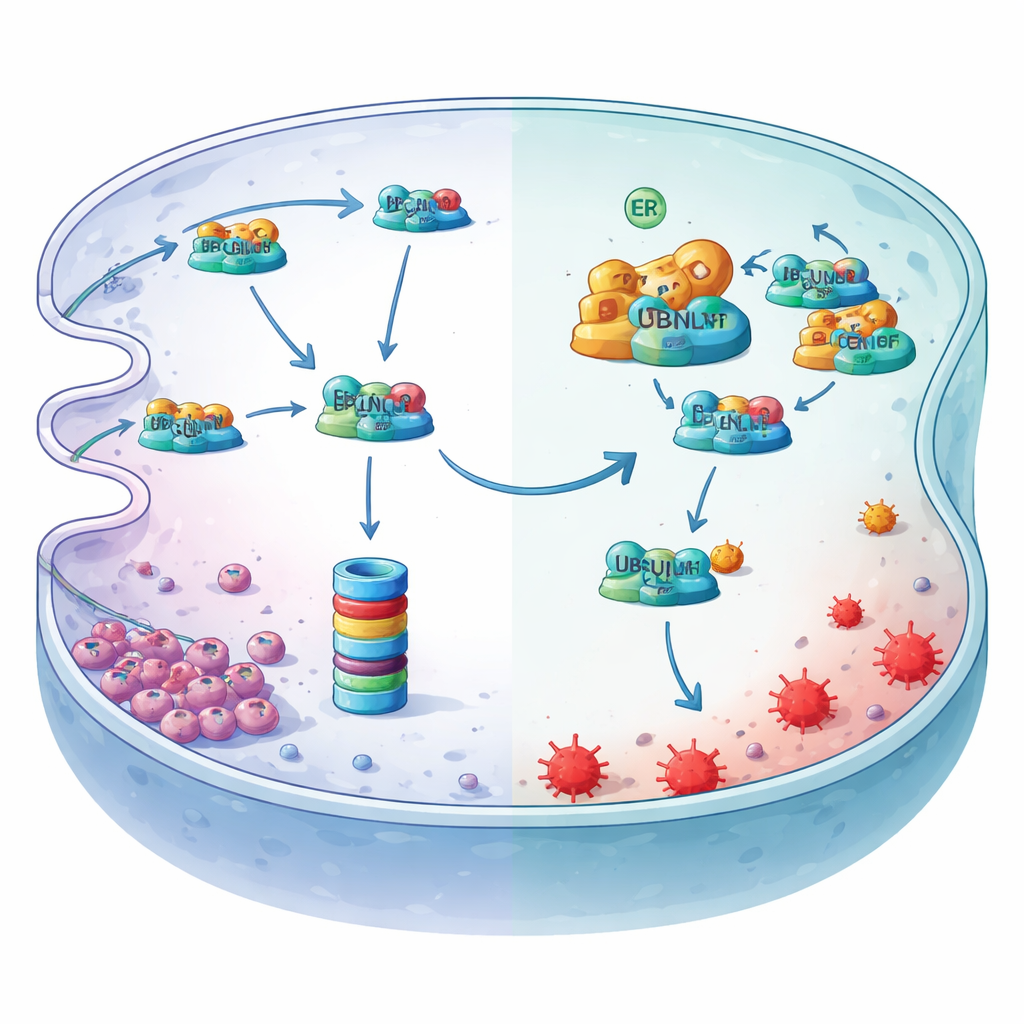
نقص الأكسجة يبدل المفتاح الرئيسي إلى الأعلى
تكشف الدراسة أيضًا كيف تُشغّل ناقصة الأكسجة هذا المحور الوقائي. تُجهد قلة الأكسجين الشبكة الإندوبلازمية وتُفعّل شكلًا مؤشّرًا منقوصًا من عامل النسخ يُدعى XBP1s. من خلال مسح منطقة التحكم في جين MYDGF واستخدام تجارب ربط الكروماتين ومؤشرات المراسل، أظهر الباحثون أن XBP1s يرسو عند موقع محدد ويزيد مباشرة إنتاج MYDGF. عندما قللوا XBP1s، هبطت مستويات MYDGF وانخفضت مستويات LCN2 وارتفعت علامات الفيروبتوسيس—تأثيرات أمكن عكسها باستعادة MYDGF أو LCN2. معًا، ترسم هذه التجارب خط دفاعي متسلسل: تُفعّل ناقصة الأكسجة XBP1s، الذي يعزز MYDGF، الذي يعيق تدمير LCN2 المدفوع بـ UBQLN1، والذي يلتقط الحديد إذًا ويحمي خلايا سرطان المعدة من الفيروبتوسيس.
طرق جديدة لمحاصرة الأورام العنيدة في المعدة
لغير المتخصصين، الخلاصة أن أورام المعدة ناقصة الأكسجة بنت «خط طوارئ» داخليًا يُبقي بروتينًا حاميًا لارتباط الحديد حيًا لفترة كافية لتجنب شكل واعد من الموت الخلوي. عبر رسم سلسلة XBP1s–MYDGF–UBQLN1–LCN2 بتفصيل، يشرح العمل لماذا قد تقاوم بعض مناطق الورم علاجات قائمة على الفيروبتوسيس ويشير إلى استراتيجيات ملموسة لتعطيل هذا الدفاع—مثل حجب MYDGF أو XBP1s أو أسطح التفاعل على UBQLN1. إذا أمكن ترجمة مثل هذه التدخلات بأمان للمرضى، فقد تساعد مستقبلًا الأدوية المحفِّزة للفيروبتوسيس على العمل بشكل أفضل في أجزاء سرطان المعدة الأكثر مقاومة والعطشى للأكسجين.
الاستشهاد: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
الكلمات المفتاحية: سرطان المعدة, نقص الأكسجة, الفيروبتوسيس, تحلل البروتين, استقلاب الحديد