Clear Sky Science · sv
Hypoxi‑inducerad XBP1s–MYDGF‑axel dämpar ferroptos genom UBQLN1‑medierad stabilisering av LCN2 i magcancer
Varför det spelar roll att svälta tumörer på järn
Magcancer är en av världens dödligaste cancerformer, delvis därför att tumörceller blir anmärkningsvärt bra på att överleva i syrefattiga, eller hypoxiska, fickor djupt i magsäcksväggen. Många nya läkemedel försöker döda cancerceller genom att utlösa en form av järnberoende celldöd kallad ferroptos. Denna studie ställer en avgörande fråga för framtida patienter: hur undviker hypoxiska magtumörer denna järnavhängiga död, och kan den flyktvägen blockeras?
En dold räddningslinje inne i syrebristiga tumörer
Genom att använda stora single‑cell RNA‑sekvenseringsdataset från mänsklig magslemhinna kartlade forskarna genaktivitet cell för cell över övergången från normal slemhinna till fullt utvecklad magcancer. De fann att maligna epitelceller slår på ett utsöndrat protein kallat myeloid‑derived growth factor (MYDGF) mycket starkare än närliggande friska celler. Dessa MYDGF‑rika cancerceller visade också tydliga signaturer för hantering och borttagning av proteiner i det endoplasmatiska retiklet, vilket antyder att MYDGF kan vara kopplat till hur tumörceller styr livet och döden för viktiga proteiner.
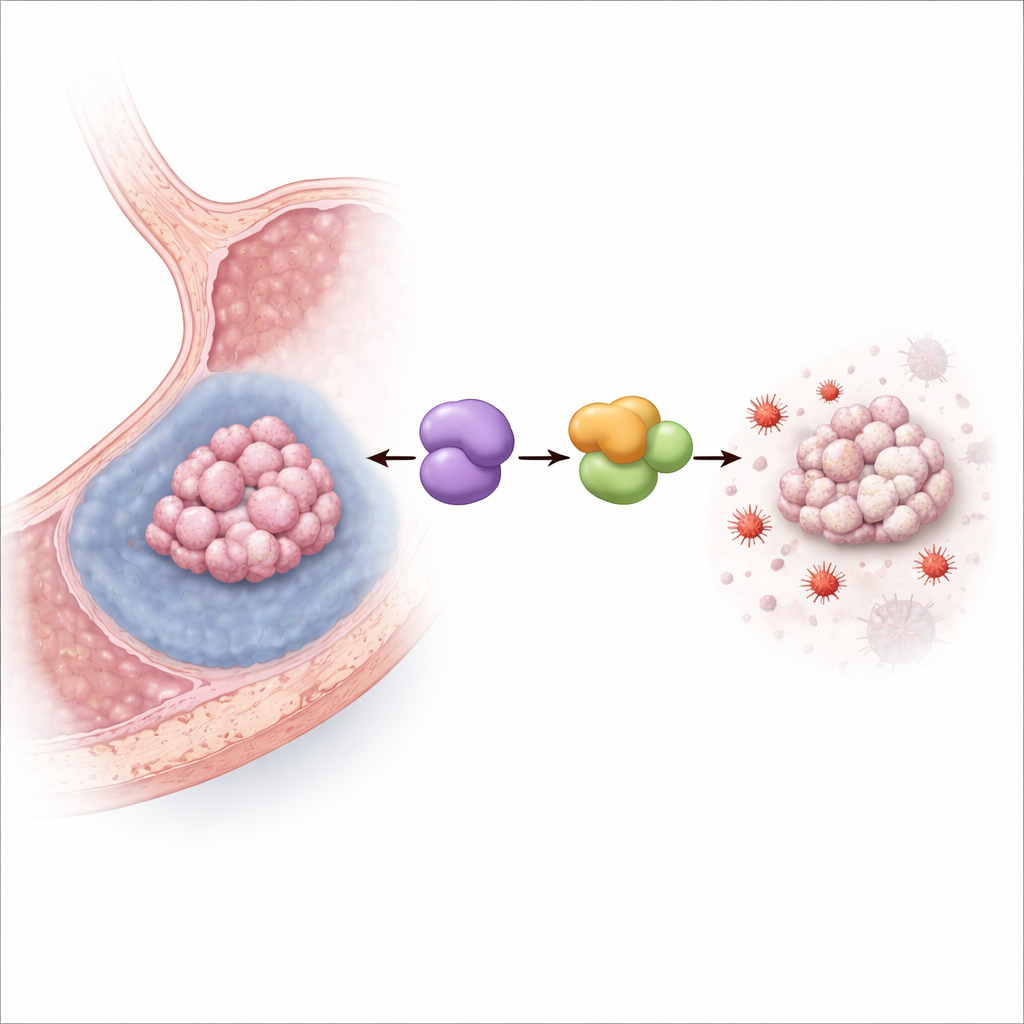
Att stänga av järndriven celldöd
Teamet odlade därefter humana magcancerceller under hypoxiska förhållanden som efterliknar den svältande insidan av solida tumörer. Lågt syre ökade MYDGF‑nivåerna och, som väntat, minskade cellöverlevnaden. När MYDGF experimentellt minskades blev hypoxin mycket mer dödlig, särskilt genom ferroptos: markörer för lipidsskada och järn‑driven oxidativ stress steg, mitokondrierna fick ett skadat, förminskat utseende, och en potent ferroptoshämmare räddade till stor del cellerna. I möss med magcancergraft gav ökat MYDGF minskad tumörminskningseffekt av ett ferroptos‑inducerande läkemedel, medan blockad av en partnerprotein kallad LCN2 gav motsatt effekt, vilket bekräftar att denna bana fungerar i levande tumörer.
Hur cancerceller skyddar sin järnbindande väktare
Genom ytterligare undersökningar identifierade författarna LCN2, ett järnbindande protein, som den kritiska nedströmsaktören. Under hypoxi minskade LCN2:s proteinnivåer trots att genaktiviteten inte gjorde det, vilket pekar på aktiv nedbrytning snarare än minskad produktion. De visade att LCN2 normalt märks med ubiquitin och förs in i cellens proteinmallning, proteasomen, via en kvalitetssäkringsrutt i det endoplasmatiska retiklet känd som ER‑associerad nedbrytning. En transportadapter kallad UBQLN1 levererar ubiquitinerat LCN2 till denna nedbrytningsapparat. MYDGF träder in som livvakt: det binder till UBQLN1 vid en specifik dokningsdomän, tränger undan LCN2 och förhindrar dess överlämning till proteasomen. Som ett resultat stabiliseras LCN2‑proteinet, fortsätter att binda reaktivt järn och dämpar den lipidperoxidation som driver ferroptos.
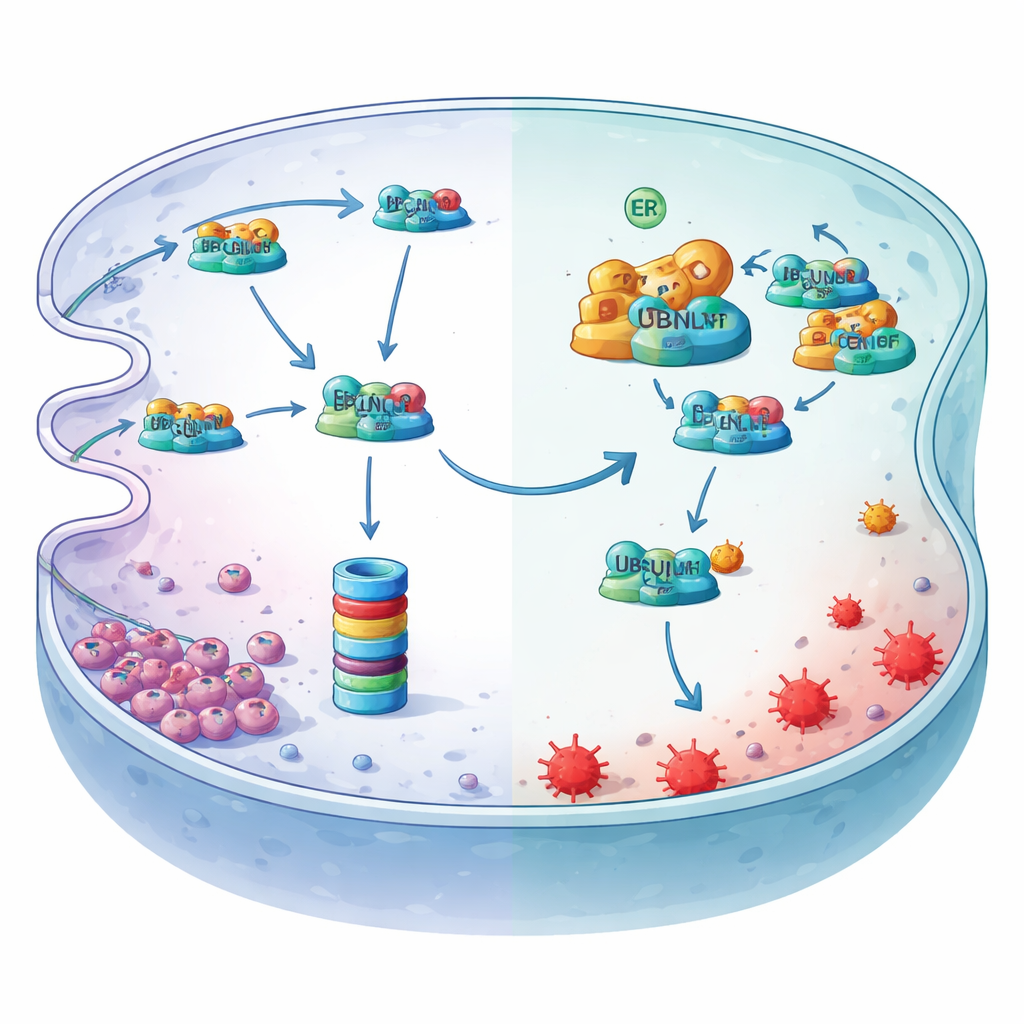
Hypoxi slår på huvudbrytaren uppströms
Studien visar också hur hypoxi slår på denna skyddande axel. Lågt syre stressar det endoplasmatiska retiklet och aktiverar en splitsad form av en transkriptionsfaktor kallad XBP1s. Genom att skanna kontrollregionen för MYDGF‑genen och använda kromatinbindnings‑ och reporterassayer visade forskarna att XBP1s dockar vid en specifik plats och direkt ökar MYDGF‑produktionen. När XBP1s minskades föll MYDGF‑nivåerna, LCN2‑nivåerna sjönk och ferroptosmarkörer steg — effekter som kunde återställas genom att återinföra MYDGF eller LCN2. Tillsammans skisserar dessa experiment en linjär försvarslinje: hypoxi aktiverar XBP1s, vilket ökar MYDGF, vilket blockerar UBQLN1‑driven nedbrytning av LCN2, som i sin tur binder upp järn och skyddar magcancerceller från ferroptos.
Nya sätt att tränga in i envisa magtumörer
För icke‑experter är slutsatsen att hypoxiska magtumörer byggt upp en intern "nödlinje" som håller ett järnbindande skyddsprotein vid liv precis tillräckligt länge för att undvika en lovande ny typ av celldöd. Genom att kartlägga denna XBP1s–MYDGF–UBQLN1–LCN2‑kedja i detalj förklarar arbetet varför vissa tumörområden kan motstå ferroptos‑baserade terapier och pekar på konkreta strategier för att avväpna det försvaret — till exempel genom att blockera MYDGF, XBP1s eller interaktionsytorna på UBQLN1. Om sådana interventioner kan översättas säkert till patienter kan de göra framtida ferroptos‑inducerande läkemedel mer effektiva i de mest behandlingsresistenta, syrefattiga delarna av magcancer.
Citering: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Nyckelord: magcancer, hypoxi, ferroptos, proteinnedbrytning, järnmetabolism