Clear Sky Science · tr
Hipoksi kaynaklı XBP1s-MYDGF ekseni, UBQLN1 aracılı LCN2 stabilizasyonu yoluyla gastrik kanserde ferroptozu baskılar
Tümörleri demirden mahrum bırakmanın önemi
Mide kanseri, kısmen tümör hücrelerinin mide duvarının derinliklerindeki düşük oksijenli (hipoksik) alanlarda hayatta kalma konusunda son derece yetenekli hale gelmesi nedeniyle dünyadaki en ölümcül kanserlerden biridir. Birçok yeni ilaç, ferroptoz adı verilen demir kaynaklı bir hücre ölüm şekli tetikleyerek kanser hücrelerini öldürmeyi amaçlıyor. Bu çalışma gelecekteki hastalar için kritik bir soruyu gündeme getiriyor: Hipoksik mide tümörleri bu demir‑bağımlı ölümden nasıl kaçıyor ve bu kaçış yolu engellenebilir mi?
Oksijen fakiri tümörlerin içinde gizli bir kurtarma hattı
Araştırmacılar, insan mide dokusundan alınan büyük tek hücre RNA dizileme veri setlerini kullanarak normal örtüden tam gelişmiş mide kanserine kadar hücre hücre gen etkinliğini haritaladılar. Kötü huylu epitel hücrelerin, yakınlarındaki sağlıklı hücrelerden çok daha güçlü bir şekilde salgılanan bir protein olan miyeloid kaynaklı büyüme faktörü (MYDGF) açtığını buldular. MYDGF yüksek kanser hücreleri ayrıca endoplazmik retikulum içindeki protein işleme ve yok etme sistemlerine ait güçlü imzalar gösteriyordu; bu da MYDGF’nin tümör hücrelerinin belirli anahtar proteinlerin yaşam ve ölümünü nasıl yönettiğiyle bağlantılı olabileceğini düşündürdü.
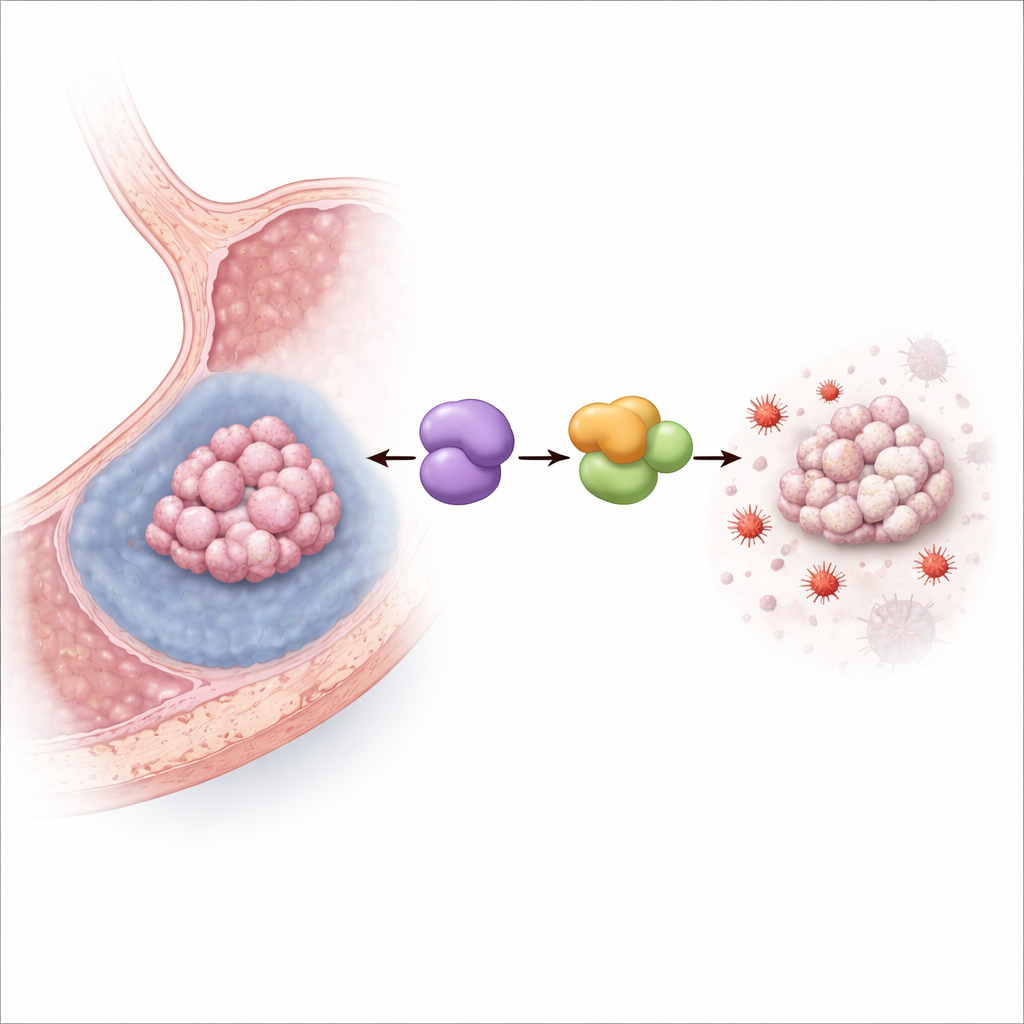
Demir kaynaklı hücre ölümünü kapatmak
Araştırma ekibi daha sonra insan mide kanseri hücrelerini katı tümörlerin yetersiz iç kısımlarını taklit eden hipoksik koşullar altında yetiştirdi. Düşük oksijen MYDGF düzeylerini artırdı ve beklenildiği gibi hücre hayatta kalımını azalttı. MYDGF deneysel olarak azaltıldığında, hipoksi çok daha öldürücü hâle geldi; özellikle ferroptoz yoluyla: lipid hasarı ve demir kaynaklı oksidatif stres belirteçleri arttı, mitokondriler hasarlı ve büzülmüş bir görünüme büründü ve güçlü bir ferroptoz inhibitörü hücreleri büyük ölçüde kurtardı. Gastrik kanser nakilleri taşıyan farelerde MYDGF’yi artırmak, bir ferroptoz indükleyici ilacın tümör küçültme etkisini azalttı; buna karşılık LCN2 adlı eşlikçi proteini engellemek ters etki gösterdi ve bu yolun canlı tümörlerde işlediğini doğruladı.
Kanser hücrelerinin demir bağlayan koruyucusunu nasıl koruduğu
Daha derine indiklerinde, yazarlar kritik aşağı akış oyuncusu olarak demir bağlayan protein LCN2’yi tanımladılar. Hipoksi altında, LCN2 proteininin düzeyi gen etkinliği değişmemesine rağmen düştü; bu durum üretim azalmasından çok aktif yıkımı işaret ediyordu. LCN2’nin normalde ubikitin ile etiketlenip endoplazmik retikulum ilişkili degradasyon (ER‑associated degradation) olarak bilinen kalite kontrol yoluyla proteazoma gönderildiğini gösterdiler. UBQLN1 adlı bir taşıyıcı adaptör, ubikitinlenmiş LCN2’yi bu yıkım makinelerine teslim ediyor. MYDGF ise bir koruma görevi görüyor: UBQLN1’e belirli bir kenetlenme bölgesinde bağlanarak LCN2’yi dışluyor ve proteazoma teslim edilmesini engelliyor. Sonuç olarak LCN2 proteini stabil kalıyor, reaktif demiri bağlamaya devam ediyor ve ferroptozu tetikleyen lipid peroksidasyonunu azaltıyor.
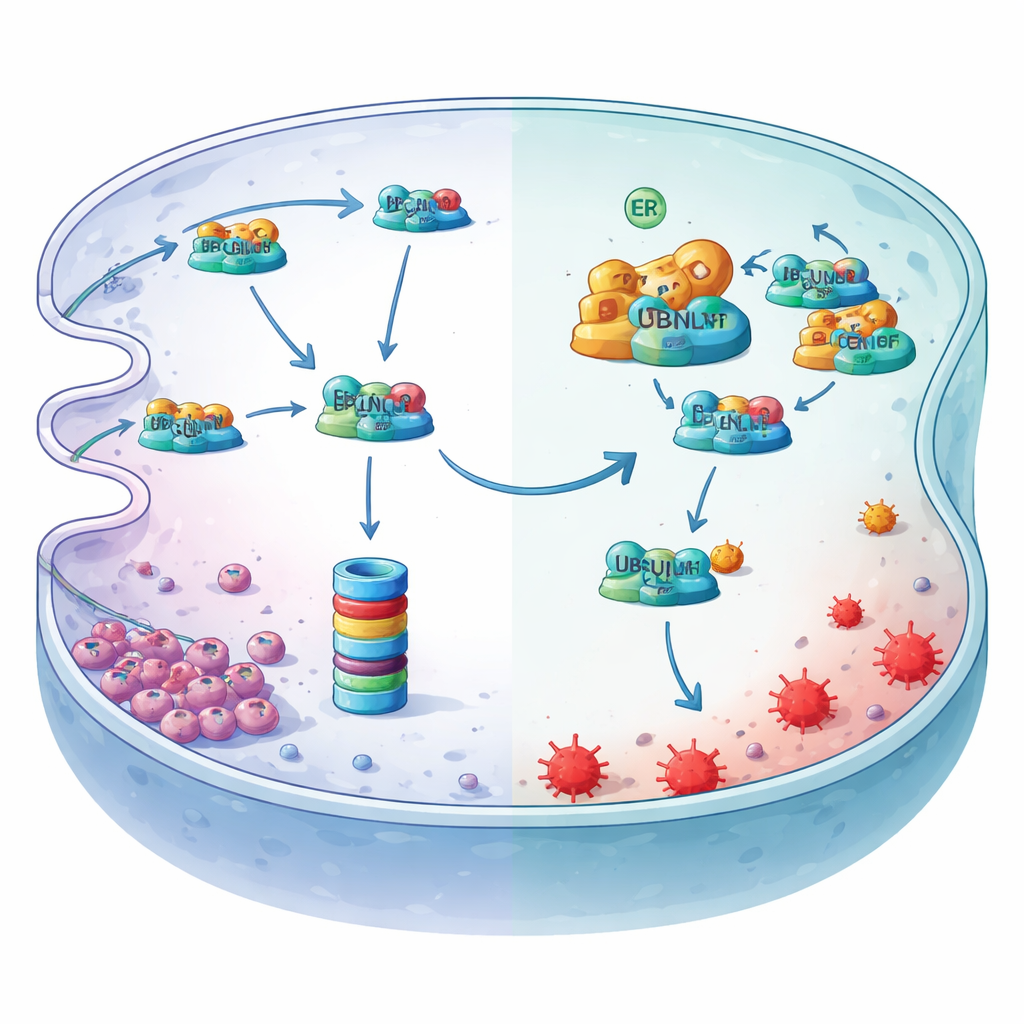
Hipoksi yukarı akıştaki ana anahtarı çeviriyor
Çalışma ayrıca hipoksinin bu koruyucu ekseni nasıl açığa çıkardığını ortaya koyuyor. Düşük oksijen endoplazmik retikulumda stres oluşturuyor ve XBP1s adı verilen, kesilmiş biçimdeki bir transkripsiyon faktörünü aktive ediyor. Araştırmacılar MYDGF geninin kontrol bölgesini tarayarak ve kromatin‑bağlanma ile raporlayıcı deneyler kullanarak XBP1s’nin belirli bir bölgede kenetlendiğini ve doğrudan MYDGF üretimini artırdığını gösterdiler. XBP1s azaltıldığında MYDGF düzeyleri düştü, LCN2 seviyeleri azaldı ve ferroptoz belirteçleri yükseldi—bu etkiler MYDGF veya LCN2 yeniden sağlanarak geri döndürülebiliyordu. Birlikte, bu deneyler doğrusal bir korunma hattını özetliyor: hipoksi XBP1s’yi aktive ediyor, XBP1s MYDGF’yi artırıyor, MYDGF UBQLN1 kaynaklı LCN2 yıkımını engelliyor, böylece LCN2 demiri bünyesinde tutup gastrik kanser hücrelerini ferroptozdan koruyor.
İnatçı mide tümörlerini köşeye sıkıştırmanın yeni yolları
Uzman olmayanlar için çıkarım şudur: Hipoksik mide tümörleri, demir bağlayan koruyucu bir proteini umut verici bir hücre ölümünden kaçmak için yeterince uzun süre yaşatan dahili bir "acil hat" oluşturmuş durumda. XBP1s–MYDGF–UBQLN1–LCN2 zincirini ayrıntılarıyla haritalayarak çalışma, bazı tümör bölgelerinin neden ferroptoz temelli tedavilere dirençli olabileceğini açıklıyor ve bu savunmayı etkisiz kılmaya yönelik somut stratejilere işaret ediyor—örneğin MYDGF’yi, XBP1s’yi veya UBQLN1 üzerindeki etkileşim yüzeylerini engellemek. Bu tür müdahaleler güvenli bir şekilde hastalara çevrilebilirse, gelecekte ferroptoz tetikleyici ilaçların mide kanserlerinin en tedaviye dirençli, oksijen yoksunu bölgelerinde daha etkili olmasına yardımcı olabilir.
Atıf: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Anahtar kelimeler: mide kanseri, hipoksi, ferroptoz, protein degradasyonu, demir metabolizması