Clear Sky Science · nl
Door hypoxie geïnduceerde XBP1s-MYDGF-as remt ferroptose via UBQLN1-gemedieerde stabilisatie van LCN2 bij maagkanker
Waarom het uithongeren van tumoren van ijzer ertoe doet
Maagkanker behoort tot de dodelijkste kankers ter wereld, deels omdat tumorcellen opmerkelijk goed leren overleven in zuurstofarme, of hypoxische, zones diep in de maagwand. Veel nieuwe geneesmiddelen proberen kankercellen te doden door een vorm van ijzerafhankelijke celdood teweeg te brengen die ferroptose heet. Deze studie stelt een cruciale vraag voor toekomstige patiënten: hoe ontlopen hypoxische maagtumoren deze ijzerafhankelijke dood, en kan die ontsnappingsroute worden geblokkeerd?
Een verborgen reddingslijn binnen zuurstofarme tumoren
Met grote single‑cell RNA‑sequencing datasets van menselijk maagweefsel brachten de onderzoekers genactiviteit cel voor cel in kaart tijdens de progressie van normaal slijmvlies naar gevorderde maagkanker. Ze vonden dat maligne epitheliale cellen een uitgescheiden eiwit genaamd myeloid‑derived growth factor (MYDGF) veel sterker inschakelen dan nabijgelegen gezonde cellen. Deze MYDGF‑rijke kankercellen toonden ook sterke signaturen van eiwitverwerking en afbraak binnen het endoplasmatisch reticulum, wat suggereert dat MYDGF verbonden kan zijn met hoe tumorcellen het leven en de dood van sleutelproteïnen reguleren.
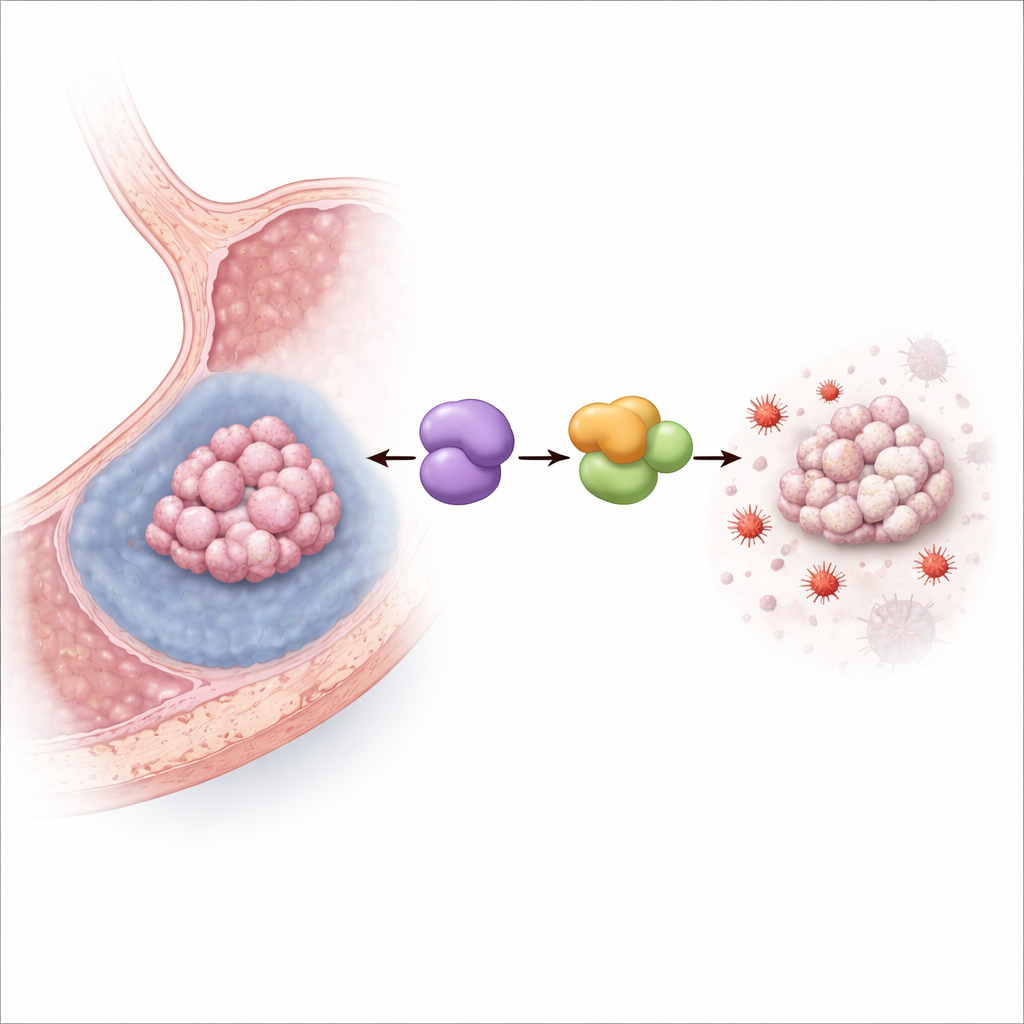
Het uitschakelen van ijzergedreven celdood
Het team kweekte vervolgens menselijke maagkankercellen onder hypoxische condities die het uitgehongerde binnenste van solide tumoren nabootsen. Lage zuurstof verhoogde MYDGF‑niveaus en verminderde, zoals verwacht, de overleving van cellen. Wanneer MYDGF experimenteel werd verlaagd, werd hypoxie veel dodelijker, vooral via ferroptose: merkers van lipidedamage en ijzer‑gedreven oxidatieve stress schoten omhoog, mitochondriën kregen een beschadigd, gekrompen uiterlijk, en een krachtige ferroptose‑remmer redde grotendeels de cellen. In muizen met maagkankerxenografts verminderde het verhogen van MYDGF het tumorkrimpende effect van een ferroptose‑inducerend middel, terwijl blokkade van een partnerproteïne genaamd LCN2 het tegenovergestelde effect had, wat bevestigt dat deze route ook in levende tumoren werkt.
Hoe kankercellen hun ijzerbindende beschermer afschermen
Dieper gravend identificeerden de auteurs LCN2, een ijzerbindend eiwit, als de kritieke downstreamspeler. Onder hypoxie daalden de eiwitniveaus van LCN2 hoewel de genactiviteit niet veranderde, wat wijst op actieve afbraak in plaats van verminderde productie. Ze toonden aan dat LCN2 normaal wordt gemerkt met ubiquitine en via een kwaliteitscontrolespoor van het endoplasmatisch reticulum, bekend als ER‑associated degradation (ERAD), naar de proteasoom‑afbraakeenheid wordt geleid. Een transportadaptor genaamd UBQLN1 levert het geubiquitineerde LCN2 aan dit afbraaksysteem. MYDGF treedt op als lijfwacht: het bindt aan UBQLN1 op een specifiek aangrijpingsdomein, waardoor LCN2 wordt verdrongen en de overdracht naar het proteasoom wordt voorkomen. Daardoor wordt LCN2‑eiwit gestabiliseerd, blijft het reactief ijzer binden en dempt het de lipideperoxidatie die ferroptose aandrijft.
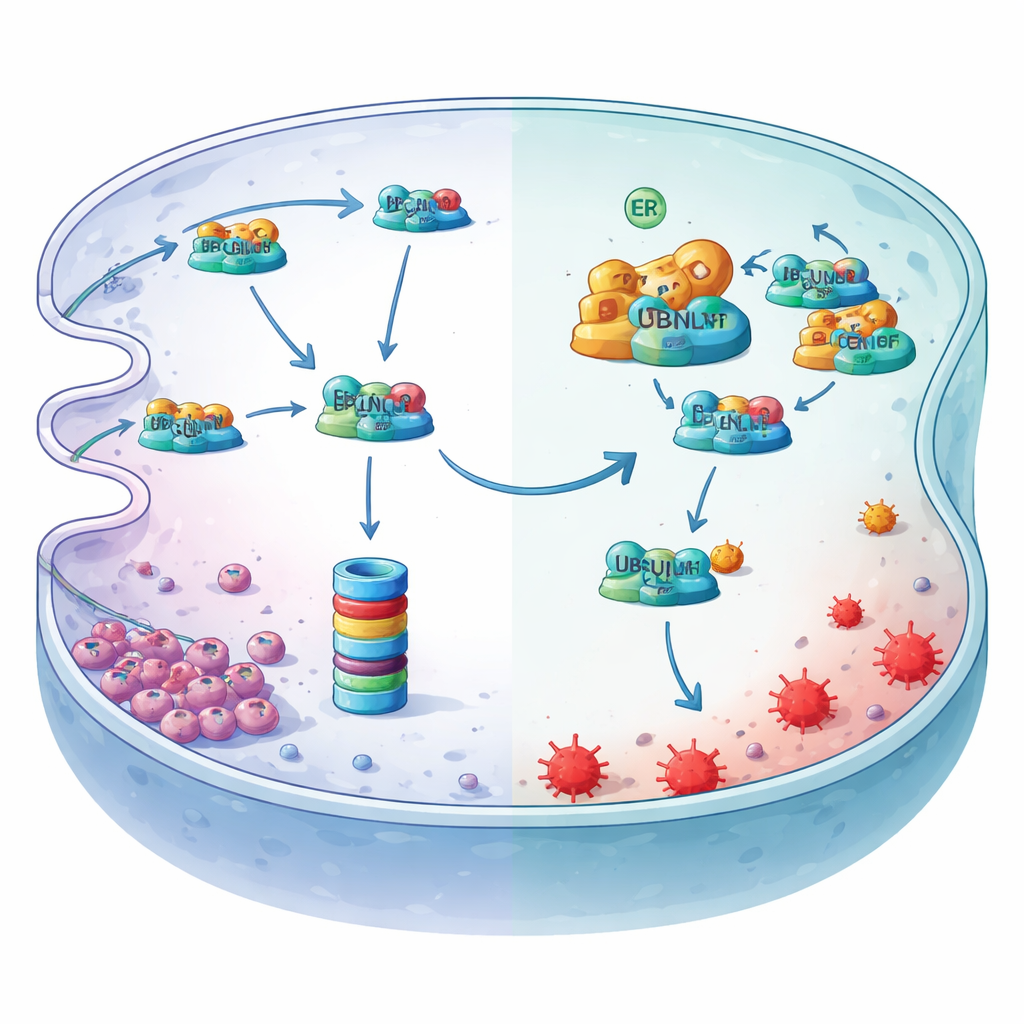
Hypoxie schakelt de bovenliggende schakelaar om
De studie onthult ook hoe hypoxie deze beschermende as activeert. Lage zuurstof belast het endoplasmatisch reticulum en activeert een gespliceerde vorm van de transcriptiefactor XBP1s. Door de regelregio van het MYDGF‑gen te scannen en chromatinebindende en reporterassays te gebruiken, lieten de onderzoekers zien dat XBP1s op een specifieke site bindt en direct de productie van MYDGF opvoert. Wanneer XBP1s werd geremd, daalden MYDGF‑niveaus, vielen LCN2‑niveaus terug en stegen ferroptose‑merkers — effecten die ongedaan konden worden gemaakt door MYDGF of LCN2 te herstellen. Samen beschrijven deze experimenten een lineaire bescherming: hypoxie activeert XBP1s, dat MYDGF opdrijft, dat de UBQLN1‑gedreven vernietiging van LCN2 blokkeert, waarna LCN2 ijzer opvangt en maagkankercellen beschermt tegen ferroptose.
Nieuwe manieren om hardnekkige maagtumoren in het nauw te drijven
Voor niet‑experts is de conclusie dat hypoxische maagtumoren een interne 'noodlijn' hebben gebouwd die een ijzerbindend beschermend eiwit net lang genoeg in leven houdt om een veelbelovende nieuwe vorm van celdood te vermijden. Door deze XBP1s–MYDGF–UBQLN1–LCN2‑keten gedetailleerd in kaart te brengen, verklaart het werk waarom sommige tumorgedeelten resistent kunnen zijn tegen therapieën gebaseerd op ferroptose en wijst het op concrete strategieën om die verdediging uit te schakelen — zoals het blokkeren van MYDGF, XBP1s of de interactieoppervlakken op UBQLN1. Als dergelijke interventies veilig naar patiënten kunnen worden vertaald, kunnen ze helpen dat ferroptose‑inducerende middelen beter werken in de meest therapieresistente, zuurstof‑arme delen van maagkankers.
Bronvermelding: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Trefwoorden: maagkanker, hypoxie, ferroptose, eiwitafbraak, ijzermetabolisme