Clear Sky Science · he
ציר XBP1s–MYDGF המושרה על ידי היפוקסיה מדכא פרופרוטוזה דרך היציבות של LCN2 באמצעות UBQLN1 בסרטן הקיבה
מדוע חנק ברזל בגידולים חשוב
סרטן הקיבה הוא אחד הסרטן הקטלניים בעולם, בין השאר מפני שתאי הגידול מפתחים יכולת יוצאת דופן לשרוד בכיסי חוסר־חמצן (היפוקסיה) עמוקים בדופן הקיבה. תרופות חדשות רבות מנסות להרוג תאים סרטניים על־ידי זירוז צורת מוות תאית מונעת־ברזל הנקראת פרופרוטוזה. המחקר הזה שואל שאלה מכרעת למטופלים עתידיים: כיצד גידולי קיבה ההיפוקסיים מתחמקים ממות תלויית־ברזל זו, והאם אפשר לחסום את דרך הבריחה הזו?
קו הצלה סמוי בתוך גידולים דלים בחמצן
באמצעות מערכי נתונים גדולים של רצף RNA חד‑תאי מרקמות קיבה אנושיות, החוקרים מיפו פעילות גנים תא‑תא לאורך ההתקדמות מרירית תקינה לסרטן קיבה מתקדם. הם גילו שתאים אפיתליאליים ממאירים מדליקים חלבון מופרש בשם גורם גדילה נגזר ממיאלואידי (MYDGF) בעוצמה רבה הרבה יותר מתאים בריאים צמודים. תאי סרטן עם רמות גבוהות של MYDGF הפגינו גם סימנים חזקים של מערכות טיפול ובזבוז חלבונים בתוך הרשתית האנדופלזמטית, דבר המצביע על כך ש‑MYDGF עשוי להיות קשור לאופן שבו תאים סרטניים מנהלים חיים ומוות של חלבונים מפתח.
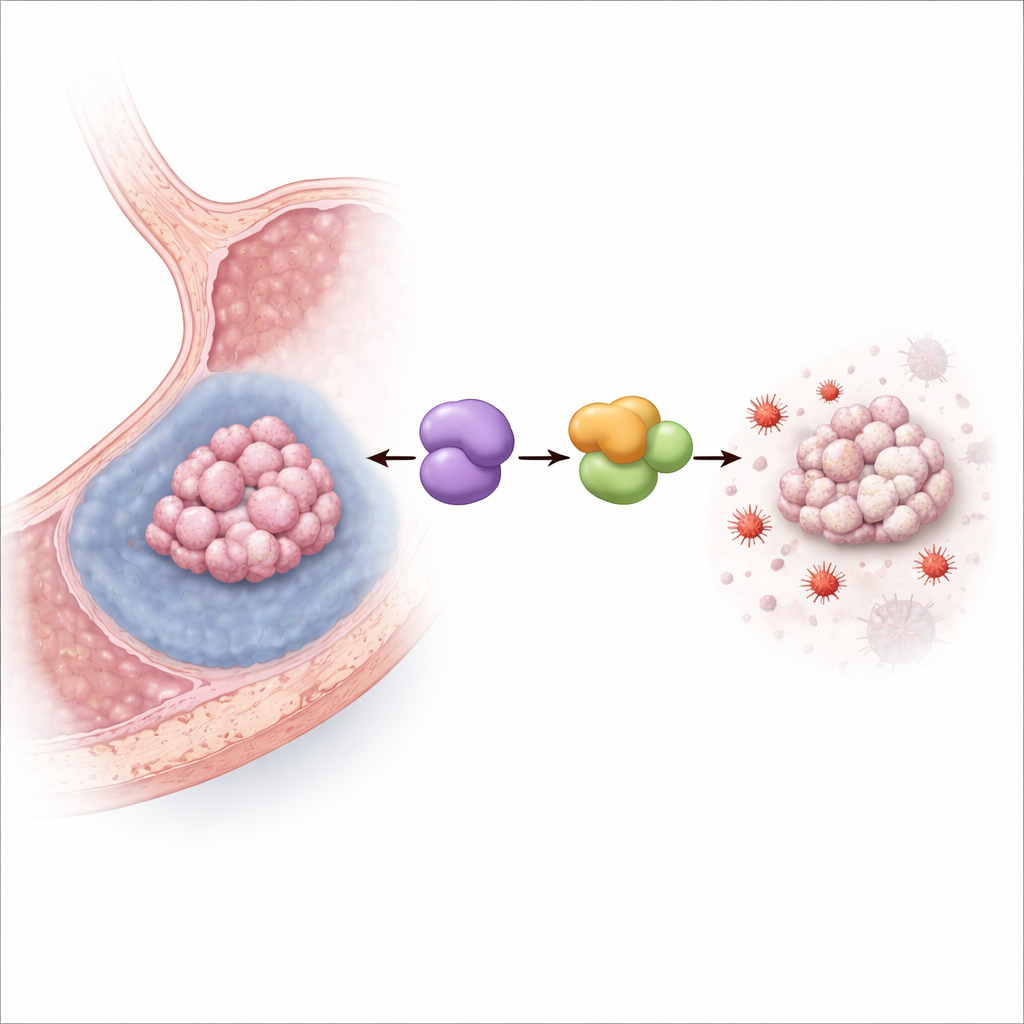
כיבוי מוות תאי מונע־ברזל
הצוות גדל אז תאי סרטן קיבה אנושיים בתנאי היפוקסיה המדמים את פנים הגידול הרעב לחמצן. חוסר חמצן העלה את רמות MYDGF וכפי שצפו, צמצם את הישרדות התאים. כאשר MYDGF הופחת ניסויית, ההיפוקסיה הפכה להרבה יותר קטלנית, ובמיוחד דרך פרופרוטוזה: סמני נזק לליפידים ולדחק חמצוני מונע־ברזל זינקו, המיטוכונדריה קיבלו מראה פגום ומכווץ, ומעכב עוצמתי של פרופרוטוזה הציל ברובו את התאים. בעכברים שנושאים השתלות סרטן קיבה, הגברת MYDGF צמצמה את השפעת הכיווץ של גידול על‑ידי תרופה המפעילה פרופרוטוזה, בעוד חסימת חלבון שותף בשם LCN2 הפכה את המצב—מה שאישר שהמסלול הזה פועל בגידולים חיים.
כיצד תאים סרטניים מגוננים על שומר הברזל שלהם
בחינה מעמיקה יותר זיהתה את LCN2, חלבון קשור־ברזל, כשחקן קריטי שממוקם במורד הזרם. תחת היפוקסיה רמות החלבון של LCN2 ירדו אף על פי שפעילות הגן שלו לא ירדה, מה שמעיד על פירוק פעיל ולא על ירידה בייצור. הם הראו ש‑LCN2 בדרך כלל מתויג באוביקוויטין ומוזרם למטחנת החלבונים של התא, הפרוטאוזום, דרך מסלול בקרת איכות של הרשתית האנדופלזמטית הידוע כ־ER‑associated degradation. מתאם טרנספורט בשם UBQLN1 מספק את LCN2 המתויג לאותן מכונות פירוק. כאן נכנס MYDGF כשומר: הוא נקשר ל‑UBQLN1 בתחום עגינה ספציפי, דוחק החוצה את LCN2 ומונע את מסירתו לפרוטאוזום. כתוצאה מכך, חלבון LCN2 מייצב עצמו, ממשיך לקשור ברזל תגובתי ומרכך את הפראוקסידציה של ליפידים שמניעה את הפרופרוטוזה.
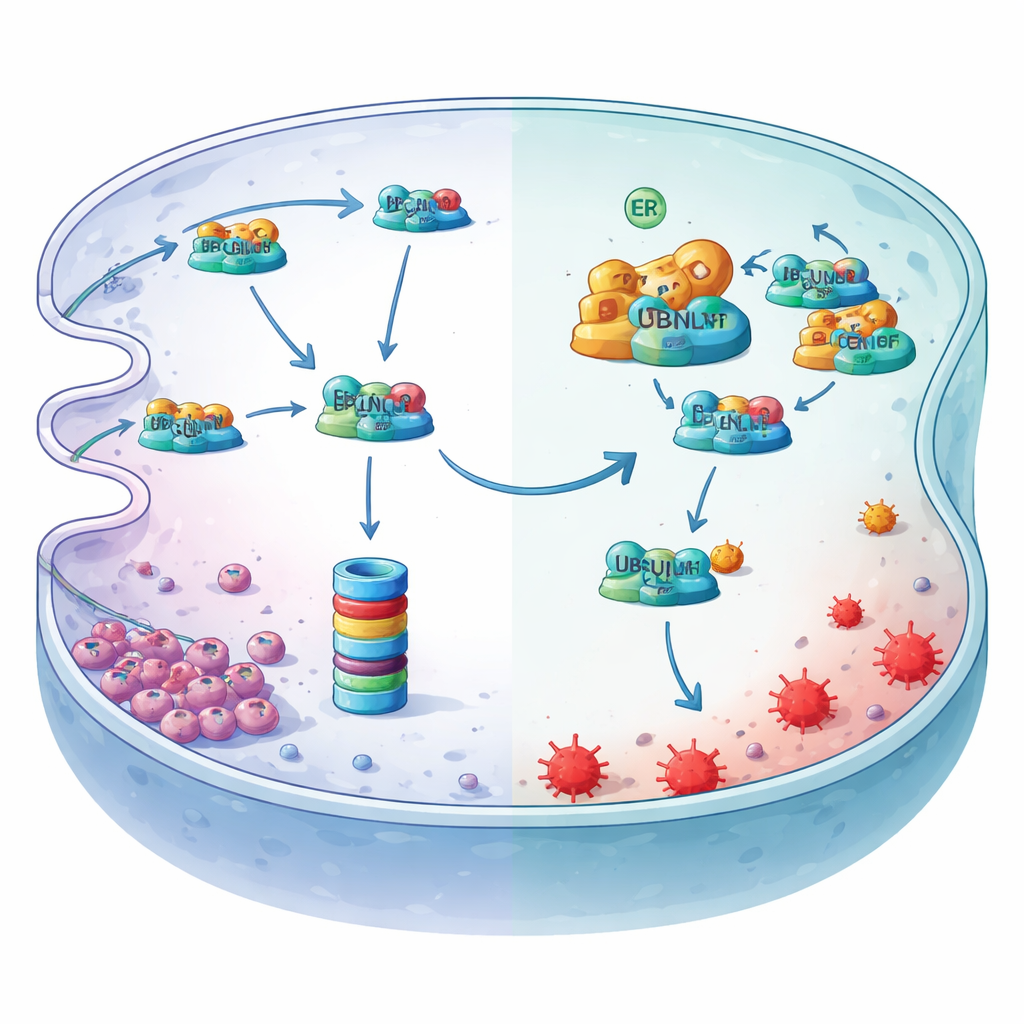
היפוקסיה מפעילה את מתג המאסטר במעלה הזרם
המחקר גם חושף כיצד היפוקסיה מפעילה את הציר המגן הזה. חוסר חמצן מעמיס על הרשתית האנדופלזמטית ומפעיל צורה מסוייגת (מושתלת‑חיתוך) של פקטור שעתוק בשם XBP1s. על‑ידי סריקה של אזור הבקרה של גן MYDGF ושימוש בניסויי קשירת כרומטין ודוחות, החוקרים הראו ש‑XBP1s עוגן באתר ספציפי ומגבירה ישירות את ייצור MYDGF. כאשר XBP1s הופחת, רמות MYDGF ירדו, רמות LCN2 צנחו וסמני פרופרוטוזה עלו—השפעות שניתן היה לבטל על‑ידי שחזור MYDGF או LCN2. ביחד, הניסויים משרטטים מגן ליניארי: היפוקסיה מפעילה XBP1s, שמגבירה MYDGF, שחוסמת את ההרס שמניע UBQLN1 של LCN2, אשר לאחר מכן קולטת ברזל ומגנה על תאי סרטן הקיבה מפרופרוטוזה.
דרכים חדשות לסגור פינות על גידולי קיבה עקשניים
לעיני הקוראים הלא‑מומחים, המסקנה היא שגידולי קיבה היפוקסיים בנו "קו חירום" פנימי שמחזיק חלבון שומר־ברזל בחיים מספיק זמן כדי להימנע מצורת מוות תאית מבטיחה. על ידי מיפוי מפורט של שרשרת XBP1s–MYDGF–UBQLN1–LCN2, העבודה מסבירה מדוע אזורים מסוימים בגידול עשויים לעמוד בפני טיפולים מבוססי פרופרוטוזה ומצביעה על אסטרטגיות קונקרטיות לנטרול ההגנה—כגון חסימת MYDGF, XBP1s או משטחים אינטראקציה ב‑UBQLN1. אם ניתן לתרגם התערבויות כאלה בבטחה למטופלים, הן עשויות לשפר את יעילות התרופות המפעילות פרופרוטוזה בחלקים העקשניים ביותר, דלי־החמצן של סרטן הקיבה.
ציטוט: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
מילות מפתח: סרטן הקיבה, היפוקסיה, פרופרוטוזה, דה־גרדציה של חלבונים, מטבוליזם הברזל