Clear Sky Science · pt
Eixo XBP1s–MYDGF induzido por hipóxia suprime a ferroptose por meio da estabilização de LCN2 mediada por UBQLN1 no câncer gástrico
Por que privar tumores de ferro importa
O câncer gástrico está entre os mais letais do mundo, em parte porque as células tumorais se tornam notavelmente hábeis em sobreviver em bolsões com baixo oxigênio, ou hipóxia, no interior da parede do estômago. Muitos fármacos novos visam matar células cancerosas desencadeando uma forma de morte celular dependente de ferro chamada ferroptose. Este estudo aborda uma questão crucial para pacientes futuros: como tumores gástricos hipóxicos escapam dessa forma de morte dependente de ferro, e esse caminho de escape pode ser bloqueado?
Uma linha de resgate oculta dentro de tumores pobres em oxigênio
Usando grandes conjuntos de dados de transcriptoma de célula única de tecido gástrico humano, os pesquisadores mapearam a atividade gênica célula a célula ao longo da progressão do epitélio normal até o câncer gástrico desenvolvido. Eles descobriram que células epiteliais malignas ativam uma proteína secretada chamada fator de crescimento derivado de mieloide (MYDGF) muito mais fortemente do que células saudáveis vizinhas. Essas células cancerosas com alto teor de MYDGF também exibiram assinaturas fortes de sistemas de manejo e descarte de proteínas no retículo endoplasmático, sugerindo que o MYDGF pode estar ligado à forma como células tumorais controlam a vida e a morte de proteínas-chave.
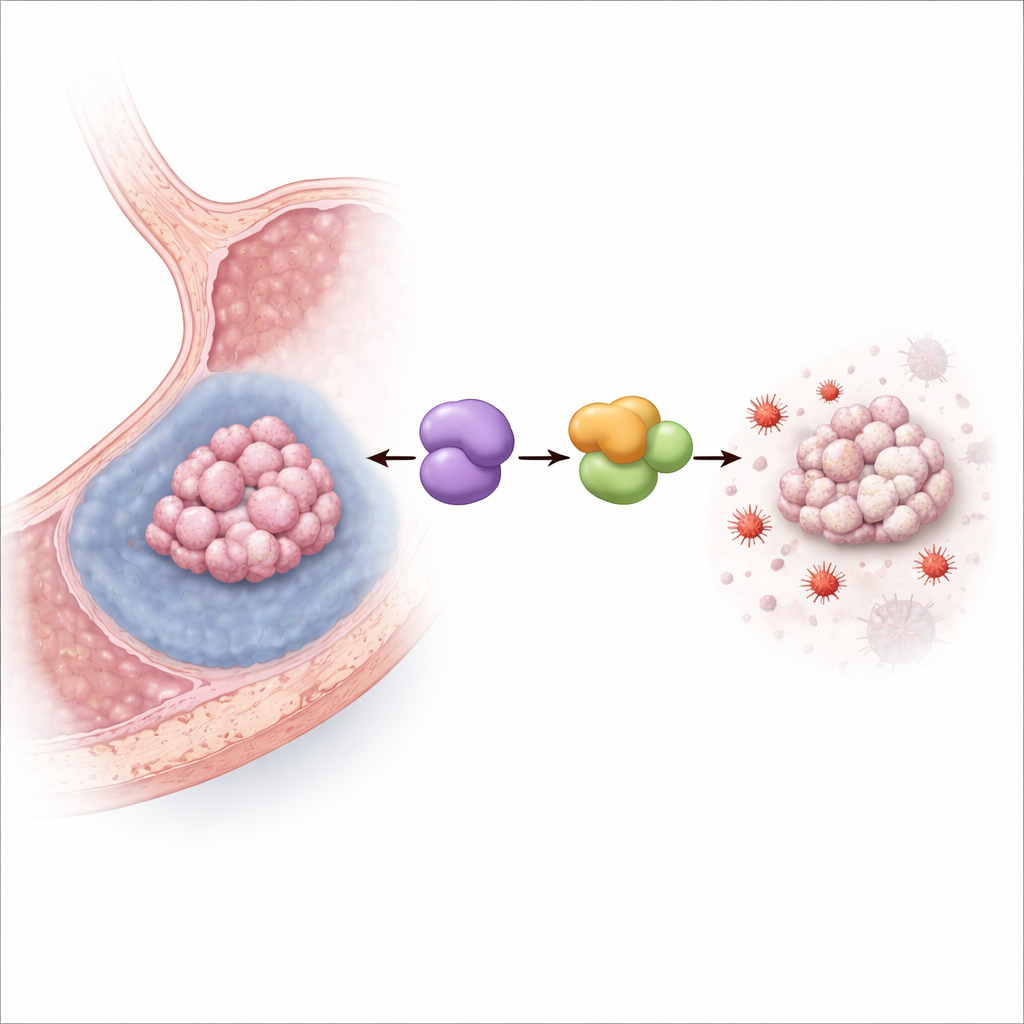
Desligando a morte celular impulsionada por ferro
A equipe então cultivou células de câncer gástrico humano sob condições hipóxicas que imitam o interior faminto de tumores sólidos. O baixo oxigênio aumentou os níveis de MYDGF e, como esperado, reduziu a sobrevivência celular. Quando o MYDGF foi experimentalmente reduzido, a hipóxia tornou‑se muito mais letal, sobretudo por ferroptose: marcadores de dano lipídico e estresse oxidativo impulsionado por ferro dispararam, as mitocôndrias adotaram uma aparência encolhida e danificada, e um potente inibidor de ferroptose resgatou em grande parte as células. Em camundongos com enxertos de câncer gástrico, aumentar o MYDGF reduziu o efeito de encolhimento tumoral de um fármaco que induz ferroptose, enquanto bloquear uma proteína parceira chamada LCN2 teve o efeito oposto, confirmando que essa via opera em tumores vivos.
Como as células cancerosas protegem seu guardião de ligação ao ferro
Aprofundando, os autores identificaram LCN2, uma proteína de ligação ao ferro, como o jogador crítico a jusante. Sob hipóxia, os níveis proteicos de LCN2 caíram mesmo que sua atividade gênica não tenha diminuído, apontando para destruição ativa em vez de menor produção. Eles mostraram que LCN2 normalmente é marcado com ubiquitina e direcionado para o triturador proteico da célula, o proteassoma, por meio de uma via de controle de qualidade do retículo endoplasmático conhecida como degradação associada ao retículo (ER‑associated degradation). Um adaptador de transporte chamado UBQLN1 entrega a LCN2 ubiquitinada a esse maquinário de degradação. O MYDGF entra como um guarda‑costas: ele se liga à UBQLN1 em um domínio de acoplamento específico, deslocando a LCN2 e impedindo sua entrega ao proteassoma. Como resultado, a proteína LCN2 é estabilizada, continua a sequestrar ferro reativo e reduz a peroxidação lipídica que impulsiona a ferroptose.
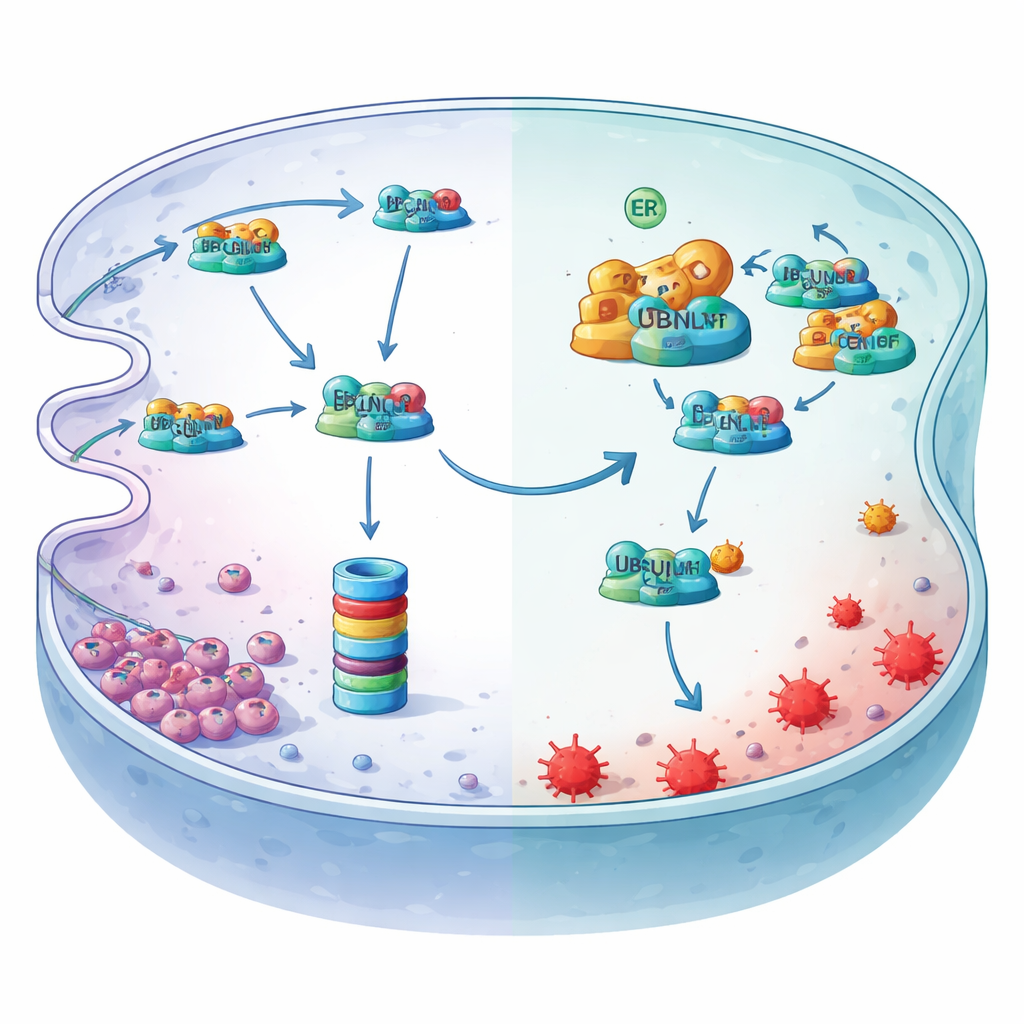
Hipóxia vira o interruptor mestre a montante
O estudo também revela como a hipóxia liga esse eixo protetor. O baixo oxigênio estressa o retículo endoplasmático e ativa uma forma emendadade um fator de transcrição chamada XBP1s. Ao escanear a região reguladora do gene MYDGF e usando ensaios de ligação à cromatina e repórter, os pesquisadores mostraram que o XBP1s se acomoda em um sítio específico e aumenta diretamente a produção de MYDGF. Quando XBP1s foi reduzido, os níveis de MYDGF caíram, os níveis de LCN2 diminuíram e os marcadores de ferroptose aumentaram — efeitos que podiam ser revertidos restaurando MYDGF ou LCN2. Juntos, esses experimentos delineiam uma salvaguarda linear: hipóxia ativa XBP1s, que aumenta MYDGF, que bloqueia a destruição de LCN2 dirigida por UBQLN1, que então absorve ferro e protege as células de câncer gástrico da ferroptose.
Novas formas de encurralar tumores gástricos persistentes
Para não especialistas, a conclusão é que tumores gástricos hipóxicos construíram uma "linha de emergência" interna que mantém uma proteína protetora de ligação ao ferro viva tempo suficiente para evitar uma promissora nova forma de morte celular. Ao mapear em detalhe a cadeia XBP1s–MYDGF–UBQLN1–LCN2, o trabalho explica por que algumas regiões tumorais podem resistir a terapias baseadas em ferroptose e aponta estratégias concretas para desarmar essa defesa — como bloquear MYDGF, XBP1s ou as superfícies de interação em UBQLN1. Se tais intervenções puderem ser traduzidas com segurança para pacientes, elas podem ajudar futuros fármacos indutores de ferroptose a funcionar melhor nas partes mais resistentes ao tratamento e privadas de oxigênio dos cânceres gástricos.
Citação: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Palavras-chave: câncer gástrico, hipóxia, ferroptose, degradação de proteínas, metabolismo do ferro