Clear Sky Science · fr
L’axe XBP1s–MYDGF induit par l’hypoxie supprime la ferroptose via la stabilisation de LCN2 médiée par UBQLN1 dans le cancer gastrique
Pourquoi priver les tumeurs de fer est important
Le cancer gastrique fait partie des cancers les plus meurtriers au monde, en partie parce que les cellules tumorales deviennent remarquablement efficaces pour survivre dans des poches à faible teneur en oxygène — ou hypoxiques — profondément ancrées dans la paroi de l’estomac. De nombreux médicaments récents visent à tuer les cellules cancéreuses en déclenchant une forme de mort cellulaire dépendante du fer appelée ferroptose. Cette étude pose une question cruciale pour les patients à venir : comment les tumeurs gastriques hypoxiques contournent‑elles cette mort dépendante du fer, et peut‑on bloquer cette voie d’échappement ?
Une ligne de secours cachée à l’intérieur des tumeurs pauvres en oxygène
En utilisant d’importants jeux de données de séquençage d’ARN unicellulaire provenant de tissus gastriques humains, les chercheurs ont cartographié l’activité génique cellule par cellule au cours de la progression de l’épithélium normal vers le cancer gastrique avancé. Ils ont constaté que les cellules épithéliales malignes activent de manière beaucoup plus marquée une protéine sécrétée appelée facteur de croissance dérivé des myéloïdes (MYDGF) que les cellules saines voisines. Ces cellules cancéreuses à forte expression de MYDGF montraient aussi des signatures prononcées des systèmes de prise en charge et d’élimination des protéines au sein du réticulum endoplasmique, ce qui suggère que MYDGF pourrait être lié à la façon dont les cellules tumorales gèrent la vie et la mort de protéines clés.
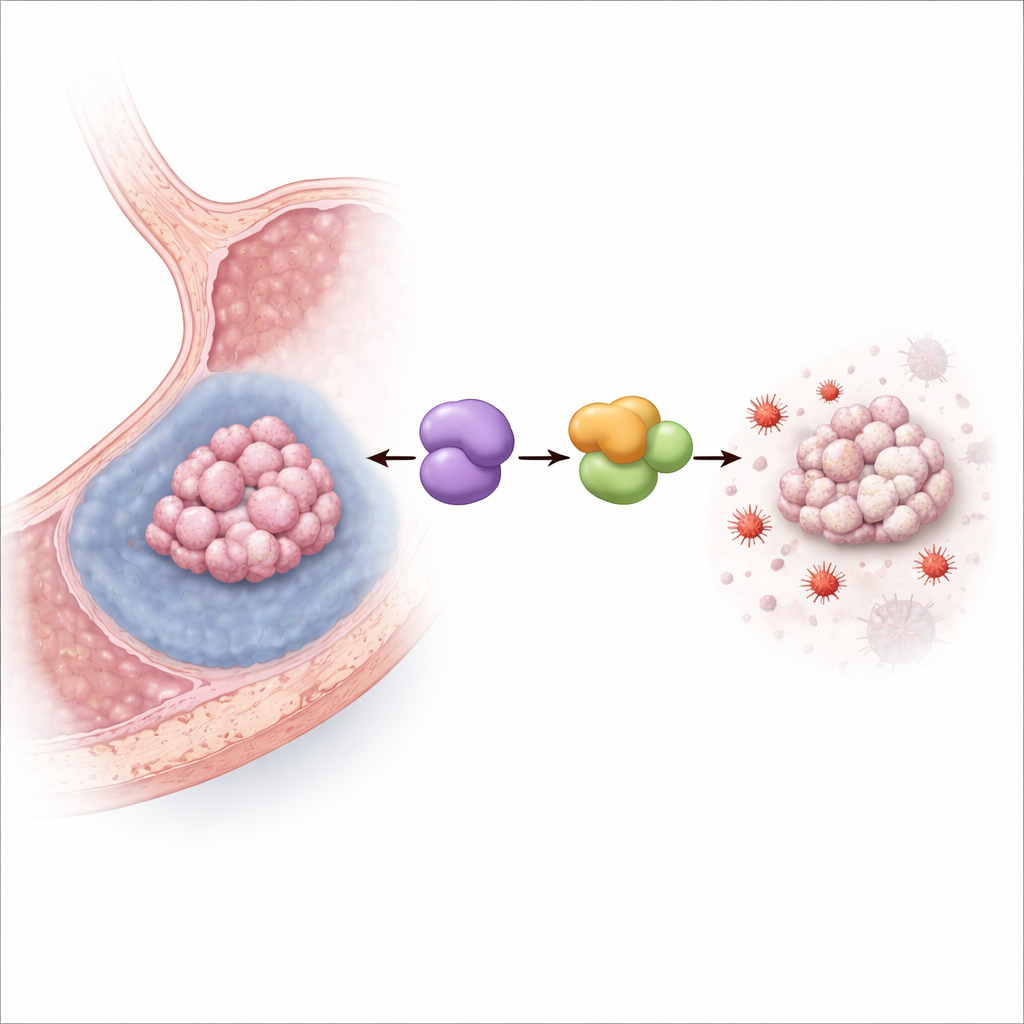
Désactiver la mort cellulaire induite par le fer
L’équipe a ensuite cultivé des cellules de cancer gastrique humain en conditions hypoxiques reproduisant l’intérieur appauvri en oxygène des tumeurs solides. La faible oxygénation a augmenté les niveaux de MYDGF et, comme prévu, réduit la survie cellulaire. Lorsque MYDGF a été réduit expérimentalement, l’hypoxie est devenue bien plus létale, en particulier par ferroptose : les marqueurs de dommages lipidiques et de stress oxydatif induit par le fer ont flambé, les mitochondries ont pris une apparence endommagée et rétractée, et un puissant inhibiteur de la ferroptose a en grande partie sauvé les cellules. Chez la souris porteuse de greffons de cancer gastrique, l’augmentation de MYDGF a atténué l’effet réducteur de tumeur d’un médicament induisant la ferroptose, tandis que le blocage d’une protéine partenaire appelée LCN2 produisait l’effet inverse, confirmant que cette voie fonctionne dans des tumeurs vivantes.
Comment les cellules cancéreuses protègent leur gardien liant le fer
En approfondissant, les auteurs ont identifié LCN2, une protéine liant le fer, comme l’acteur critique en aval. Sous hypoxie, les niveaux protéiques de LCN2 chutaient bien que son activité génique ne le fît pas, indiquant une destruction active plutôt qu’une réduction de la production. Ils ont montré que LCN2 est normalement marquée par l’ubiquitine et dirigée vers le broyeur protéique de la cellule, le protéasome, via une voie de contrôle qualité du réticulum endoplasmique connue sous le nom d’ER‑associated degradation (ERAD). Un adaptateur de transport appelé UBQLN1 délivre LCN2 ubiquitiné à ce dispositif de dégradation. MYDGF intervient comme un garde du corps : il se lie à UBQLN1 sur un domaine d’ancrage spécifique, évinçant LCN2 et empêchant sa remise au protéasome. En conséquence, la protéine LCN2 est stabilisée, continue de lier le fer réactif et atténue la peroxydation lipidique qui entraîne la ferroptose.
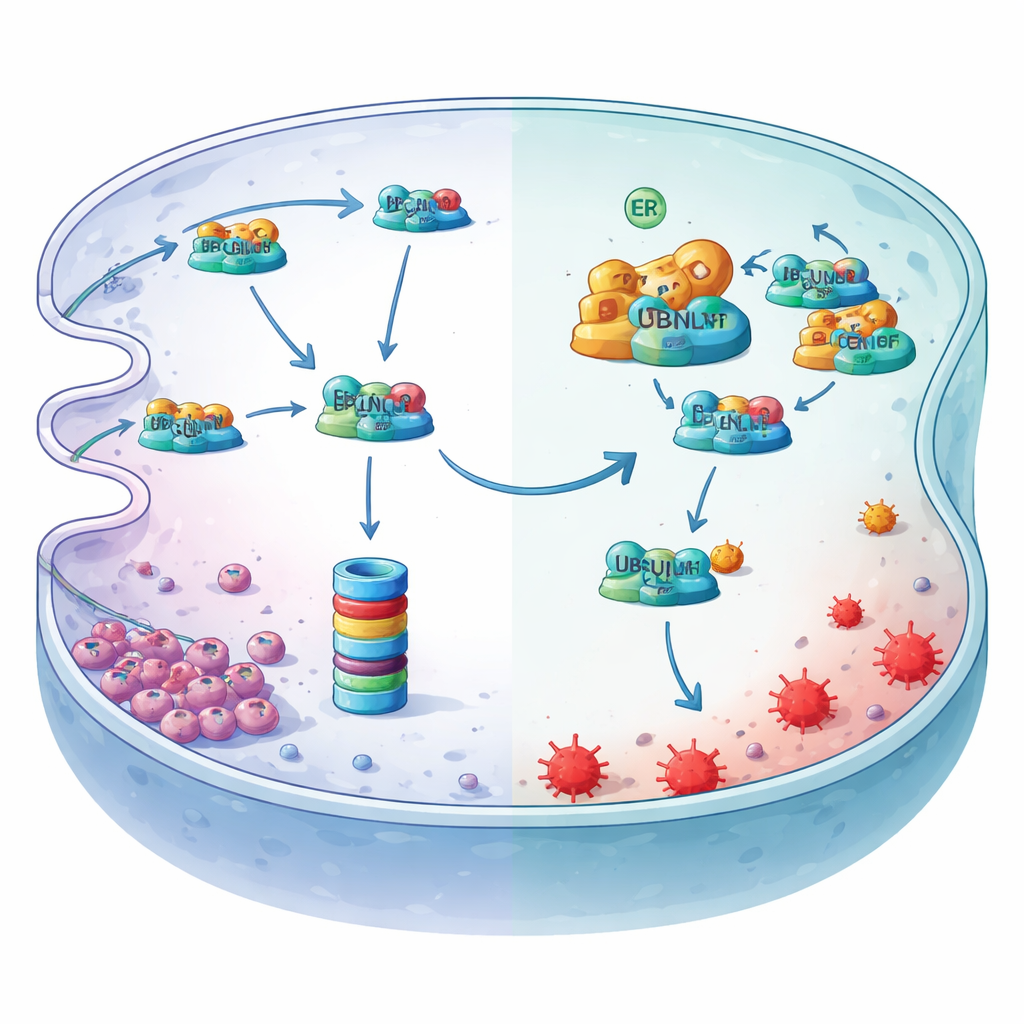
L’hypoxie actionne l’interrupteur maître en amont
L’étude révèle également comment l’hypoxie met en marche cet axe protecteur. La faible oxygénation stresse le réticulum endoplasmique et active une forme épissée d’un facteur de transcription appelé XBP1s. En sondant la région contrôle du gène MYDGF et en utilisant des essais d’occupation de la chromatine et de rapporteurs, les chercheurs ont montré que XBP1s se fixe à un site spécifique et augmente directement la production de MYDGF. Lorsque XBP1s a été réduit, les niveaux de MYDGF ont baissé, ceux de LCN2 ont chuté et les marqueurs de ferroptose ont augmenté — des effets qui pouvaient être inversés en restaurant MYDGF ou LCN2. Ensemble, ces expériences décrivent un mécanisme linéaire de protection : l’hypoxie active XBP1s, qui stimule MYDGF, lequel bloque la destruction de LCN2 par UBQLN1, permettant à LCN2 d’absorber le fer et de protéger les cellules du cancer gastrique de la ferroptose.
Nouvelles façons d’encercler les tumeurs gastriques récalcitrantes
Pour les non‑spécialistes, la conclusion est que les tumeurs gastriques hypoxiques ont construit une « ligne d’urgence » interne qui maintient une protéine protectrice liant le fer suffisamment longtemps pour éviter une forme prometteuse de mort cellulaire. En cartographiant en détail la chaîne XBP1s–MYDGF–UBQLN1–LCN2, ce travail explique pourquoi certaines régions tumorales peuvent résister aux thérapies basées sur la ferroptose et suggère des stratégies concrètes pour désarmer cette défense — comme bloquer MYDGF, XBP1s ou les surfaces d’interaction d’UBQLN1. Si de telles interventions peuvent être traduites en toute sécurité chez les patients, elles pourraient améliorer l’efficacité des médicaments inducteurs de ferroptose dans les régions les plus résistantes et appauvries en oxygène des cancers gastriques.
Citation: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Mots-clés: cancer gastrique, hypoxie, ferroptose, dégradation des protéines, métabolisme du fer