Clear Sky Science · ru
Ось XBP1s–MYDGF, индуцированная гипоксией, подавляет ферроптоз через стабилизацию LCN2 опосредованную UBQLN1 при раке желудка
Почему важно лишать опухоли железа
Рак желудка — один из самых смертоносных видов рака в мире, отчасти потому, что опухолевые клетки прекрасно приспосабливаются к выживанию в зонах с низким содержанием кислорода, или гипоксии, глубоко в стенке желудка. Многие новые препараты нацелены на то, чтобы убивать раковые клетки, вызывая форму гибели, зависящую от железа, называемую ферроптозом. В этом исследовании поставлен ключевой вопрос для будущих пациентов: как гипоксические опухоли желудка обходят эту железозависимую гибель и можно ли перекрыть этот путь ухода?
Скрытая линия спасения внутри кислородно‑бедных опухолей
Используя большие наборы данных одиночного клеточного РНК‑сиквенирования человеческой желудочной ткани, авторы картировали активность генов по отдельным клеткам на протяжении перехода от нормального эпителия к развернувшемуся раку желудка. Они обнаружили, что злокачественные эпителиальные клетки гораздо сильнее включают секрецируемый белок миелоид‑происходящего фактора роста (MYDGF) по сравнению с прилежащими здоровыми клетками. Эти клетки с высоким уровнем MYDGF также демонстрировали выраженные признаки систем обработки и утилизации белков в эндоплазматическом ретикулуме, что указывает на то, что MYDGF может быть связан с тем, как опухолевые клетки регулируют жизнь и гибель ключевых белков.
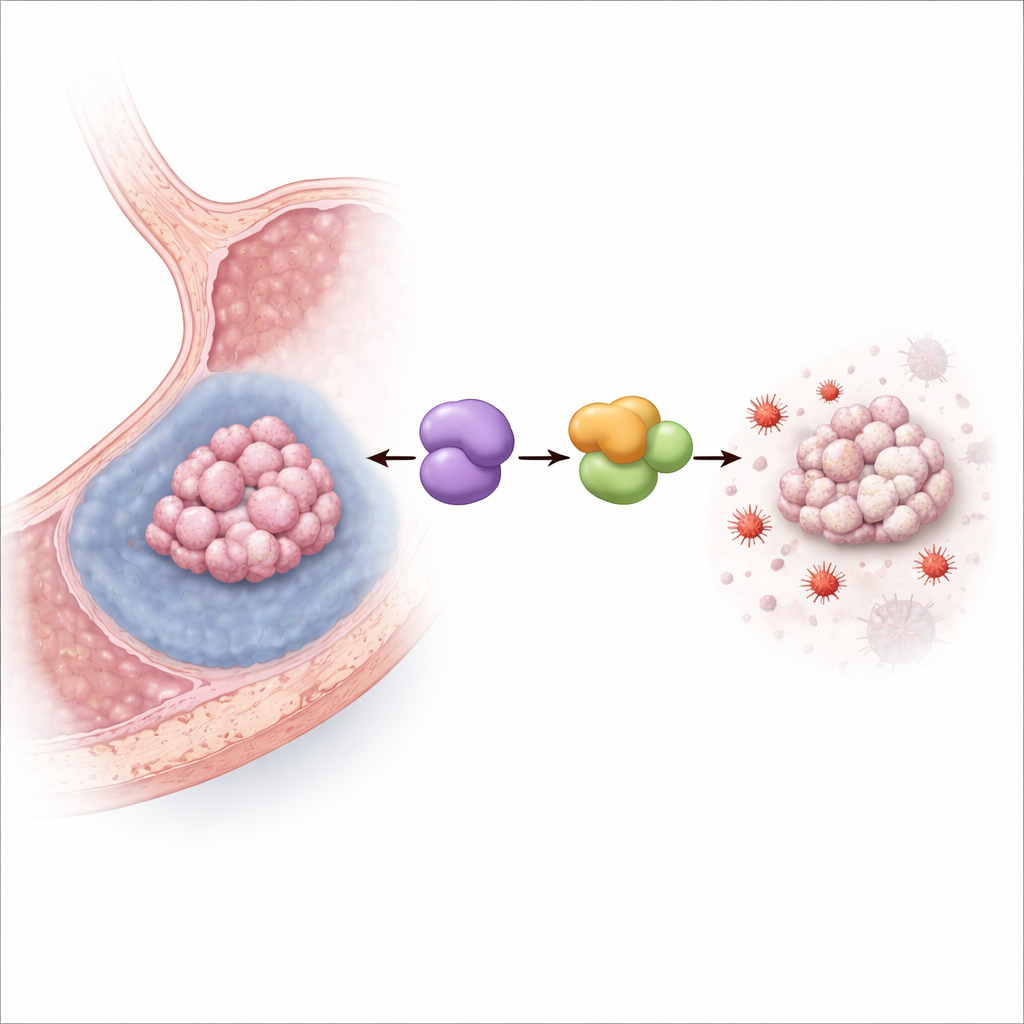
Выключение железозависимой гибели клеток
Далее команда выращивала человеческие клетки рака желудка в условиях гипоксии, имитирующих лишённую кислорода внутренность солидных опухолей. Низкий уровень кислорода повышал содержание MYDGF и, как следовало ожидать, снижал выживаемость клеток. При экспериментальном снижении MYDGF гипоксия становилась значительно более летальной, особенно за счёт ферроптоза: возрастали маркёры окислительного повреждения липидов и ионно‑железного стресса, митохондрии принимали повреждённый, сжатый вид, а сильный ингибитор ферроптоза в значительной степени спасал клетки. У мышей с трансплантатами рака желудка увеличение MYDGF ослабляло эффект препарата, индуцирующего ферроптоз, тогда как блокада связанного белка LCN2 давала противоположный эффект, подтверждая, что этот путь действует и в живых опухолях.
Как раковые клетки защищают своего железосвязывающего «охранника»
Углубляясь, авторы выделили LCN2, железосвязывающий белок, как критически важный нисходящий компонент. При гипоксии уровни белка LCN2 падали, несмотря на отсутствие снижения транскрипции, что указывало на активное разрушение, а не на уменьшение синтеза. Они показали, что LCN2 обычно помечается убиквитином и направляется в протеасому — клеточный «измельчитель» белков — через маршрут контроля качества в эндоплазматическом ретикулуме, известный как ER‑ассоциированная деградация. Транспортный адаптер UBQLN1 доставляет убиквитинированный LCN2 к этой системе деградации. В этом процессе MYDGF выступает телохранителем: он связывается с UBQLN1 в специфическом докинговом домене, вытесняя LCN2 и препятствуя его передаче в протеасому. В результате белок LCN2 стабилизируется, продолжает захватывать реактивное железо и снижает липидную перекисность, ведущую к ферроптозу.
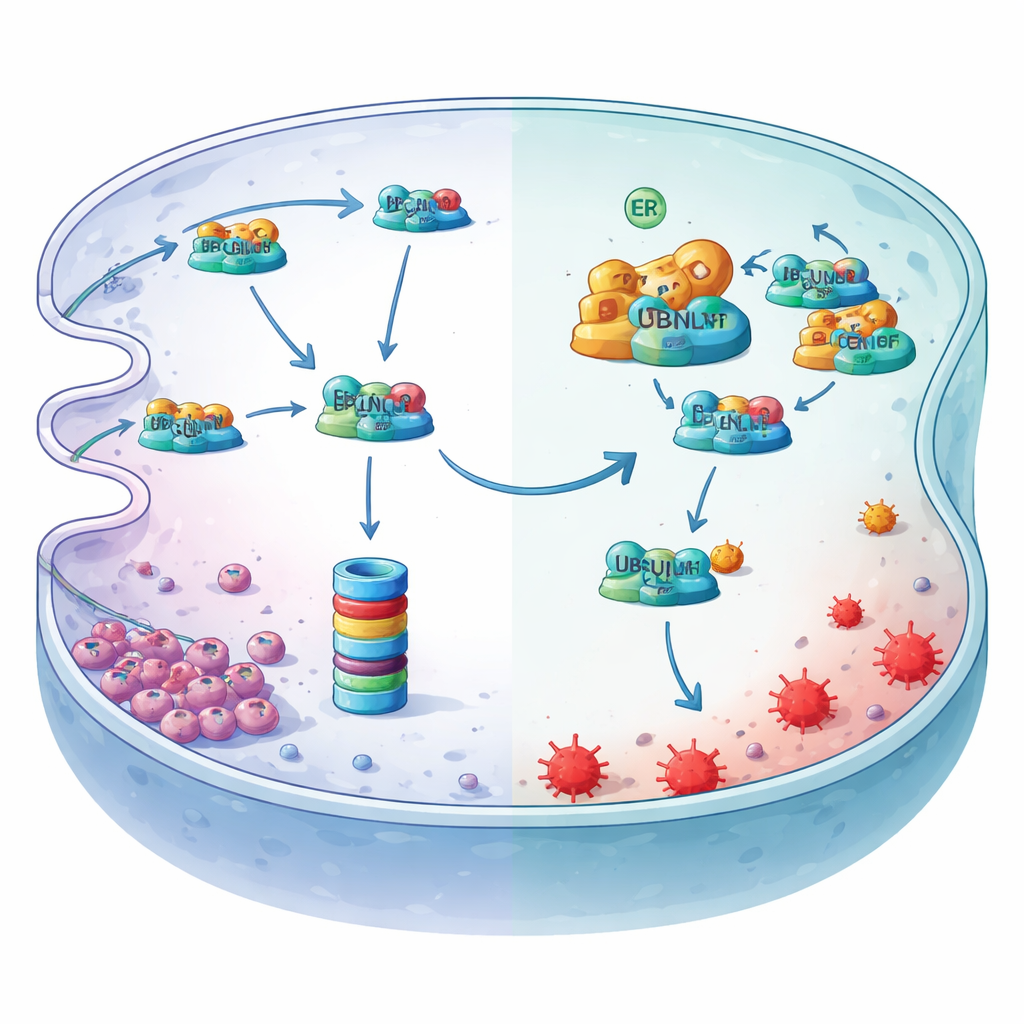
Гипоксия включает главный переключатель выше по цепочке
Исследование также показывает, как гипоксия включает эту защитную ось. Низкий кислород создаёт стресс в эндоплазматическом ретикулуме и активирует сплайсинговую форму транскрипционного фактора XBP1s. Сканируя контрольную область гена MYDGF и используя хроматин‑связывающие и репортерные анализы, исследователи продемонстрировали, что XBP1s прикрепляется к конкретному участку и прямо усиливает продукцию MYDGF. При снижении XBP1s уровни MYDGF падали, LCN2 снижался, а маркёры ферроптоза возрастали — эффекты, которые можно было обратить восстановлением MYDGF или LCN2. В совокупности эти эксперименты описывают линейный защитный механизм: гипоксия активирует XBP1s, что увеличивает MYDGF, который блокирует UBQLN1‑опосредованную деградацию LCN2, что затем поглощает железо и защищает клетки рака желудка от ферроптоза.
Новые подходы к взятию в угол упорных опухолей желудка
Для непрофессионалов основной вывод в том, что гипоксические опухоли желудка создали внутреннюю «аварийную линию», которая сохраняет жизнь железосвязывающему защитному белку достаточно долго, чтобы избежать перспективной новой формы гибели клеток. Подробное картирование цепочки XBP1s–MYDGF–UBQLN1–LCN2 объясняет, почему некоторые области опухоли могут сопротивляться терапии, основанной на ферроптозе, и указывает на конкретные стратегии подрыва этой защиты — например, блокаду MYDGF, XBP1s или взаимодействующих поверхностей UBQLN1. Если такие вмешательства удастся безопасно перевести в клинику, они могут помочь в повышении эффективности препаратов, индуцирующих ферроптоз, в самых устойчивых к лечению, лишённых кислорода участках рака желудка.
Цитирование: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Ключевые слова: рак желудка, гипоксия, ферроптоз, деградация белков, метаболизм железа