Clear Sky Science · es
El eje XBP1s–MYDGF inducido por hipoxia suprime la ferroptosis mediante la estabilización de LCN2 mediada por UBQLN1 en el cáncer gástrico
Por qué importa dejar a los tumores sin hierro
El cáncer gástrico es uno de los más letales del mundo, en parte porque las células tumorales se vuelven extraordinariamente hábiles para sobrevivir en nichos de bajo oxígeno, o hipoxia, dentro de la pared del estómago. Muchos fármacos nuevos intentan matar las células cancerosas desencadenando una forma de muerte dependiente del hierro llamada ferroptosis. Este estudio plantea una pregunta crucial para futuros pacientes: ¿cómo eluden los tumores gástricos hipóxicos esta muerte dependiente del hierro, y se puede bloquear esa vía de escape?
Una línea de rescate oculta dentro de tumores con poco oxígeno
Usando grandes conjuntos de datos de secuenciación de ARN unicelular del tejido gástrico humano, los investigadores mapearon la actividad génica célula por célula a lo largo de la progresión desde el epitelio normal hasta el cáncer gástrico avanzado. Encontraron que las células epiteliales malignas activan una proteína secretada llamada factor de crecimiento derivado de mieloides (MYDGF) con mucha más intensidad que las células sanas cercanas. Estas células cancerosas con alto nivel de MYDGF también mostraron marcadores fuertes de sistemas de manejo y eliminación de proteínas en el retículo endoplásmico, lo que sugiere que MYDGF podría estar ligado a cómo las células tumorales regulan la vida y la muerte de proteínas clave.
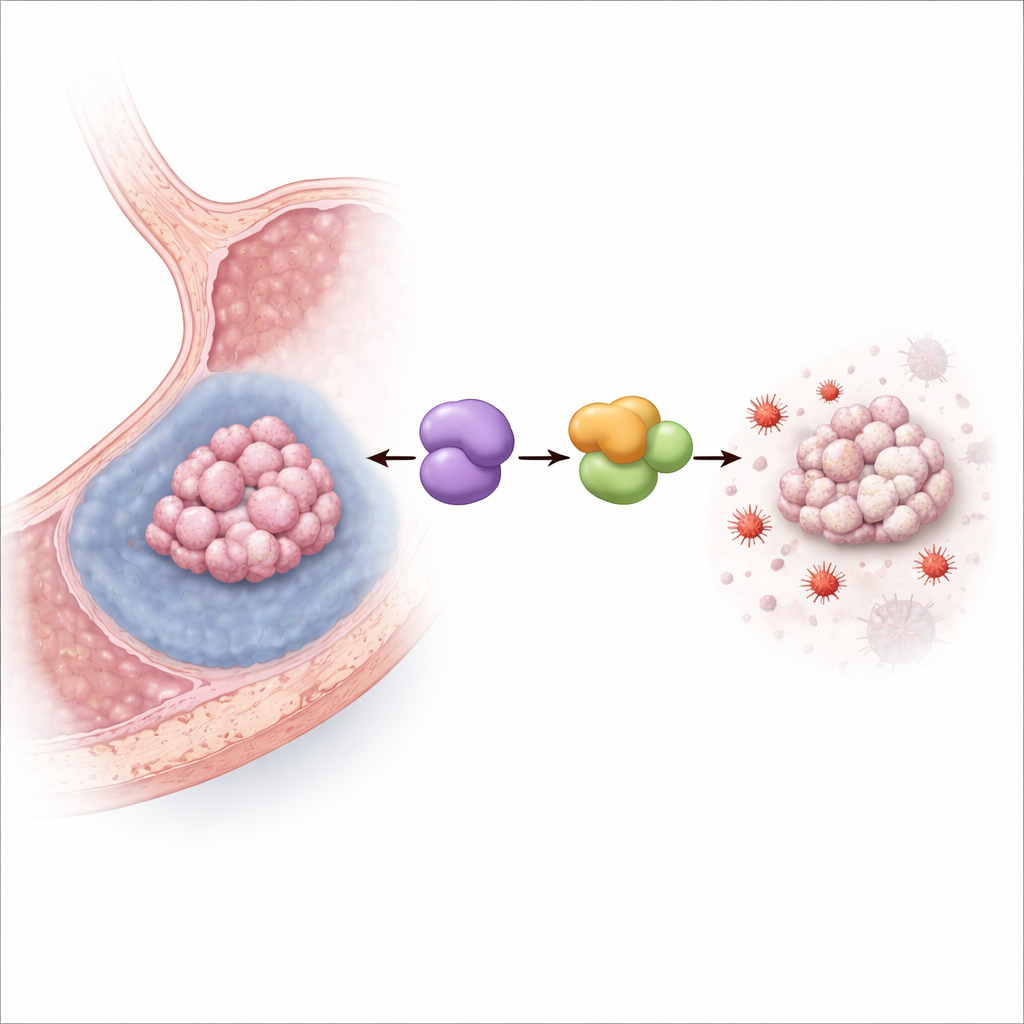
Apagar la muerte celular impulsada por el hierro
El equipo cultivó entonces células humanas de cáncer gástrico en condiciones hipóxicas que imitan el interior carente de nutrientes de los tumores sólidos. El bajo oxígeno aumentó los niveles de MYDGF y, como era de esperar, redujo la supervivencia celular. Cuando MYDGF se redujo experimentalmente, la hipoxia resultó mucho más letal, especialmente mediante ferroptosis: aumentaron los marcadores de daño lipídico y estrés oxidativo impulsado por hierro, las mitocondrias adoptaron una apariencia dañada y replegada, y un potente inhibidor de la ferroptosis rescató en gran medida a las células. En ratones con implantes de cáncer gástrico, aumentar MYDGF redujo el efecto reductor del tumor de un fármaco que induce ferroptosis, mientras que bloquear una proteína compañera llamada LCN2 tuvo el efecto contrario, confirmando que esta vía opera en tumores vivos.
Cómo las células cancerosas protegen a su guardián que une hierro
Indagando más, los autores identificaron a LCN2, una proteína que une hierro, como el actor crítico aguas abajo. Bajo hipoxia, los niveles proteicos de LCN2 cayeron aunque la actividad de su gen no lo hizo, lo que apunta a una destrucción activa más que a una reducción de la producción. Mostraron que LCN2 normalmente se marca con ubiquitina y se introduce en la trituradora proteica de la célula, el proteasoma, a través de una ruta de control de calidad del retículo endoplásmico conocida como degradación asociada al retículo endoplásmico (ERAD). Un adaptador de transporte llamado UBQLN1 entrega la LCN2 ubiquitinada a esta maquinaria de degradación. MYDGF actúa como guardaespaldas: se une a UBQLN1 en un dominio de acoplamiento específico, desplazando a LCN2 e impidiendo su entrega al proteasoma. Como resultado, la proteína LCN2 se estabiliza, sigue captando hierro reactivo y atenúa la peroxidación lipídica que impulsa la ferroptosis.
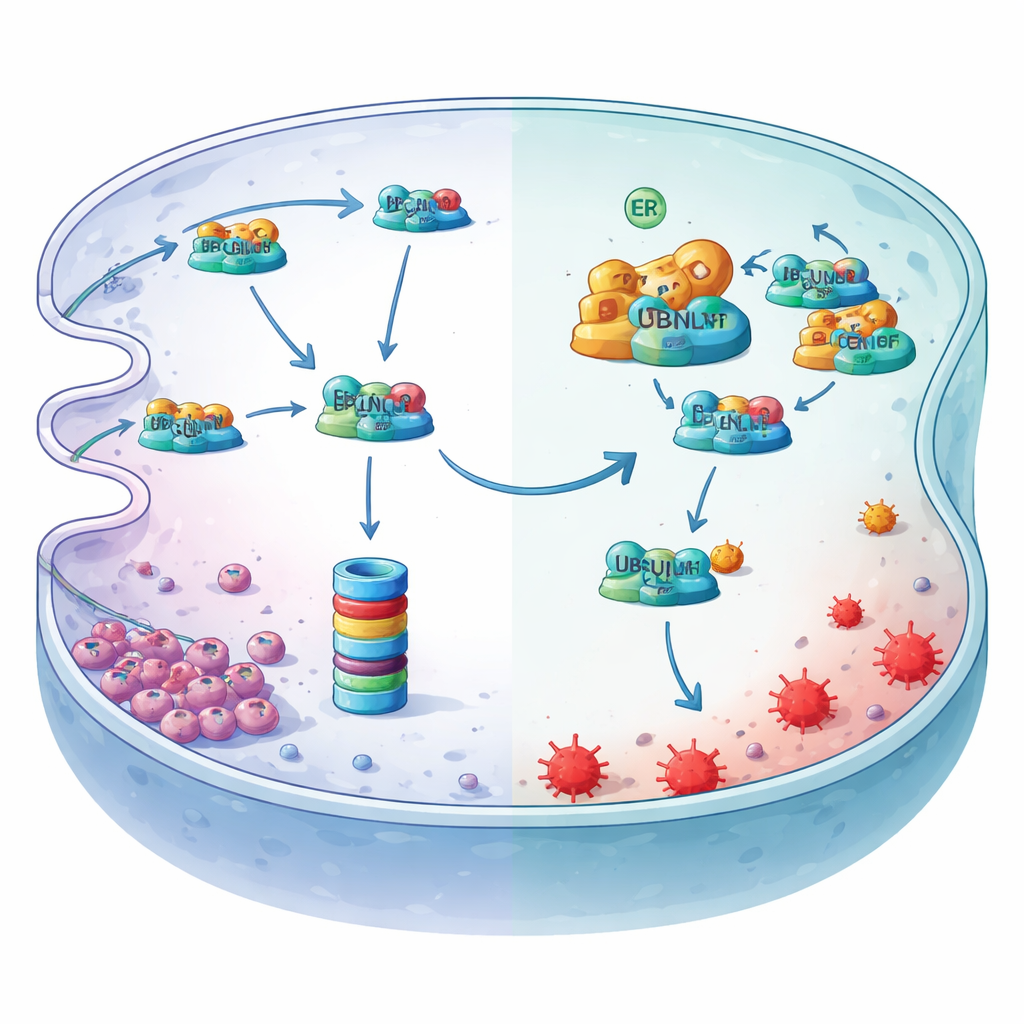
La hipoxia activa el interruptor maestro aguas arriba
El estudio también revela cómo la hipoxia pone en marcha este eje protector. El bajo oxígeno estresa el retículo endoplásmico y activa una forma empalmada de un factor de transcripción llamado XBP1s. Mediante el análisis de la región reguladora del gen MYDGF y utilizando ensayos de unión a la cromatina y de reportero, los investigadores mostraron que XBP1s se acopla en un sitio específico y aumenta directamente la producción de MYDGF. Cuando XBP1s se redujo, los niveles de MYDGF descendieron, los de LCN2 disminuyeron y aumentaron los marcadores de ferroptosis —efectos que pudieron revertirse restaurando MYDGF o LCN2. En conjunto, estos experimentos describen una salvaguardia lineal: la hipoxia activa XBP1s, que aumenta MYDGF, que bloquea la destrucción de LCN2 mediada por UBQLN1, y esta LCN2 secuestra hierro y protege así a las células del cáncer gástrico contra la ferroptosis.
Nuevas formas de acorralar tumores gástricos obstinados
Para el público general, la conclusión es que los tumores gástricos hipóxicos han construido una "línea de emergencia" interna que mantiene con vida a una proteína protectora que une hierro el tiempo suficiente para evitar una prometedora forma nueva de muerte celular. Al trazar en detalle esta cadena XBP1s–MYDGF–UBQLN1–LCN2, el trabajo explica por qué algunas regiones tumorales pueden resistir las terapias basadas en ferroptosis y apunta a estrategias concretas para desarmar esa defensa —como bloquear MYDGF, XBP1s o las superficies de interacción en UBQLN1. Si tales intervenciones pueden traducirse con seguridad a pacientes, podrían ayudar a que los fármacos inductores de ferroptosis funcionen mejor en las partes más resistentes al tratamiento y con falta de oxígeno de los cánceres gástricos.
Cita: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Palabras clave: cáncer gástrico, hipoxia, ferroptosis, degradación de proteínas, metabolismo del hierro