Clear Sky Science · pl
Oś XBP1s–MYDGF indukowana niedotlenieniem hamuje ferroptozę poprzez stabilizację LCN2 zależną od UBQLN1 w raku żołądka
Dlaczego odcinanie guzów od żelaza ma znaczenie
Rak żołądka należy do najbardziej śmiertelnych nowotworów na świecie, częściowo dlatego, że komórki nowotworowe potrafią wyjątkowo dobrze przetrwać w obszarach o niskiej zawartości tlenu, czyli w warunkach niedotlenienia, głęboko w ścianie żołądka. Wiele nowych leków celuje w zabicie komórek nowotworowych przez wywołanie formy śmierci zależnej od żelaza zwanej ferroptozą. W badaniu zadano kluczowe pytanie dla przyszłych pacjentów: jak niedotlenione guzy żołądka unikają tej żelazozależnej śmierci i czy tę drogę ucieczki można zablokować?
Ukryta linia ratunkowa w guzach pozbawionych tlenu
Wykorzystując obszerne zbiory danych z pojedynczokomórkowego RNA-seq z ludzkiej tkanki żołądka, badacze mapowali aktywność genów komórka po komórce w przebiegu od normalnego nabłonka do pełnoobjawowego raka żołądka. Stwierdzili, że komórki nabłonkowe nowotworu silnie uruchamiają wydzielane białko zwane czynnikiem wzrostu pochodzenia mieloidalnego (MYDGF) znacznie silniej niż pobliskie zdrowe komórki. Komórki nowotworowe o wysokim poziomie MYDGF wykazywały też wyraźne sygnatury systemów obsługi i utylizacji białek w obrębie retikulum endoplazmatycznego, co sugeruje, że MYDGF może być powiązany z tym, jak komórki guza zarządzają losami kluczowych białek.
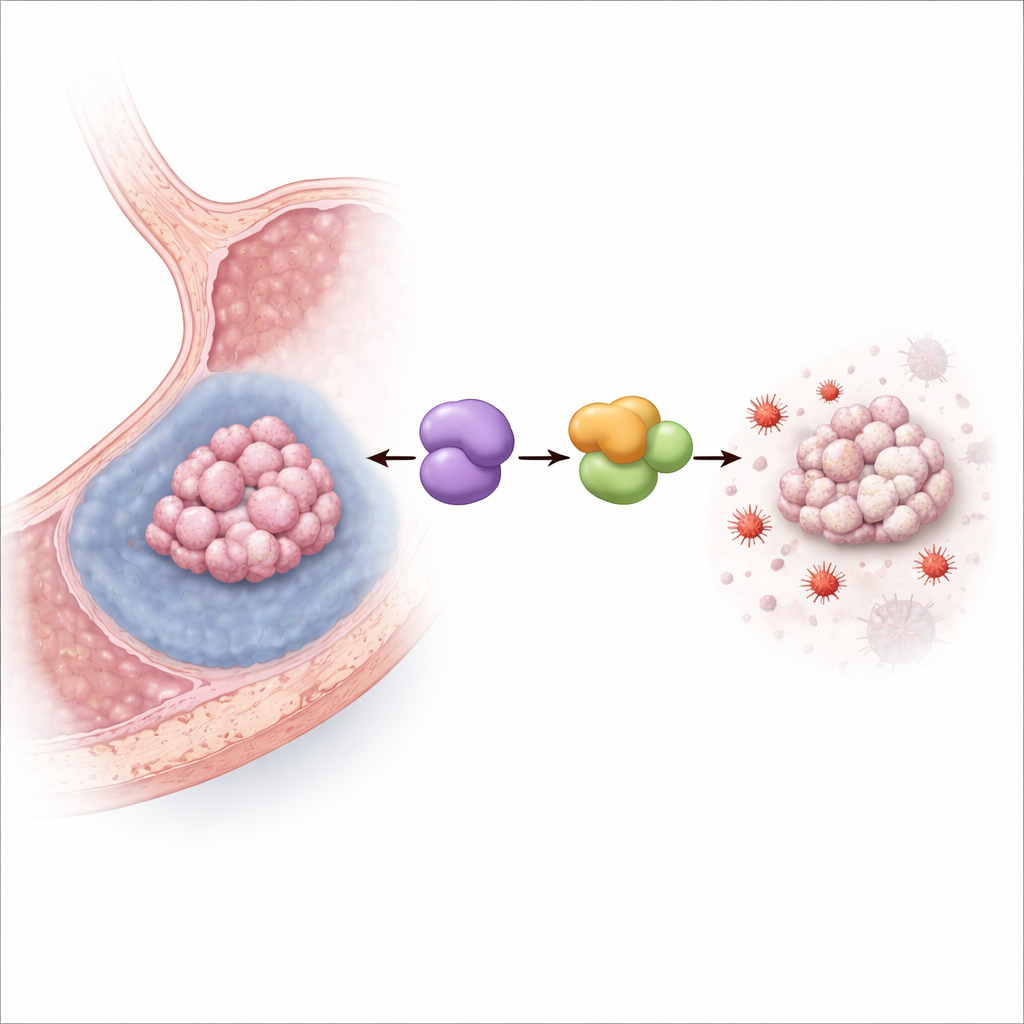
Wyłączanie żelazozależnej śmierci komórkowej
Zespół następnie hodował ludzkie komórki raka żołądka w warunkach niedotlenienia naśladujących wynędzniały środek guzów litych. Niski poziom tlenu podniósł poziomy MYDGF i, jak oczekiwano, obniżył przeżywalność komórek. Gdy MYDGF został eksperymentalnie zmniejszony, niedotlenienie stało się znacznie bardziej śmiertelne, szczególnie w przebiegu ferroptozy: wzrosły markery uszkodzeń lipidów i stresu oksydacyjnego zależnego od żelaza, mitochondria przybrały uszkodzony, skurczony wygląd, a silny inhibitor ferroptozy w dużej mierze uratował komórki. U myszy z wszczepami raka żołądka zwiększenie MYDGF osłabiło efekt kurczenia się guza wywołany lekiem indukującym ferroptozę, natomiast zablokowanie białka-partnera LCN2 miało efekt przeciwny, potwierdzając, że ta ścieżka działa również w żywych guzach.
Jak komórki nowotworowe osłaniają swojego strażnika wiążącego żelazo
Pogłębiając analizę, autorzy zidentyfikowali LCN2, białko wiążące żelazo, jako krytycznego gracza docelowego. Pod niedotlenieniem poziomy białka LCN2 malały, mimo że aktywność jego genu się nie zmieniała, co wskazuje na aktywne niszczenie, a nie zmniejszoną produkcję. Wykazali, że LCN2 jest normalnie znakowany ubikwityną i kierowany do komórkowego rozdrabniacza białek — proteasomu — przez szlak kontroli jakości retikulum endoplazmatycznego znany jako ER‑associated degradation. Adapter transportowy o nazwie UBQLN1 dostarcza ubikwitynowane LCN2 do tego układu degradacji. MYDGF wchodzi jako ochroniarz: wiąże się z UBQLN1 w określonym miejscu dokowania, wypierając LCN2 i uniemożliwiając jego przekazanie do proteasomu. W rezultacie białko LCN2 zostaje ustabilizowane, nadal wiąże żelazo reaktywne i tłumi peroksydację lipidów napędzającą ferroptozę.
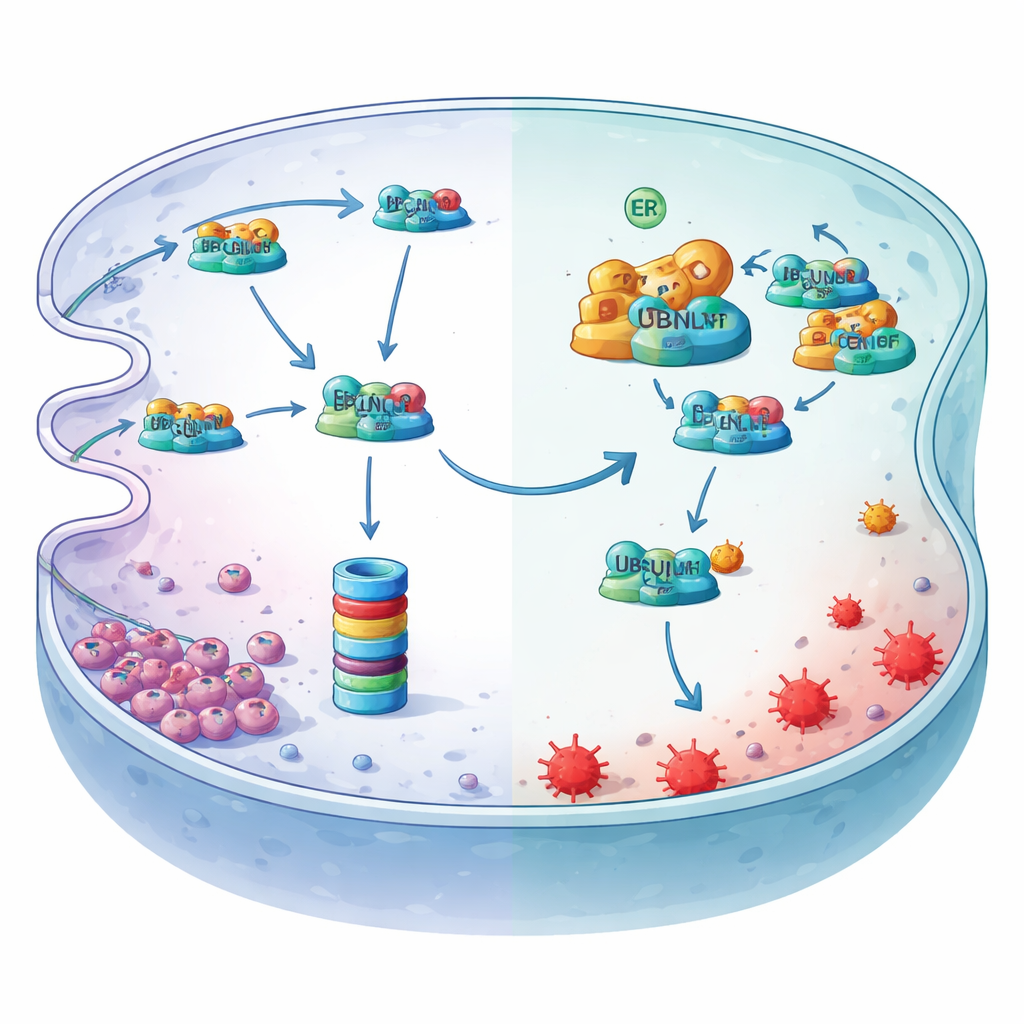
Niedotlenienie przełącza główny wyłącznik powyżej
Badanie pokazuje też, jak niedotlenienie włącza tę ochronną oś. Niski poziom tlenu obciąża retikulum endoplazmatyczne i aktywuje spliced formę czynnika transkrypcyjnego zwaną XBP1s. Skanując region kontrolny genu MYDGF i stosując testy wiązania chromatyny oraz assay reporterowe, badacze wykazali, że XBP1s osadza się w konkretnym miejscu i bezpośrednio zwiększa produkcję MYDGF. Gdy XBP1s został zmniejszony, spadły poziomy MYDGF, zmalały poziomy LCN2, a markery ferroptozy wzrosły — efekty, które można było cofnąć przez przywrócenie MYDGF lub LCN2. Razem te eksperymenty wskazują na liniowy mechanizm ochronny: niedotlenienie aktywuje XBP1s, co zwiększa MYDGF, który blokuje UBQLN1‑zależne niszczenie LCN2, a LCN2 następnie pochłania żelazo i chroni komórki raka żołądka przed ferroptozą.
Nowe sposoby na okrążenie opornych guzów żołądka
Dla czytelników niebędących ekspertami wniosek jest taki, że niedotlenione guzy żołądka zbudowały wewnętrzną „linię alarmową”, która utrzymuje przy życiu białko‑opiekuna wiążącego żelazo wystarczająco długo, by uniknąć obiecującej nowej formy śmierci komórkowej. Opisując szczegółowo łańcuch XBP1s–MYDGF–UBQLN1–LCN2, praca wyjaśnia, dlaczego niektóre regiony guza mogą być oporne na terapie oparte na ferroptozie i wskazuje konkretne strategie neutralizacji tej obrony — na przykład blokowanie MYDGF, XBP1s lub powierzchni interakcji na UBQLN1. Jeśli takie interwencje da się bezpiecznie przetłumaczyć na leczenie pacjentów, mogą poprawić skuteczność przyszłych leków indukujących ferroptozę w najbardziej opornych, pozbawionych tlenu partiach raków żołądka.
Cytowanie: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Słowa kluczowe: rak żołądka, niedotlenienie, ferroptoza, degradacja białek, metabolizm żelaza