Clear Sky Science · it
L’asse XBP1s–MYDGF indotto dall’ipossia sopprime la ferroptosi tramite la stabilizzazione di LCN2 mediata da UBQLN1 nel carcinoma gastrico
Perché privare i tumori del ferro è importante
Il carcinoma gastrico è uno dei tumori più letali al mondo, in parte perché le cellule tumorali diventano straordinariamente abili a sopravvivere in nicchie a basso contenuto di ossigeno, o ipossiche, profonde nella parete gastrica. Molti farmaci di nuova generazione mirano a uccidere le cellule tumorali inducendo una forma di morte cellulare guidata dal ferro chiamata ferroptosi. Questo studio pone una domanda cruciale per i pazienti futuri: come fanno i tumori gastrici ipossici a eludere questa morte dipendente dal ferro, e si può bloccare questa via di fuga?
Una linea di salvataggio nascosta all’interno dei tumori poveri di ossigeno
Usando ampi dataset di sequenziamento dell’RNA a singola cellula da tessuto gastrico umano, i ricercatori hanno mappato l’attività genica cellula per cellula lungo la progressione dalla mucosa normale al carcinoma gastrico invasivo. Hanno scoperto che le cellule epiteliali maligne attivano una proteina secreta chiamata fattore di crescita derivato dai mieloidi (MYDGF) molto più intensamente delle cellule sane circostanti. Queste cellule tumorali ad alta espressione di MYDGF mostravano anche forti firme dei sistemi di gestione e smaltimento delle proteine all’interno del reticolo endoplasmatico, suggerendo che MYDGF potrebbe essere collegato al modo in cui le cellule tumorali regolano la vita e la morte di proteine chiave.
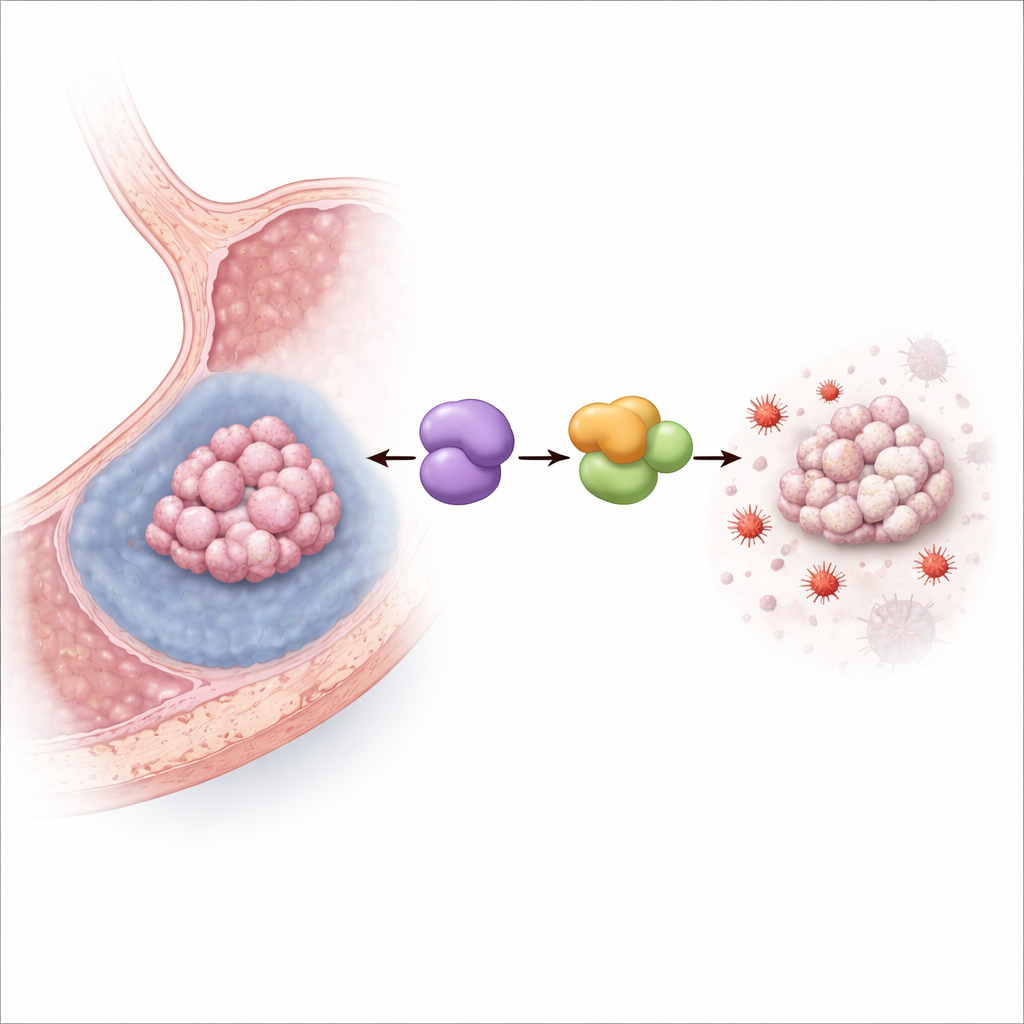
Spegnere la morte cellulare guidata dal ferro
Il gruppo ha quindi coltivato cellule di carcinoma gastrico umano in condizioni ipossiche che imitano l’interno affamato di ossigeno dei tumori solidi. Il basso ossigeno ha aumentato i livelli di MYDGF e, come previsto, ha ridotto la sopravvivenza cellulare. Quando MYDGF è stato sperimentalmente ridotto, l’ipossia è diventata molto più letale, soprattutto attraverso la ferroptosi: sono aumentati i marcatori di danno lipidico e stress ossidativo indotto dal ferro, i mitocondri hanno assunto un aspetto danneggiato e rimpicciolito, e un potente inibitore della ferroptosi ha in gran parte salvato le cellule. In topi portatori di innesti di carcinoma gastrico, aumentare MYDGF ha ridotto l’effetto di riduzione tumorale di un farmaco che induce ferroptosi, mentre bloccare una proteina partner chiamata LCN2 ha prodotto l’effetto opposto, confermando che questa via opera nei tumori viventi.
Come le cellule tumorali proteggono il loro guardiano legante il ferro
Approfondendo, gli autori hanno identificato LCN2, una proteina che lega il ferro, come il componente a valle critico. In condizioni di ipossia, i livelli proteici di LCN2 sono diminuiti nonostante l’attività genica non fosse ridotta, indicando una distruzione attiva piuttosto che una minore produzione. Hanno dimostrato che LCN2 è normalmente etichettata con ubiquitina e indirizzata allo sminuzzatore proteico della cellula, il proteasoma, tramite una via di controllo qualità del reticolo endoplasmatico nota come degradazione associata al reticolo endoplasmatico (ER‑associated degradation). Un adattatore di trasporto chiamato UBQLN1 consegna LCN2 ubiquitinata a questa macchina di degradazione. MYDGF entra in scena come una guardia del corpo: si lega a UBQLN1 in un dominio di ancoraggio specifico, escludendo LCN2 e impedendone la consegna al proteasoma. Di conseguenza, la proteina LCN2 viene stabilizzata, continua a legare il ferro reattivo e attenua la perossidazione lipidica che guida la ferroptosi.
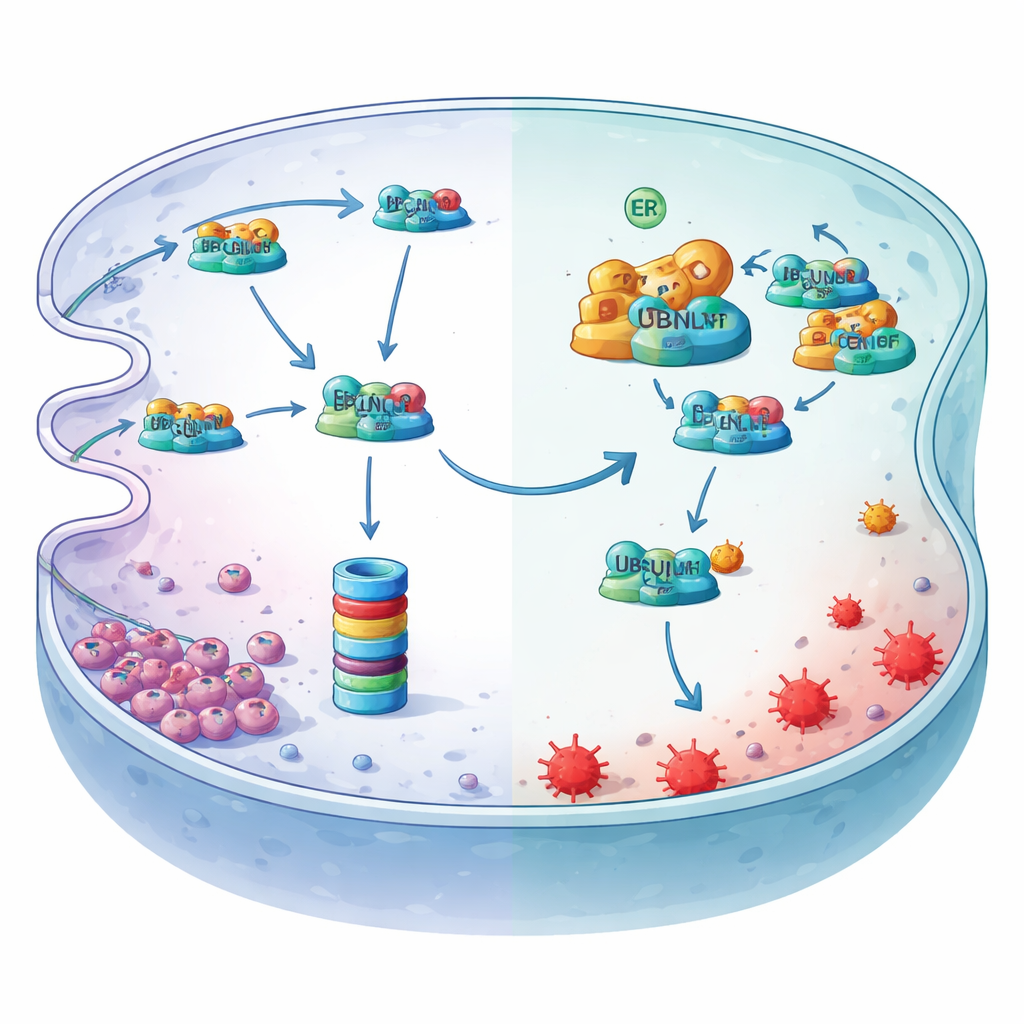
L’ipossia attiva l’interruttore maestro a monte
Lo studio rivela anche come l’ipossia attivi questo asse protettivo. Il basso ossigeno stressa il reticolo endoplasmatico e attiva una forma splicing di un fattore di trascrizione chiamato XBP1s. Scansionando la regione di controllo del gene MYDGF e usando saggi di legame alla cromatina e reporter, i ricercatori hanno mostrato che XBP1s si lega in un sito specifico e incrementa direttamente la produzione di MYDGF. Quando XBP1s è stato ridotto, i livelli di MYDGF sono diminuiti, i livelli di LCN2 sono scesi e i marcatori di ferroptosi sono aumentati—effetti che potevano essere annullati ripristinando MYDGF o LCN2. Complessivamente, questi esperimenti delineano un meccanismo lineare di salvaguardia: l’ipossia attiva XBP1s, che aumenta MYDGF, il quale blocca la distruzione di LCN2 mediata da UBQLN1, permettendo a LCN2 di sequestrare il ferro e proteggere le cellule del carcinoma gastrico dalla ferroptosi.
Nuove strategie per accerchiare i tumori gastrici ostinati
Per i non specialisti, la conclusione è che i tumori gastrici ipossici hanno costruito una "linea d’emergenza" interna che mantiene viva una proteina protettrice legante il ferro abbastanza a lungo da evitare una promettente nuova forma di morte cellulare. Mappando in dettaglio questa catena XBP1s–MYDGF–UBQLN1–LCN2, il lavoro spiega perché alcune regioni tumorali possono resistere alle terapie basate sulla ferroptosi e indica strategie concrete per disarmare questa difesa—come bloccare MYDGF, XBP1s o le superfici di interazione su UBQLN1. Se tali interventi potranno essere tradotti in modo sicuro nei pazienti, potrebbero rendere più efficaci i futuri farmaci che inducono la ferroptosi nelle zone più resistenti al trattamento e povere di ossigeno dei carcinomi gastrici.
Citazione: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Parole chiave: carcinoma gastrico, ipossia, ferroptosi, degradazione proteica, metabolismo del ferro