Clear Sky Science · de
Hypoxie‑induziierte XBP1s‑MYDGF‑Achse unterdrückt Ferroptose durch UBQLN1‑vermittelte Stabilisierung von LCN2 beim Magenkrebs
Warum es wichtig ist, Tumoren Eisen zu entziehen
Magenkrebs gehört zu den weltweit tödlichsten Krebsarten, zum Teil weil Tumorzellen erstaunlich gut darin sind, in sauerstoffarmen, also hypoxischen, Nischen tief in der Magenwand zu überleben. Viele neue Medikamente zielen darauf ab, Krebszellen durch eine Form des eisenabhängigen Zelltods namens Ferroptose zu töten. Diese Studie stellt eine entscheidende Frage für künftige Patientinnen und Patienten: Wie entziehen sich hypoxische Magentumoren diesem eisenabhängigen Tod und lässt sich dieser Fluchtweg blockieren?
Eine verborgene Rettungsleine in sauerstoffarmen Tumoren
Anhand großer Einzelzell‑RNA‑Sequenzierungsdatensätze aus menschlichem Magengewebe kartierten die Forschenden die Genaktivität Zelle für Zelle entlang der Entwicklung vom normalen Epithel bis zum ausgereiften Magenkrebs. Sie fanden heraus, dass maligne Epithelzellen ein sekretorisches Protein namens myeloid‑derived growth factor (MYDGF) deutlich stärker hochfahren als benachbarte gesunde Zellen. Diese MYDGF‑reichen Krebszellen zeigten zudem starke Signaturen von Proteinfaltungs‑ und Entsorgungssystemen im endoplasmatischen Retikulum, was darauf hindeutet, dass MYDGF mit der Art und Weise verknüpft sein könnte, wie Tumorzellen das Schicksal wichtiger Proteine regeln.
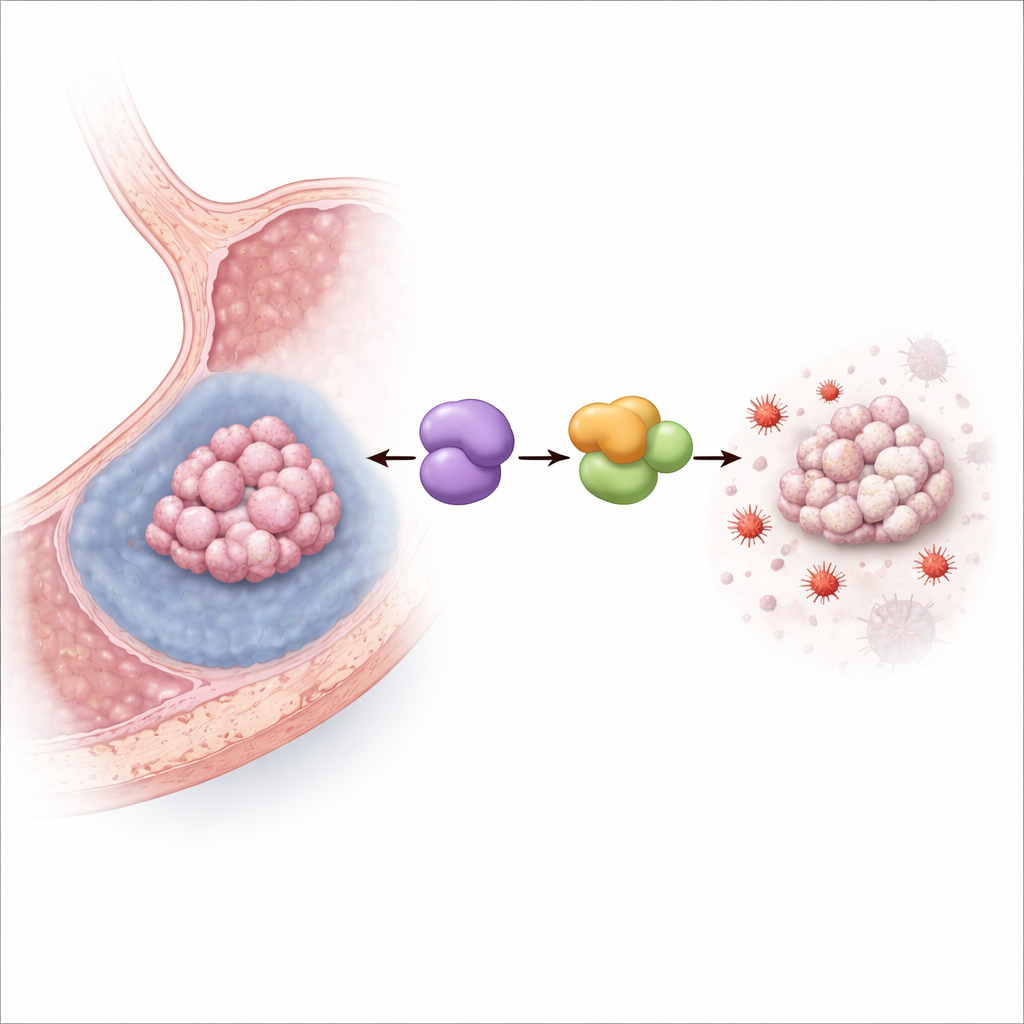
Den eisengetriebenen Zelltod abschalten
Im nächsten Schritt kultivierte das Team humane Magenkrebszellen unter hypoxischen Bedingungen, die das entbehrte Innere solider Tumoren nachahmen. Niedriger Sauerstoff erhöhte die MYDGF‑Spiegel und verringerte erwartungsgemäß die Zellüberlebensrate. Wurde MYDGF experimentell reduziert, wurde Hypoxie deutlich tödlicher, insbesondere durch Ferroptose: Marker für Lipidschäden und ironengetriebenen oxidativen Stress stiegen an, die Mitochondrien zeigten ein geschädigtes, geschrumpftes Erscheinungsbild, und ein wirksamer Ferroptose‑Inhibitor rettete die Zellen weitgehend. In Mäusen mit Magenkrebs‑Transplantaten verringerte eine Erhöhung von MYDGF die Tumorverkleinerungseffekte eines ferroptoseauslösenden Wirkstoffs, während die Blockade eines Partnerproteins namens LCN2 den gegenteiligen Effekt hatte — ein Befund, der bestätigt, dass dieser Signalweg auch in lebenden Tumoren aktiv ist.
Wie Krebszellen ihren eisenbindenden Schutzschild bewahren
Tiefer gehende Analysen identifizierten LCN2, ein eisenbindendes Protein, als den kritischen downstream‑Akteur. Unter Hypoxie sanken die LCN2‑Proteinspiegel, obwohl die Genaktivität unverändert blieb, was auf aktive Zerstörung statt verminderter Produktion hindeutet. Die Autoren zeigten, dass LCN2 normalerweise mit Ubiquitin markiert und über einen endoplasmatisch‑retikulären Qualitätskontrollweg (ER‑associated degradation) an das Proteasom zur Abbaumaschinerie übergeben wird. Ein Transportadapter namens UBQLN1 liefert ubiquitinylierte LCN2 an diese Abbauvorrichtung. MYDGF tritt als Bodyguard auf: Es bindet an UBQLN1 an einer spezifischen Andockstelle, verdrängt dadurch LCN2 und verhindert dessen Übergabe an das Proteasom. In der Folge wird LCN2‑Protein stabilisiert, bindet weiterhin reaktives Eisen und dämpft die Lipidperoxidation, die die Ferroptose antreibt.
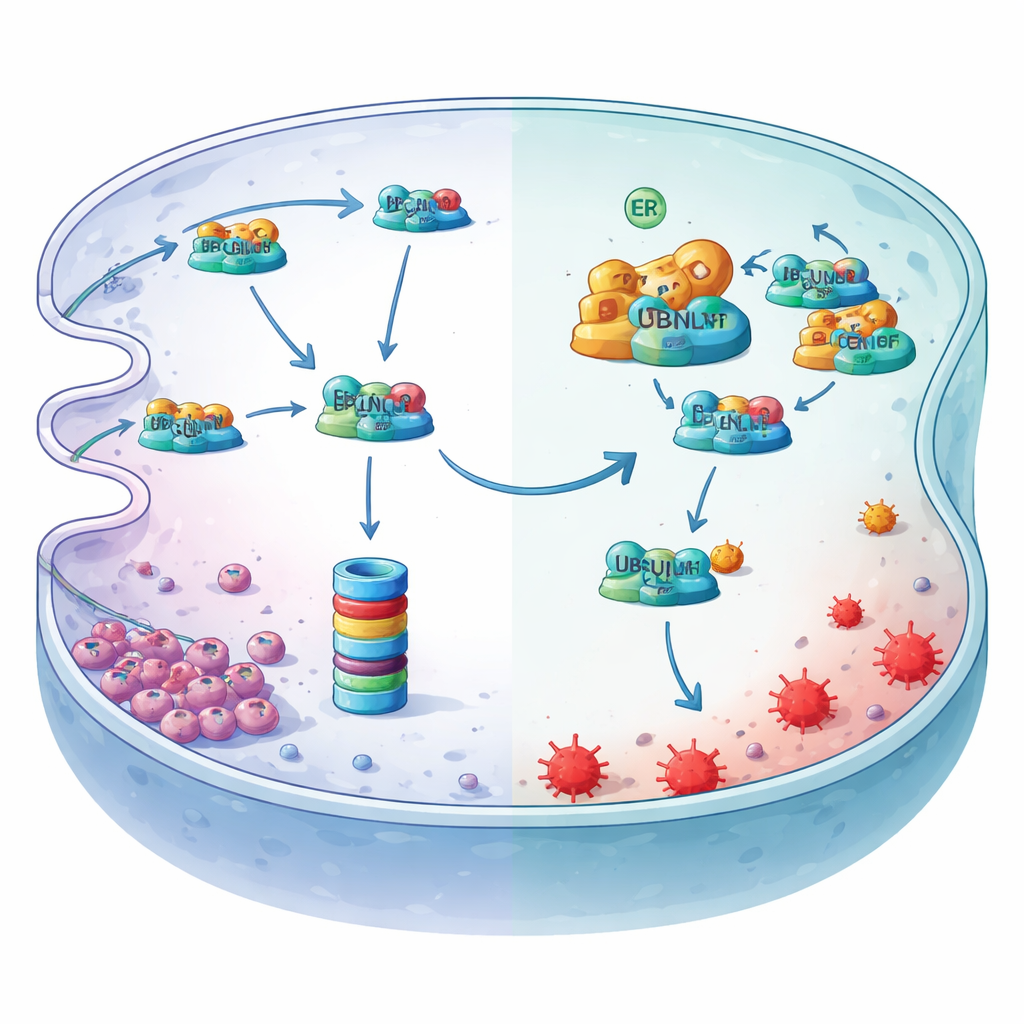
Hypoxie schaltet den Master‑Schalter stromaufwärts um
Die Studie zeigt außerdem, wie Hypoxie diese Schutzachse aktiviert. Niedriger Sauerstoff stresst das endoplasmatische Retikulum und aktiviert eine gespleißte Form eines Transkriptionsfaktors namens XBP1s. Durch Scannen der Kontrollregion des MYDGF‑Gens sowie mit Chromatinbindungs‑ und Reporterassays zeigten die Forschenden, dass XBP1s an einer spezifischen Stelle andockt und direkt die MYDGF‑Produktion hochfährt. Wenn XBP1s reduziert wurde, sanken MYDGF‑Spiegel, fielen LCN2‑Spiegel und stiegen Ferroptosemarker — Effekte, die durch Wiederherstellung von MYDGF oder LCN2 rückgängig gemacht werden konnten. Zusammen zeichnen diese Experimente eine lineare Schutzkette: Hypoxie aktiviert XBP1s, das MYDGF erhöht, das die UBQLN1‑vermittelte Zerstörung von LCN2 blockiert, woraufhin LCN2 Eisen aufnimmt und Magenkrebszellen vor Ferroptose schützt.
Neue Wege, hartnäckige Magentumoren in die Enge zu treiben
Für Nicht‑Experten lautet die Kernaussage: Hypoxische Magentumoren haben eine interne „Notfallleitung“ aufgebaut, die ein eisenbindendes Schutzprotein lange genug am Leben erhält, um einer vielversprechenden neuen Form des Zelltods zu entgehen. Indem die Studie die XBP1s–MYDGF–UBQLN1–LCN2‑Kette detailliert aufschlüsselt, erklärt sie, warum einige Tumorregionen gegenüber ferroptosebasierten Therapien resistent sein könnten, und weist auf konkrete Strategien hin, diese Abwehr zu entwaffnen — etwa durch Blockade von MYDGF, XBP1s oder der Interaktionsflächen an UBQLN1. Können solche Interventionen sicher auf Patientinnen und Patienten übertragen werden, könnten sie dazu beitragen, ferroptoseauslösende Medikamente in den am schwersten behandelbaren, sauerstoffarmen Bereichen von Magenkrebserkrankungen wirksamer zu machen.
Zitation: Zhou, Q., Qi, H., Zou, Y. et al. Hypoxia-induced XBP1s-MYDGF axis suppresses ferroptosis through UBQLN1-mediated stabilization of LCN2 in gastric cancer. Oncogene 45, 1786–1799 (2026). https://doi.org/10.1038/s41388-026-03760-6
Schlüsselwörter: Magenkrebs, Hypoxie, Ferroptose, Proteinabbau, Eisenstoffwechsel