Clear Sky Science · zh
抑制 PIAS4 可诱导细胞周期停滞并与 CDK4/6 抑制剂联用呈协同作用以治疗乳腺癌
这项研究对患者的重要性
乳腺癌是女性中最常见且致死率较高的癌症之一,许多患者最终对减缓肿瘤细胞分裂的标准药物产生耐药。该研究发现了癌细胞内一个先前被低估的助推蛋白 PIAS4,它在细胞进入生长周期的关键检查点时起推动作用。研究显示阻断 PIAS4 不仅减慢乳腺癌细胞增殖,还能增强现有一类药物的疗效,提示一种潜在的新型联合治疗策略,可能使肿瘤更长时间处于受控状态。
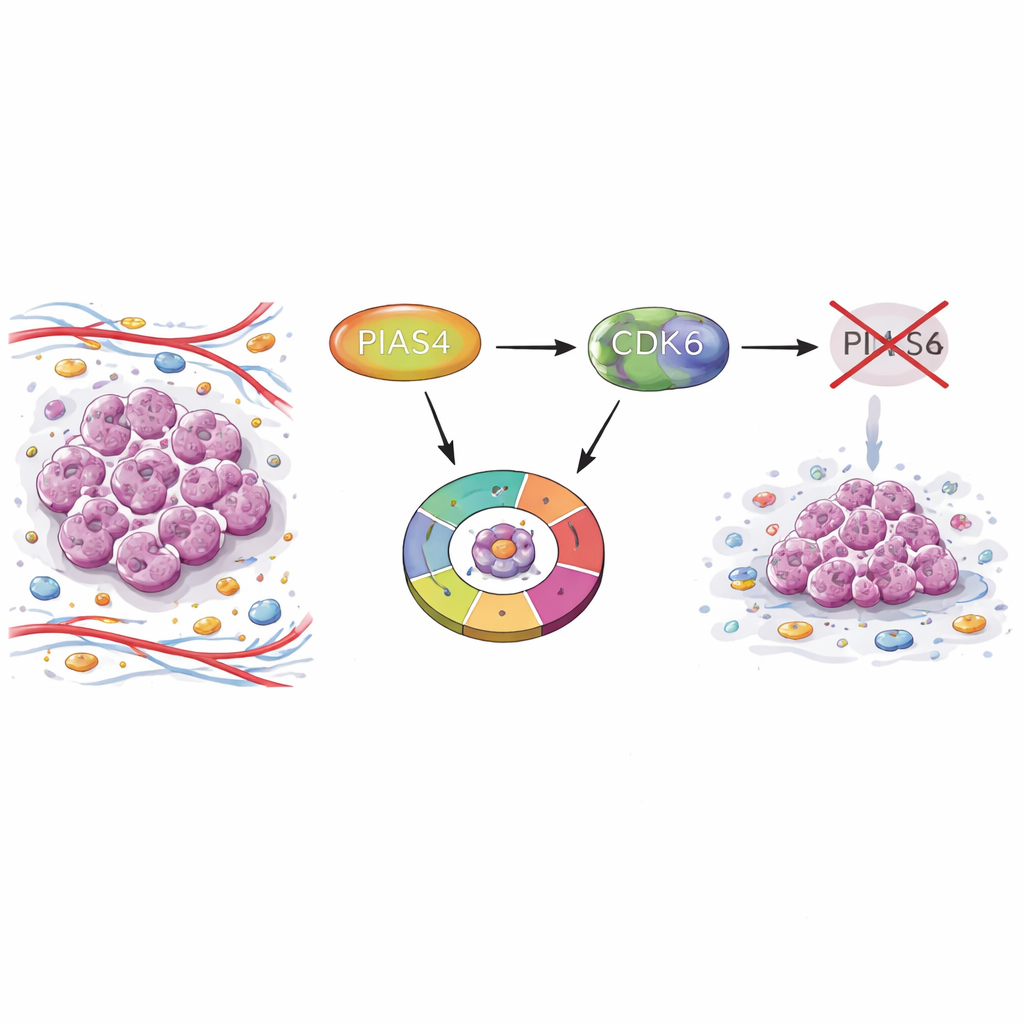
乳腺肿瘤中的隐性开关
研究人员首先利用大规模癌症数据库和患者组织微阵列比较肿瘤样本与正常乳腺组织。他们发现 PIAS4 在乳腺肿瘤中的表达持续高于健康组织。肿瘤中 PIAS4 表达较高的患者生存率更差,提示该蛋白与侵袭性疾病相关。值得注意的是,PIAS4 水平并未与常见诊断标志物(如雌激素受体、孕激素受体或 HER2)紧密相关,表明其作用可能横跨多种乳腺癌亚型。
PIAS4 如何帮助细胞加速通过周期
癌细胞通过反复经过一系列周期阶段来生长,其中早期的“G1”检查点决定细胞是否复制 DNA 并再次分裂。使用细胞培养模型,研究团队在乳腺癌细胞和小鼠细胞中下调 PIAS4。各系统中,降低 PIAS4 都减慢了细胞增殖并导致大量细胞停留在 G1 期,未能进入 DNA 复制阶段。研究者通过流式细胞术和 DNA 标记实验确认了这一停滞,结果显示在阻断 PIAS4 时进入复制期的细胞显著减少。
PIAS4、CDK6 与守门员 RB1 之间的协作
为探明机制,团队关注驱动 G1 检查点的分子机器,尤其是一种名为 CDK6 的蛋白激酶及其著名靶标肿瘤抑制蛋白 RB1。通常,活化的 CDK6 会向 RB1 添加磷酸基,使其失活,从而释放一组转录因子以开启 DNA 复制所需基因的表达。研究人员显示 PIAS4 在细胞核内与 CDK6 存在物理相互作用,并通过化学方式在 CDK6 上添加小型“SUMO”标记。这些标记增强了 CDK6 改变 RB1 的能力,并促进如 CDK1、E2F1、CCNE2 和 CCNA2 等细胞周期基因的表达。当 PIAS4 被抑制时,RB1 的磷酸化减少,RB1 的靶基因下调,细胞周期放慢。
对 CDK6 的细致调控:化学标记与结合伙伴
进一步研究中,团队绘制出 CDK6 接受 SUMO 标记的特定位点,并构建了无法被 SUMO 修饰的 CDK6 突变体。这些突变体在激活 RB1 和促使细胞通过 G1 期方面效果显著下降,证实 SUMO 修饰不仅是装饰性而是功能性的重要。与此同时,敲低 PIAS4 使 CDK6 更加稳定,但具有悖论性地活性降低:CDK6 上的抑制性磷酸标志增加,与其激活蛋白 cyclin D1 的结合减弱。生化测定显示,尽管低 PIAS4 的细胞中 CDK6 蛋白量更多,但其酶活性更低,强调了 CDK6 的修饰状态和结合伙伴比数量本身更为关键。
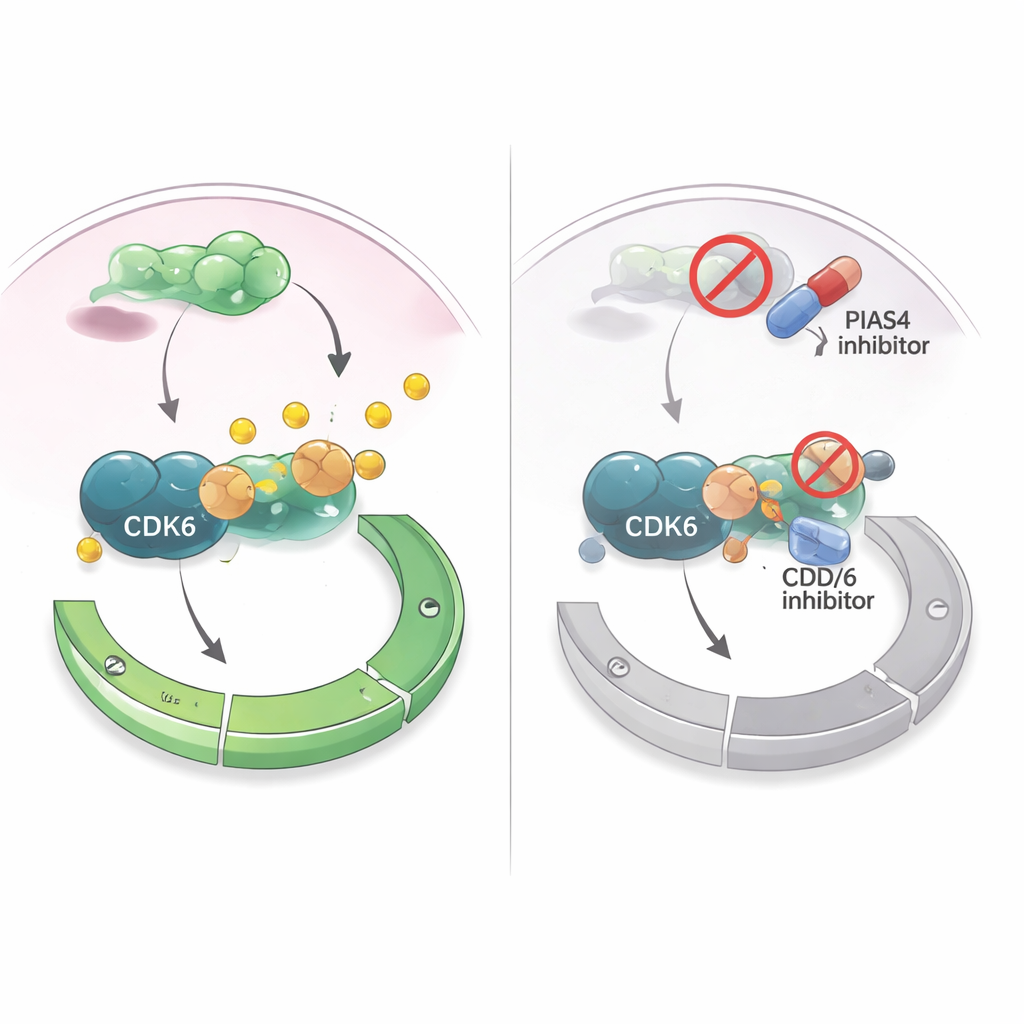
将弱点转化为治疗策略
由于抑制 CDK4/6 的药物已广泛用于激素受体阳性乳腺癌,作者探讨了靶向 PIAS4 是否能增强这些治疗。在培养的乳腺癌细胞中,一种广泛干扰 SUMO 标记(包括 PIAS4 活性)的药物使 CDK4/6 抑制剂在抑制细胞生长方面更为有效。在将乳腺癌细胞植入乳腺组织的小鼠模型中,同时降低 PIAS4 和 CDK6 比单独阻断 CDK6 更能使肿瘤缩小,且未见明显毒性。综合这些发现,研究表明 PIAS4 是 CDK6 和 G1 检查点的内部加速器,禁用这一加速器可使肿瘤对现有细胞周期药物更敏感。对患者而言,这意味着未来将 PIAS4 或 SUMO 通路抑制剂与 CDK4/6 抑制剂联合使用的疗法,可能更好地控制乳腺癌并延迟耐药的出现。
引用: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
关键词: 乳腺癌, 细胞周期, CDK4/6 抑制剂, SUMO 修饰, PIAS4