Clear Sky Science · ru
Ингибирование PIAS4 вызывает остановку клеточного цикла и проявляет синергический эффект в сочетании с ингибитором CDK4/6 при лечении рака молочной железы
Почему это исследование важно для пациентов
Рак молочной железы — одно из самых распространённых и смертельных злокачественных заболеваний у женщин, и у многих пациенток со временем прекращается ответ на стандартные препараты, замедляющие деление опухолевых клеток. В этом исследовании выявлен ранее недооценённый вспомогательный белок в опухолевых клетках — PIAS4, который незаметно продвигает клетки через ключевую контрольную точку их цикла роста. Показав, что блокирование PIAS4 не только замедляет клетки рака молочной железы, но и усиливает действие уже существующего класса препаратов, работа указывает на потенциальную новую комбинированную терапию, способную дольше удерживать опухоли под контролем.
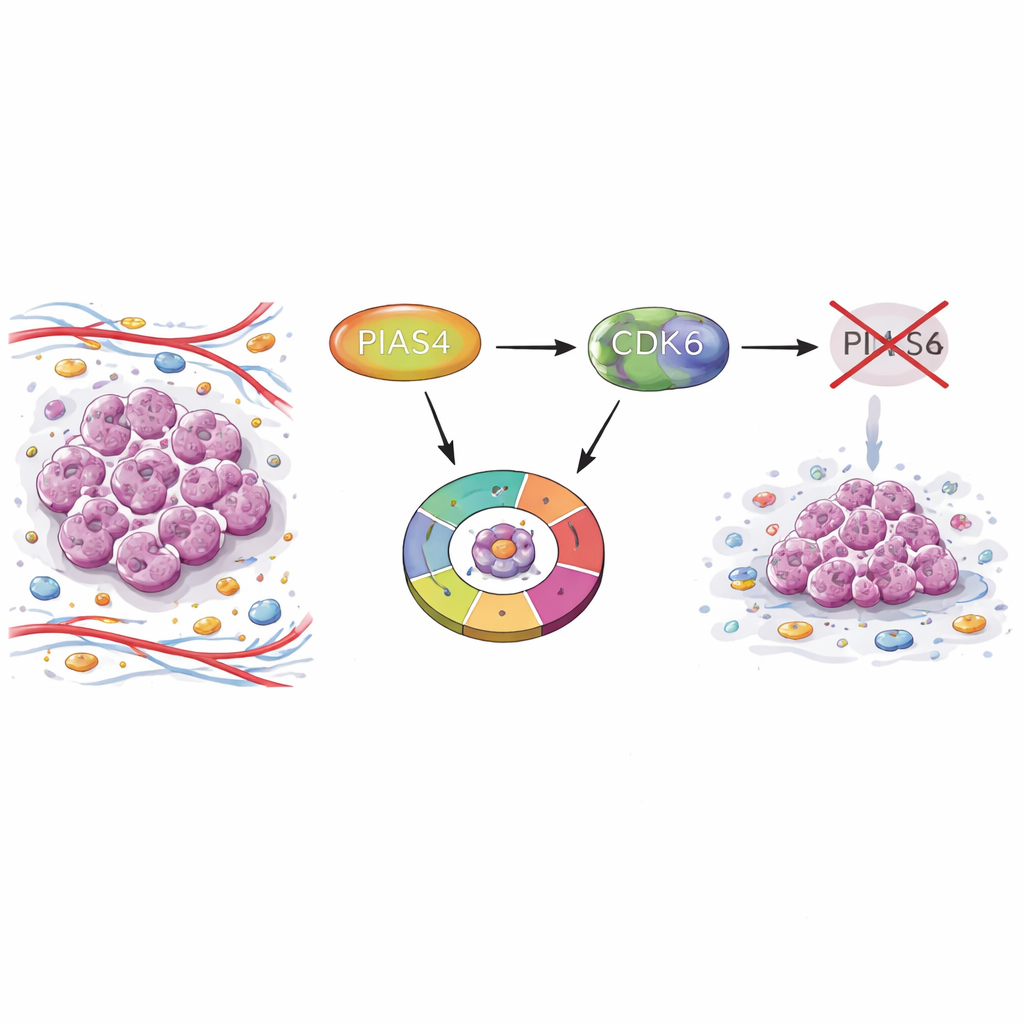
Скрытый переключатель в опухолях молочной железы
Исследователи начали с сопоставления образцов опухолей и нормальной ткани молочной железы, используя крупномасштабные онкологические базы данных и микрочипы тканей пациентов. Они обнаружили, что уровни PIAS4 последовательно выше в опухолях молочной железы, чем в здоровой ткани. У пациенток, чьи опухоли содержали больше PIAS4, выживаемость была ниже, что указывает на связь этого белка с агрессивным течением болезни. Важно, что уровни PIAS4 слабо коррелировали с типичными диагностическими маркерами, такими как рецепторы эстрогена, прогестерона или HER2, что говорит о том, что его роль может распространяться на несколько подтипов рака молочной железы.
Как PIAS4 помогает клеткам «проскочить» цикл
Раковые клетки растут, многократно проходя через цикл фаз, причём ранняя контрольная точка «G1» решает, будет ли клетка копировать ДНК и делиться дальше. В моделях культуры клеток команда понизила уровень PIAS4 в клетках рака молочной железы и в клетках мышей. В разных системах снижение PIAS4 замедляло рост клеток и приводило к накоплению большого числа клеток в фазе G1, которые не переходили к репликации ДНК. Учёные подтвердили эту остановку с помощью проточной цитометрии и тестов с маркировкой ДНК: при блокировании PIAS4 меньше клеток входило в фазу репликации.
Взаимодействие PIAS4, CDK6 и «строго охраняющего» RB1
Чтобы понять механизм, команда сосредоточилась на молекулярном оборудовании, управляющем контрольной точкой G1, особенно на киназе CDK6 и её известной мишени, опухолевом супрессоре RB1. Обычно активный CDK6 добавляет фосфатные группы к RB1, выключая его и освобождая семейство транскрипционных факторов для включения генов, необходимых для копирования ДНК. Исследователи показали, что PIAS4 физически ассоциируется с CDK6 в ядре и химически метит CDK6 маленькими «SUMO»-маркерами. Эти метки усиливают способность CDK6 модифицировать RB1 и стимулировать экспрессию генов клеточного цикла, таких как CDK1, E2F1, CCNE2 и CCNA2. При блокировании PIAS4 фосфорилирование RB1 снижалось, гены-мишени RB1 приглушались, и клеточный цикл замедлялся.
Тонкая настройка CDK6: химические метки и партнеры
Углубившись, команда нанесла на карту конкретные участки CDK6, получающие SUMO-метки, и создала мутантные формы CDK6, неспособные к SUMO-модификации. Эти мутанты были значительно менее эффективны в активации RB1 или продвижении клеток через G1, что подтверждает функциональную значимость SUMO-модификации. Одновременно с понижением PIAS4 стабильность CDK6 повышалась, но парадоксально его активность снижалась: увеличивалась ингибирующая фосфорная метка на CDK6, и ослабевало взаимодействие с активатором циклин D1. Биохимические анализы показали, что несмотря на большее количество белка CDK6, в клетках с низким уровнем PIAS4 активность киназы CDK6 была ниже, подчёркивая, что важнее не столько количество, сколько характер модификаций и партнёрские взаимодействия.
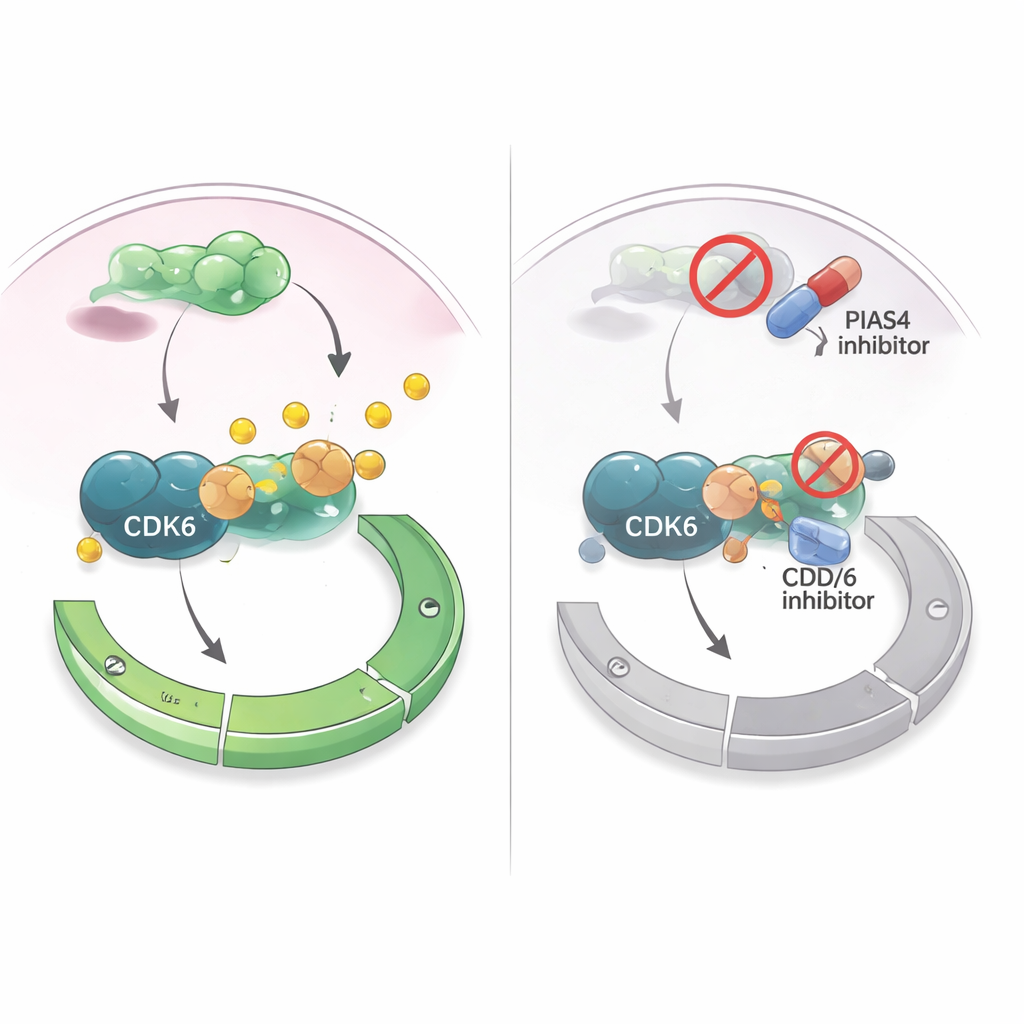
Преобразование уязвимости в терапевтическую стратегию
Поскольку ингибиторы CDK4/6 уже широко применяются при гормонально-рецептор–положительном раке молочной железы, авторы задали вопрос, не усилит ли нацеливание на PIAS4 эти препараты. В культурах клеток рака молочной железы препарат, который в целом мешает SUMO-маркировке (включая действия PIAS4), сделал ингибиторы CDK4/6 более эффективными в подавлении роста клеток. В моделях на мышах, куда имплантировали клетки рака молочной железы в молочную железу, одновременное снижение PIAS4 и CDK6 уменьшало опухоли сильнее, чем блокада только CDK6, без очевидного вреда для животных. Вместе эти результаты свидетельствуют о том, что PIAS4 функционирует как внутренний «акселератор» для CDK6 и контрольной точки G1, и что отключение этого акселератора может сделать опухоли более чувствительными к существующим препаратам, влияющим на клеточный цикл. Для пациентов это создаёт перспективу, что будущие терапии, комбинирующие ингибиторы PIAS4 или путей SUMO с ингибиторами CDK4/6, могут лучше контролировать рак молочной железы и отсрочить развитие резистентности.
Цитирование: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Ключевые слова: рак молочной железы, клеточный цикл, ингибиторы CDK4/6, SUMOилирование, PIAS4