Clear Sky Science · pl
Inhibicja PIAS4 wywołuje zatrzymanie cyklu komórkowego i wykazuje efekt synergiczny w połączeniu z inhibitorem CDK4/6 w leczeniu raka piersi
Dlaczego te badania są istotne dla pacjentów
Rak piersi jest jednym z najczęstszych i najgroźniejszych nowotworów u kobiet, a wielu pacjentek z czasem przestaje reagować na standardowe leki hamujące podziały komórek nowotworowych. W tej pracy zidentyfikowano dotąd niedoceniany białkowy „pomocnik” w komórkach nowotworowych, zwany PIAS4, który subtelnie popycha komórki przez kluczowy punkt kontrolny w cyklu wzrostu. Pokazując, że blokowanie PIAS4 nie tylko spowalnia komórki raka piersi, ale także zwiększa skuteczność istniejącej klasy leków, badanie wskazuje na potencjalną nową strategię łączoną, która mogłaby dłużej utrzymywać guzy pod kontrolą.
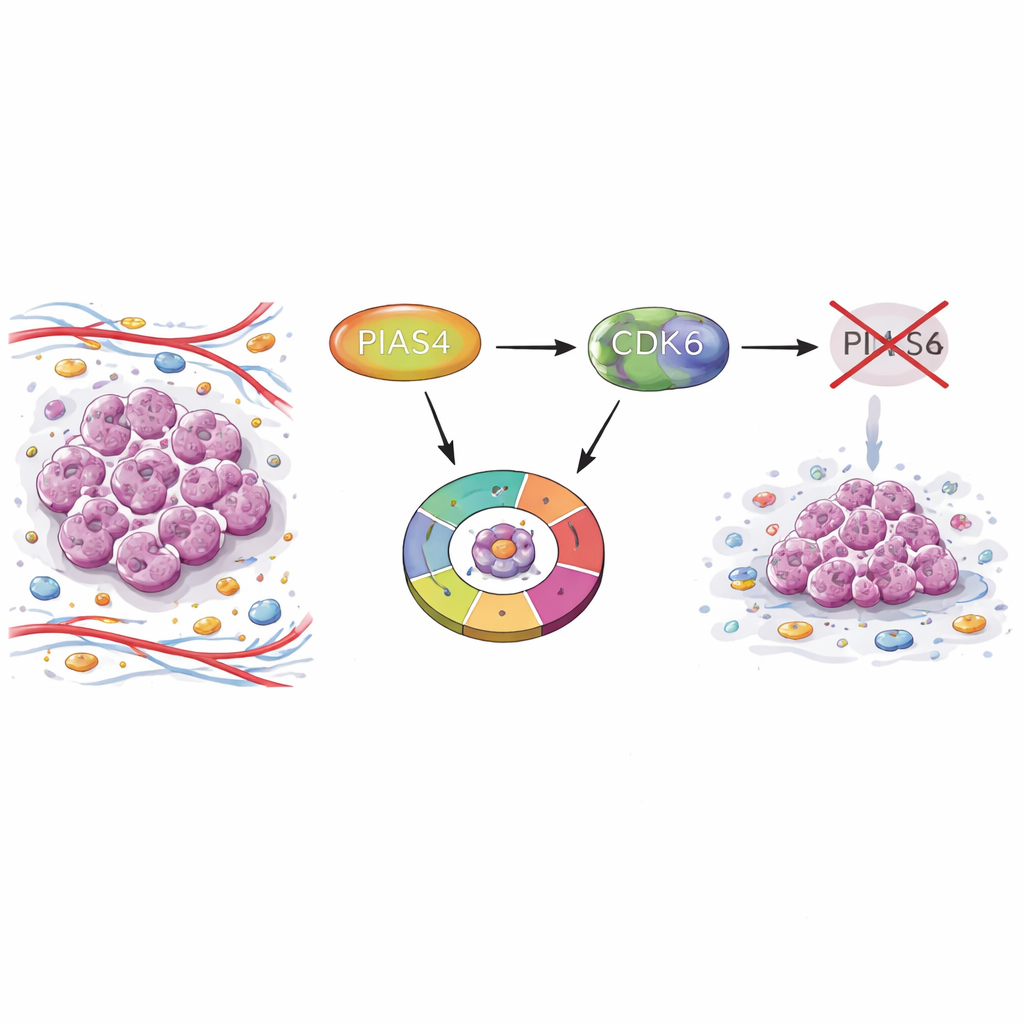
Ukryty przełącznik w guzach piersi
Naukowcy rozpoczęli od porównania próbek guzów z prawidłową tkanką piersi, korzystając z dużych baz danych nowotworowych i mikromacierzy tkanek pacjentek. Stwierdzili, że poziomy PIAS4 były konsekwentnie wyższe w guzach piersi niż w tkance zdrowej. Pacjentki, których guzy wytwarzały więcej PIAS4, miały gorsze przeżycie, co sugeruje związek tego białka z agresywnym przebiegiem choroby. Co ważne, poziomy PIAS4 nie korelowały silnie z powszechnymi markerami diagnostycznymi, takimi jak receptory estrogenowe, progesteronowe czy HER2, co wskazuje, że jego rola może obejmować kilka podtypów raka piersi.
Jak PIAS4 pomaga komórkom przechodzić przez cykl
Komórki nowotworowe proliferują przez wielokrotne przechodzenie cyklu fazowego, przy czym wczesny punkt kontrolny „G1” decyduje, czy komórka zduplikuje DNA i ponownie się podzieli. W modelach hodowlanych zespół obniżył poziom PIAS4 w komórkach raka piersi i w komórkach mysich. W różnych systemach zmniejszenie PIAS4 spowolniło wzrost komórek i spowodowało akumulację wielu komórek w fazie G1, które nie przechodziły do replikacji DNA. Naukowcy potwierdzili to zatrzymanie za pomocą cytometrii przepływowej i testów znakowania DNA, które wykazały mniej komórek wchodzących w fazę replikacji po zahamowaniu PIAS4.
Współpraca między PIAS4, CDK6 i strażnikiem RB1
Aby zrozumieć mechanizm, zespół skupił się na maszynerii molekularnej napędzającej punkt kontrolny G1, w szczególności na kinazie białkowej CDK6 i jej znanym celu, supresorze nowotworowym RB1. Normalnie aktywny CDK6 dodaje grupy fosforanowe do RB1, wyłączając go i uwalniając rodzinę czynników transkrypcyjnych do włączania genów potrzebnych do kopiowania DNA. Badacze wykazali, że PIAS4 fizycznie współdziała z CDK6 w jądrze i chemicznie modyfikuje CDK6 małymi znakami „SUMO”. Te modyfikacje zwiększają zdolność CDK6 do modyfikowania RB1 oraz promowania ekspresji genów cyklu komórkowego, takich jak CDK1, E2F1, CCNE2 i CCNA2. Przy blokadzie PIAS4 fosforylacja RB1 spadała, geny docelowe RB1 były wyciszane, a cykl komórkowy zwalniał.
Dostrajanie CDK6: chemiczne znaczniki i białkowi partnerzy
Zagłębiając się dalej, zespół zmapował konkretne miejsca na CDK6 podlegające SUMOylacji i stworzył mutanty CDK6 niemożliwe do modyfikacji SUMO. Te mutanty były znacznie mniej skuteczne w aktywowaniu RB1 i przepychaniu komórek przez G1, co potwierdza, że znakowanie SUMO ma istotne funkcjonalne znaczenie. Jednocześnie zredukowanie PIAS4 stabilizowało CDK6, lecz paradoksalnie zmniejszało jego aktywność: wzrósł hamujący znak fosforylacji na CDK6, a jego współpraca z aktywatorem, cykliną D1, osłabła. Testy biochemiczne pokazały, że mimo wyższej ilości białka CDK6, komórki z niskim PIAS4 miały niższą aktywność enzymatyczną CDK6, podkreślając, że to sposób modyfikacji i interakcje białkowe decydują bardziej niż sama ilość.
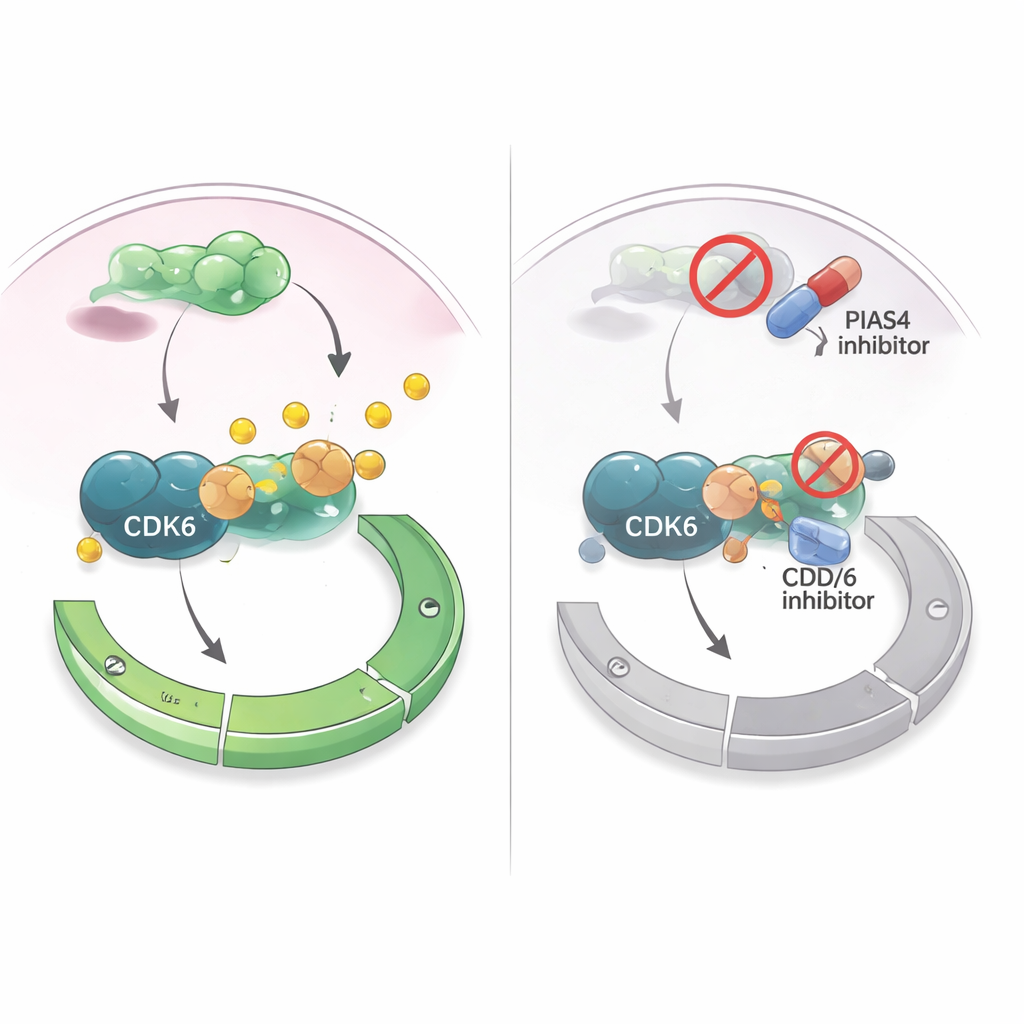
Przekucie słabości w strategię leczenia
Ponieważ inhibitory CDK4/6 są już szeroko stosowane w raku piersi dodatnim w receptorach hormonalnych, autorzy zapytali, czy ukierunkowanie na PIAS4 może wzmocnić te terapie. W hodowlach komórkowych lek, który szeroko hamuje znakowanie SUMO (w tym działanie PIAS4), uczynił inhibitory CDK4/6 bardziej skutecznymi w tłumieniu wzrostu komórek. W modelach mysich, gdzie komórki raka piersi wszczepiano do tkanki gruczołu mlekowego, jednoczesne zmniejszenie PIAS4 i CDK6 zmniejszyło guzy bardziej niż blokada samego CDK6, bez oczywistych szkód dla zwierząt. Razem wyniki sugerują, że PIAS4 działa jako wewnętrzny przyspieszacz dla CDK6 i punktu kontrolnego G1, a wyłączenie tego przyspieszacza może uczulić guzy na istniejące leki hamujące cykl komórkowy. Dla pacjentów otwiera to perspektywę, że przyszłe terapie łączące inhibitory PIAS4 lub szlaku SUMO z inhibitorami CDK4/6 mogłyby lepiej kontrolować raka piersi i opóźniać rozwój oporności.
Cytowanie: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Słowa kluczowe: rak piersi, cykl komórkowy, inhibitory CDK4/6, SUMOylacja, PIAS4