Clear Sky Science · pt
Inibição de PIAS4 induz parada do ciclo celular e exibe efeito sinérgico em combinação com inibidor de CDK4/6 no tratamento do câncer de mama
Por que esta pesquisa importa para os pacientes
O câncer de mama é um dos tipos de câncer mais comuns e letais entre mulheres, e muitos pacientes eventualmente deixam de responder aos medicamentos padrão que retardam a divisão das células tumorais. Este estudo revela uma proteína auxiliar dentro das células cancerosas, até então pouco valorizada, chamada PIAS4, que impulsiona discretamente as células através de um ponto de verificação crucial em seu ciclo de crescimento. Ao mostrar que bloquear a PIAS4 não apenas desacelera células de câncer de mama, mas também torna uma classe existente de fármacos mais potente, o trabalho aponta para uma possível nova terapia combinada que poderia manter os tumores controlados por mais tempo.
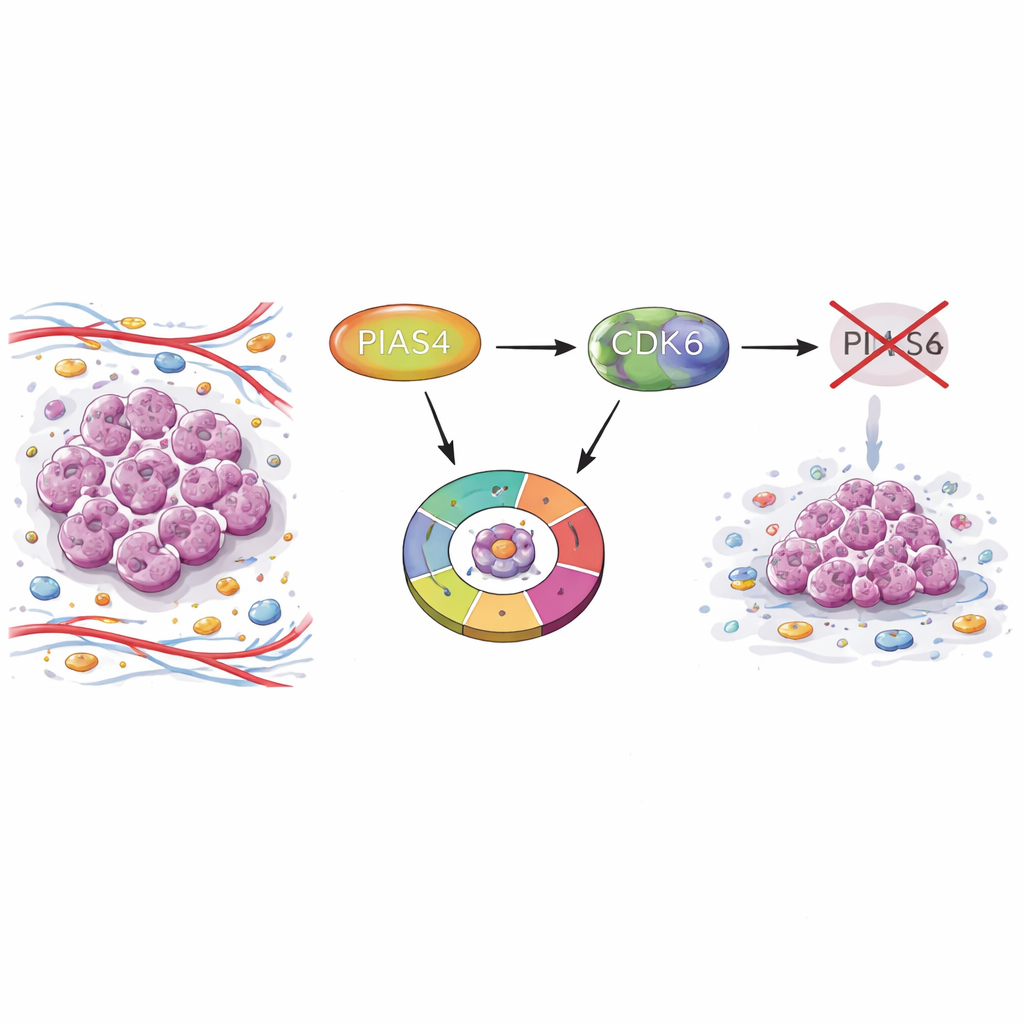
Um interruptor escondido nos tumores de mama
Os pesquisadores começaram comparando amostras tumorais com tecido mamário normal usando bases de dados de câncer em grande escala e microarranjos de tecido de pacientes. Eles descobriram que os níveis de PIAS4 eram consistentemente mais altos em tumores de mama do que em tecido saudável. Pacientes cujos tumores expressavam mais PIAS4 apresentaram pior sobrevida, sugerindo que essa proteína está ligada a uma doença mais agressiva. Importante, os níveis de PIAS4 não se correlacionaram fortemente com marcadores diagnósticos comuns como receptores de estrogênio, progesterona ou HER2, indicando que seu papel pode atravessar vários subtipos de câncer de mama.
Como a PIAS4 ajuda as células a avançarem no ciclo
As células cancerosas crescem ao passar repetidamente por um ciclo de fases, com um ponto de verificação inicial “G1” decidindo se a célula copiará seu DNA e se dividirá novamente. Usando modelos em cultura celular, a equipe reduziu a PIAS4 em células de câncer de mama e em células de camundongo. Em todos os sistemas, diminuir a PIAS4 retardou o crescimento celular e fez com que muitas células se acumulassem na fase G1, falhando em progredir para a replicação do DNA. Os cientistas confirmaram essa paralisação usando citometria de fluxo e ensaios de marcação de DNA, que mostraram menos células entrando na fase de replicação quando a PIAS4 foi bloqueada.
A parceria entre PIAS4, CDK6 e o guardião RB1
Para entender o mecanismo, a equipe concentrou-se na maquinaria molecular que rege o ponto de verificação G1, especialmente uma quinase proteica chamada CDK6 e seu famoso alvo, o supressor tumoral RB1. Normalmente, a CDK6 ativa adiciona grupos fosfato ao RB1, inativando-o e liberando uma família de fatores de transcrição para ligar genes necessários à cópia do DNA. Os pesquisadores mostraram que a PIAS4 se associa fisicamente à CDK6 dentro do núcleo e modifica quimicamente a CDK6 com pequenas marcas “SUMO”. Essas marcas aumentam a capacidade da CDK6 de modificar o RB1 e promover a expressão de genes do ciclo celular, como CDK1, E2F1, CCNE2 e CCNA2. Quando a PIAS4 foi bloqueada, a fosforilação de RB1 diminuiu, os genes-alvo do RB1 foram reduzidos e o ciclo celular desacelerou.
Refinando a CDK6: marcas químicas e proteínas parceiras
Aprofundando, a equipe mapeou sítios específicos na CDK6 que recebem marcas SUMO e criou formas mutantes de CDK6 que não podem ser SUMO-modificadas. Esses mutantes foram muito menos eficazes em ativar o RB1 ou em empurrar as células através de G1, confirmando que a marcação por SUMO não é apenas decorativa, mas funcionalmente importante. Ao mesmo tempo, a redução de PIAS4 tornou a CDK6 mais estável, mas paradoxalmente menos ativa: uma marca fosfórica inibitória na CDK6 aumentou, e sua parceria com a proteína ativadora ciclina D1 enfraqueceu. Ensaios bioquímicos mostraram que, apesar de existir mais proteína CDK6, células com baixa PIAS4 apresentaram menor atividade enzimática de CDK6, enfatizando que como a CDK6 é modificada e com quem ela se liga importa mais do que a quantidade absoluta.
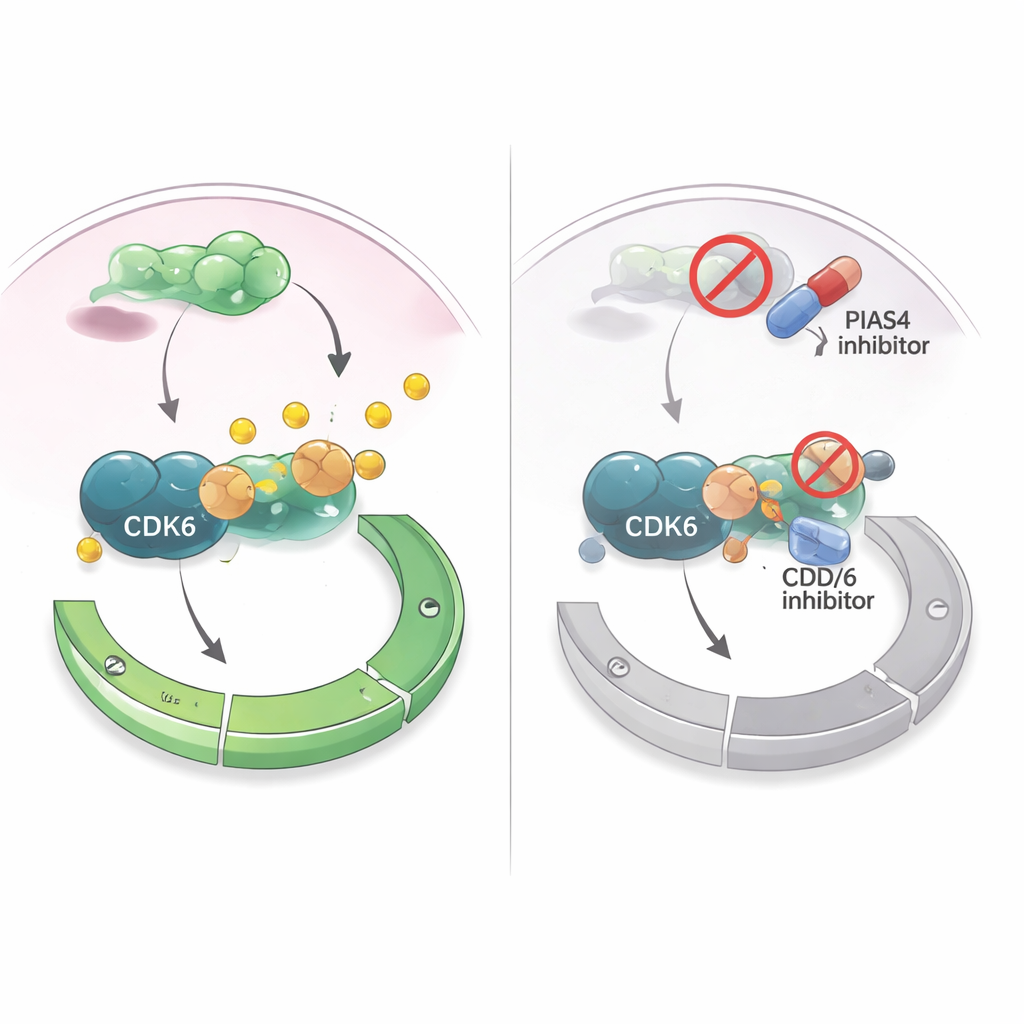
Transformando uma fraqueza em estratégia terapêutica
Como fármacos que inibem CDK4/6 já são amplamente usados no câncer de mama com receptor hormonal positivo, os autores perguntaram se direcionar a PIAS4 poderia potencializar esses tratamentos. Em células de câncer de mama cultivadas, um fármaco que interfere de forma ampla com a marcação por SUMO (incluindo as ações da PIAS4) tornou os inibidores de CDK4/6 mais eficazes em suprimir o crescimento celular. Em modelos de camundongo nos quais células de câncer de mama foram implantadas no tecido mamário, reduzir simultaneamente PIAS4 e CDK6 encolheu tumores mais do que bloquear apenas CDK6, sem dano óbvio aos animais. Em conjunto, os achados sugerem que a PIAS4 atua como um acelerador interno da CDK6 e do ponto de verificação G1, e que desabilitar esse acelerador pode sensibilizar os tumores aos fármacos existentes que atuam no ciclo celular. Para os pacientes, isso levanta a perspectiva de que terapias futuras combinando inibidores de PIAS4 ou da via SUMO com inibidores de CDK4/6 possam controlar melhor o câncer de mama e atrasar a resistência.
Citação: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Palavras-chave: câncer de mama, ciclo celular, inibidores de CDK4/6, SUMOilação, PIAS4