Clear Sky Science · es
La inhibición de PIAS4 induce detención del ciclo celular y muestra un efecto sinérgico en combinación con inhibidores de CDK4/6 en el tratamiento del cáncer de mama
Por qué esta investigación importa para los pacientes
El cáncer de mama es uno de los tipos de cáncer más frecuentes y mortales en mujeres, y muchos pacientes terminan dejando de responder a los fármacos estándar que ralentizan la división de las células tumorales. Este estudio revela una proteína auxiliar dentro de las células cancerosas, llamada PIAS4, que hasta ahora había sido poco valorada y que empuja discretamente a las células a través de un punto de control clave en su ciclo de crecimiento. Al demostrar que bloquear PIAS4 no solo ralentiza las células de cáncer de mama sino que además potencia la acción de una clase de fármacos ya existente, el trabajo señala una posible nueva terapia combinada que podría mantener los tumores controlados durante más tiempo.
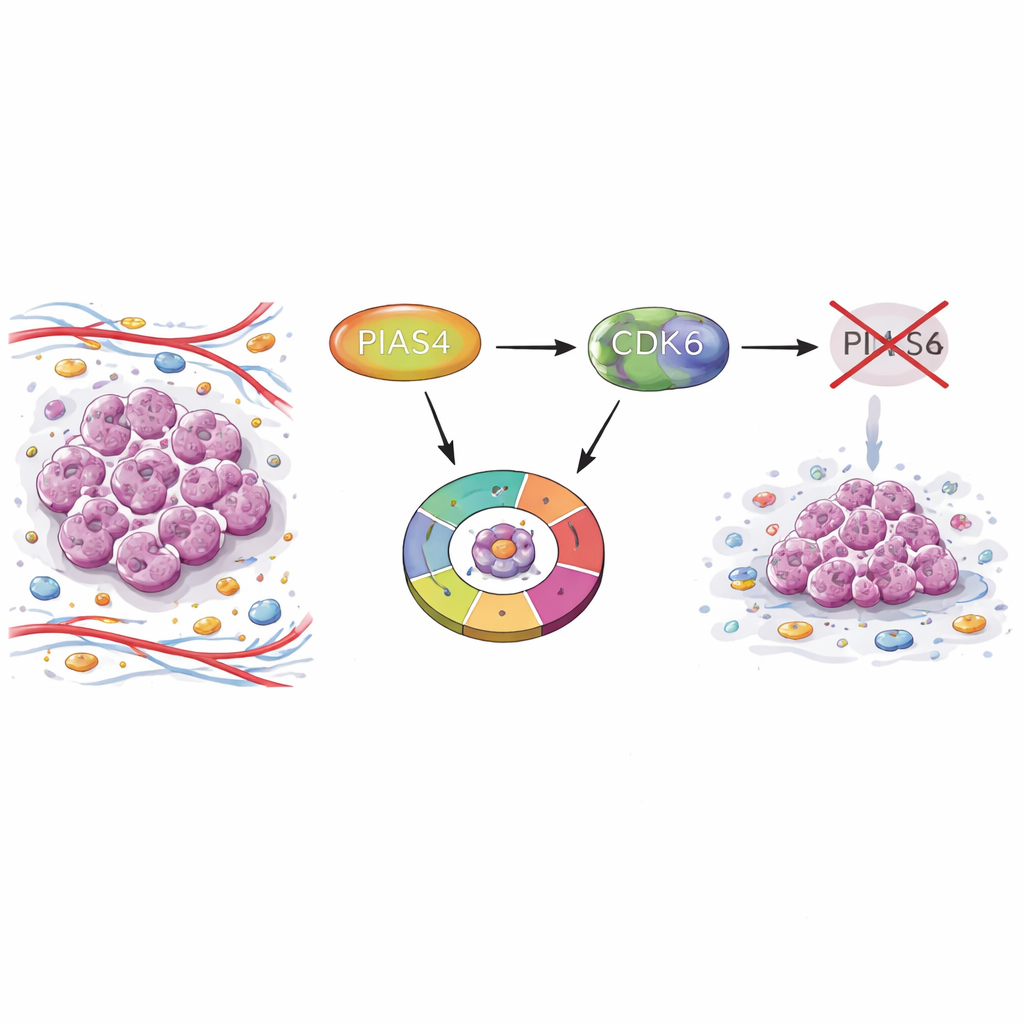
Un interruptor oculto en los tumores mamarios
Los investigadores empezaron comparando muestras tumorales con tejido mamario normal usando bases de datos oncológicas a gran escala y microarreglos de tejidos de pacientes. Encontraron que los niveles de PIAS4 eran consistentemente más altos en los tumores de mama que en el tejido sano. Los pacientes cuyos tumores producían más PIAS4 tenían una supervivencia peor, lo que sugiere que esta proteína está ligada a una enfermedad más agresiva. De forma importante, los niveles de PIAS4 no se correlacionaron fuertemente con marcadores diagnósticos comunes como los receptores de estrógeno, progesterona o HER2, lo que indica que su papel podría abarcar varios subtipos de cáncer de mama.
Cómo PIAS4 ayuda a las células a acelerar el ciclo
Las células cancerosas crecen pasando repetidamente por un ciclo de fases, con un punto de control temprano “G1” que decide si la célula copiará su ADN y volverá a dividirse. Usando modelos de cultivo celular, el equipo redujo PIAS4 en células de cáncer de mama y en células de ratón. En todos los sistemas, disminuir PIAS4 ralentizó el crecimiento celular y causó que muchas células se acumularan en la fase G1, sin avanzar a la replicación del ADN. Los científicos confirmaron este bloqueo mediante citometría de flujo y ensayos de marcado del ADN, que mostraron menos células entrando en la fase de replicación cuando PIAS4 estaba inhibida.
La asociación entre PIAS4, CDK6 y el guardián RB1
Para entender el mecanismo, el equipo se centró en la maquinaria molecular que impulsa el punto de control G1, en especial una cinasa proteica llamada CDK6 y su famoso objetivo, el supresor tumoral RB1. Normalmente, CDK6 activo añade grupos fosfato a RB1, desactivándolo y liberando a una familia de factores de transcripción para activar genes necesarios para la copia del ADN. Los investigadores mostraron que PIAS4 se asocia físicamente con CDK6 dentro del núcleo y decora químicamente a CDK6 con pequeñas etiquetas “SUMO”. Estas etiquetas mejoran la capacidad de CDK6 para modificar RB1 y promover la expresión de genes del ciclo celular como CDK1, E2F1, CCNE2 y CCNA2. Cuando PIAS4 se bloqueó, la fosforilación de RB1 disminuyó, los genes diana de RB1 se reprimieron y el ciclo celular se ralentizó.
Afinando CDK6: etiquetas químicas y proteínas asociadas
Indagando más, el equipo mapeó sitios específicos en CDK6 que reciben etiquetas SUMO y creó formas mutantes de CDK6 que no pueden ser modificadas por SUMO. Estos mutantes fueron mucho menos eficaces en activar RB1 o en impulsar a las células a través de G1, confirmando que el etiquetado por SUMO no es solo decorativo sino funcionalmente importante. Al mismo tiempo, la reducción de PIAS4 hizo que CDK6 fuera más estable pero paradójicamente menos activo: aumentó una marca fosfato inhibitoria en CDK6 y se debilitó su asociación con su proteína activadora, la ciclina D1. Ensayos bioquímicos mostraron que, pese a tener más proteína CDK6, las células con baja PIAS4 presentaban menor actividad enzimática de CDK6, subrayando que cómo se modifica CDK6 y con quién se asocia importa más que la mera cantidad.
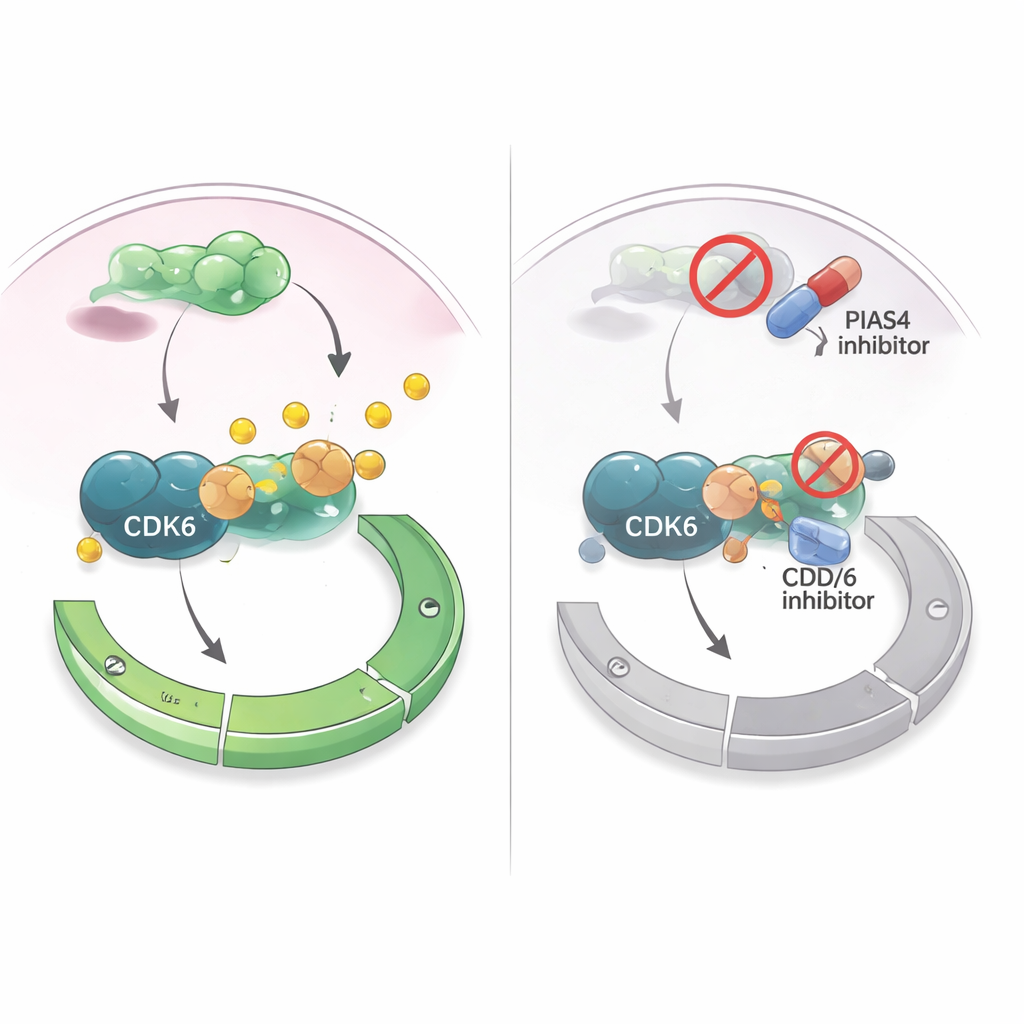
Convertir una debilidad en una estrategia terapéutica
Dado que los fármacos que inhiben CDK4/6 ya se usan ampliamente en cáncer de mama con receptores hormonales positivos, los autores se preguntaron si dirigirse a PIAS4 podría potenciar estos tratamientos. En cultivos de células de cáncer de mama, un fármaco que interfiere de forma amplia con el etiquetado por SUMO (incluyendo las acciones de PIAS4) hizo que los inhibidores de CDK4/6 fueran más eficaces suprimiendo el crecimiento celular. En modelos de ratón donde se implantaron células de cáncer de mama en tejido mamario, reducir simultáneamente PIAS4 y CDK6 encogió los tumores más que bloquear solo CDK6, sin daños evidentes en los animales. En conjunto, los hallazgos sugieren que PIAS4 actúa como un acelerador interno para CDK6 y el punto de control G1, y que deshabilitar este acelerador podría sensibilizar a los tumores a los fármacos existentes que atacan el ciclo celular. Para los pacientes, esto plantea la posibilidad de que futuras terapias que combinen inhibidores de PIAS4 o de la vía SUMO con inhibidores de CDK4/6 puedan controlar mejor el cáncer de mama y retrasar la aparición de resistencia.
Cita: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Palabras clave: cáncer de mama, ciclo celular, inhibidores de CDK4/6, SUMOilación, PIAS4