Clear Sky Science · nl
Remming van PIAS4 veroorzaakt celcyclusarrest en vertoont een synergistisch effect in combinatie met CDK4/6-remmer bij de behandeling van borstkanker
Waarom dit onderzoek belangrijk is voor patiënten
Borstkanker is een van de meest voorkomende en dodelijke vormen van kanker bij vrouwen, en veel patiënten verliezen na verloop van tijd respons op standaardmiddelen die de deling van kankercellen vertragen. Deze studie onthult een eerder onderbelicht hulpeiwit in kankercellen, PIAS4 genoemd, dat stilletjes cellen door een cruciale controlepost in hun groeicyclus duwt. Door aan te tonen dat het blokkeren van PIAS4 niet alleen borstkankercellen vertraagt maar ook een bestaande groep geneesmiddelen sterker maakt, wijst het werk op een mogelijke nieuwe combinatietherapie die tumoren langer onder controle zou kunnen houden.
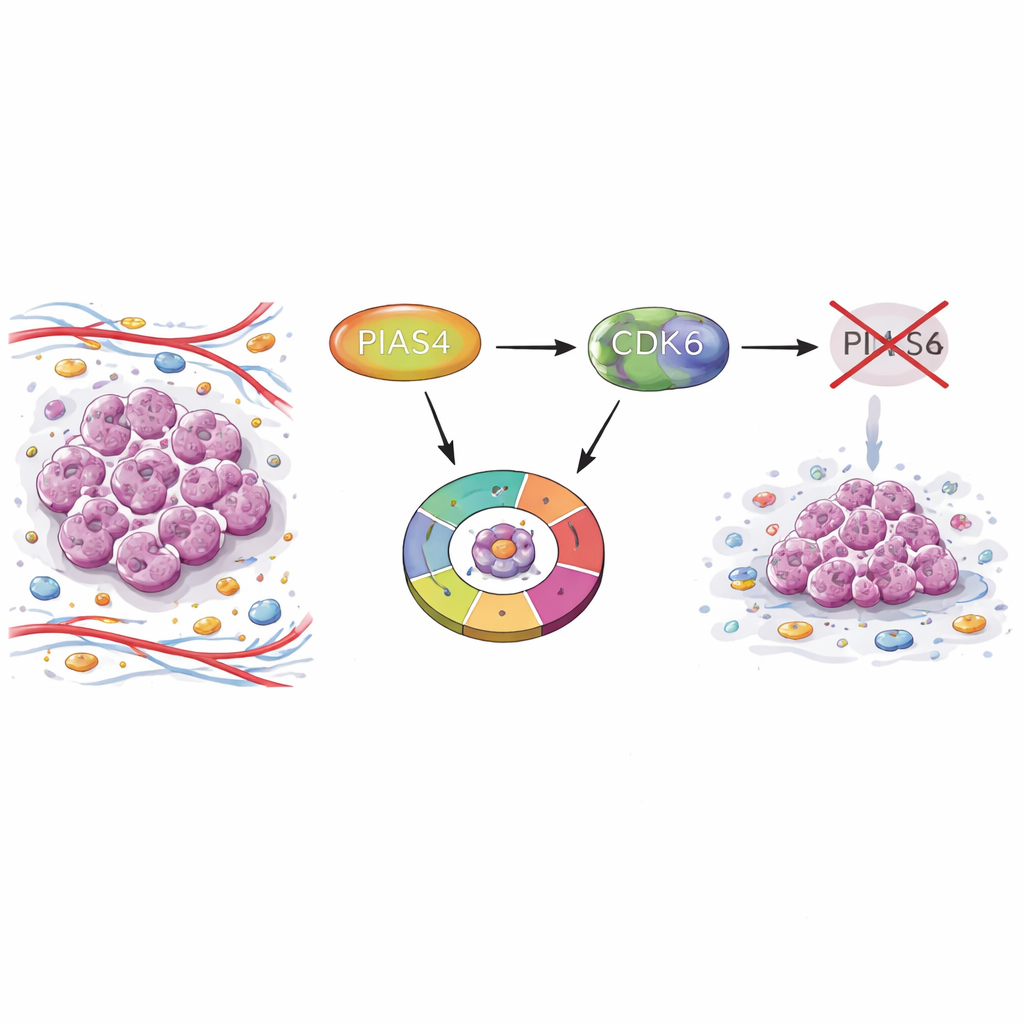
Een verborgen schakel in borsttumoren
De onderzoekers begonnen met het vergelijken van tumormonsters met normaal borstweefsel door gebruik te maken van grootschalige kankerdatabases en patiëntweefsel-microarrays. Ze ontdekten dat PIAS4-niveaus consequent hoger waren in borsttumoren dan in gezond weefsel. Patiënten van wie de tumoren meer PIAS4 produceerden, hadden een slechtere overleving, wat suggereert dat dit eiwit gekoppeld is aan agressieve ziekte. Belangrijk is dat PIAS4-niveaus niet sterk correleerden met gebruikelijke diagnostische markers zoals oestrogeen-, progesteron- of HER2-receptoren, wat aangeeft dat de rol ervan diverse borstkankersubtypen kan overspannen.
Hoe PIAS4 cellen helpt de cyclus snel te doorlopen
Kankercellen groeien door herhaaldelijk een cyclus van fasen te doorlopen, waarbij een vroege “G1”-controlepost beslist of een cel haar DNA zal kopiëren en opnieuw zal delen. Met behulp van celkweekmodellen verlaagde het team PIAS4 in borstkankercellen en in muizencellen. In alle systemen zorgde het omlaag brengen van PIAS4 voor vertraagde celgroei en stapelden veel cellen zich op in de G1-fase, waardoor ze niet doorgingen naar DNA-replicatie. De wetenschappers bevestigden deze stilstand met behulp van flowcytometrie en DNA-labelingassays, die toonden dat minder cellen de replicatiefase binnengingen wanneer PIAS4 werd geblokkeerd.
De samenwerking tussen PIAS4, CDK6 en poortwachter RB1
Om het mechanisme te begrijpen, richtte het team zich op het moleculaire machinerie dat de G1-controle stuurt, met name een proteïnekinase genaamd CDK6 en zijn bekende target, de tumorsuppressor RB1. Normaal gesproken voegt actieve CDK6 fosfaatgroepen toe aan RB1, waardoor dat uitgeschakeld wordt en een familie transcriptiefactoren vrijkomt om genen voor DNA-kopieën aan te zetten. De onderzoekers toonden aan dat PIAS4 fysiek samenkomt met CDK6 in de kern en CDK6 chemisch voorziet van kleine ‘SUMO’-labels. Deze labels verbeteren CDK6’s vermogen om RB1 te wijzigen en de expressie van celcyclusgenen zoals CDK1, E2F1, CCNE2 en CCNA2 te bevorderen. Wanneer PIAS4 werd geblokkeerd, daalde de fosforylering van RB1, werden RB1-doelgenen naar beneden bijgesteld en vertraagde de celcyclus.
Fijnregeling van CDK6: chemische labels en partnereiwitten
Dieper gravend bracht het team specifieke plaatsen op CDK6 in kaart die SUMO-tags ontvangen en creëerden mutantvormen van CDK6 die niet SUMO-gemodificeerd kunnen worden. Deze mutanten waren veel minder effectief in het activeren van RB1 of het voortstuwen van cellen door G1, wat bevestigt dat SUMO-labeling niet slechts decoratief maar functioneel belangrijk is. Tegelijkertijd zorgde PIAS4-knockdown ervoor dat CDK6 stabieler werd maar paradoxaal minder actief: een remmend fosfaatmerk op CDK6 nam toe en de samenwerking met zijn activator, cycline D1, verzwakte. Biochemische assays toonden aan dat ondanks hogere hoeveelheden CDK6-eiwit, cellen met weinig PIAS4 een lagere CDK6-enzymactiviteit hadden, wat benadrukt dat hoe CDK6 wordt gemodificeerd en met wie het bindt belangrijker is dan louter de hoeveelheid.
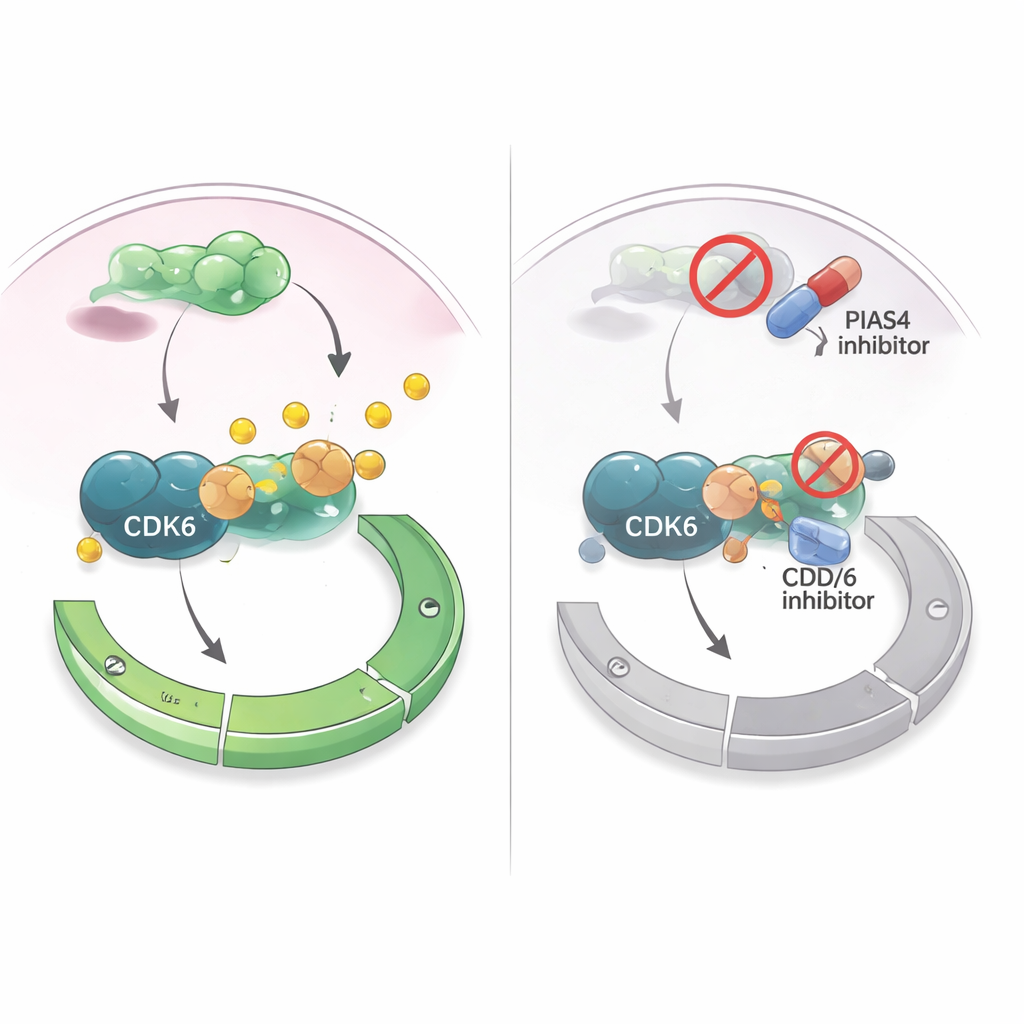
Een zwakte omzetten in een behandelingsstrategie
Aangezien geneesmiddelen die CDK4/6 remmen al veel worden gebruikt bij hormoonreceptor-positieve borstkanker, vroegen de auteurs zich af of het richten op PIAS4 deze behandelingen kon versterken. In gekweekte borstkankercellen maakte een middel dat breed de SUMO-tagging verstoort (waaronder de acties van PIAS4) CDK4/6-remmers effectiever in het onderdrukken van celgroei. In muismodellen waarin borstkankercellen in mammair weefsel werden geplaatst, krompen tumoren meer wanneer PIAS4 en CDK6 gelijktijdig werden geremd dan wanneer alleen CDK6 werd geblokkeerd, zonder duidelijke schade voor de dieren. Gezamenlijk suggereren de bevindingen dat PIAS4 fungeert als een interne versneller voor CDK6 en de G1-controle, en dat het uitschakelen van deze versneller tumoren gevoeliger kan maken voor bestaande celcyclusremmers. Voor patiënten werpt dit de mogelijkheid op dat toekomstige therapieën die PIAS4- of SUMO-route-inhibitoren combineren met CDK4/6-remmers borstkanker beter onder controle kunnen houden en resistentie mogelijk kunnen uitstellen.
Bronvermelding: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Trefwoorden: borstkanker, celcyclus, CDK4/6-remmers, SUMOylatie, PIAS4