Clear Sky Science · de
Die Hemmung von PIAS4 führt zu einem Zellzyklusstillstand und zeigt in Kombination mit CDK4/6-Inhibitoren in der Brustkrebsbehandlung einen synergistischen Effekt
Warum diese Forschung für Patientinnen wichtig ist
Brustkrebs gehört zu den häufigsten und tödlichsten Krebserkrankungen bei Frauen, und viele Patientinnen reagieren mit der Zeit nicht mehr auf Standardmedikamente, die die Teilung von Tumorzellen verlangsamen. Diese Studie identifiziert ein bislang wenig beachtetes Helferprotein in Krebszellen, PIAS4, das leise Zellen durch eine entscheidende Kontrollstation ihres Wachstumszyklus treibt. Indem gezeigt wird, dass die Blockade von PIAS4 nicht nur Brustkrebszellen verlangsamt, sondern auch eine vorhandene Wirkstoffklasse verstärkt, deutet die Arbeit auf eine mögliche neue Kombinationsstrategie hin, die Tumoren länger unter Kontrolle halten könnte.
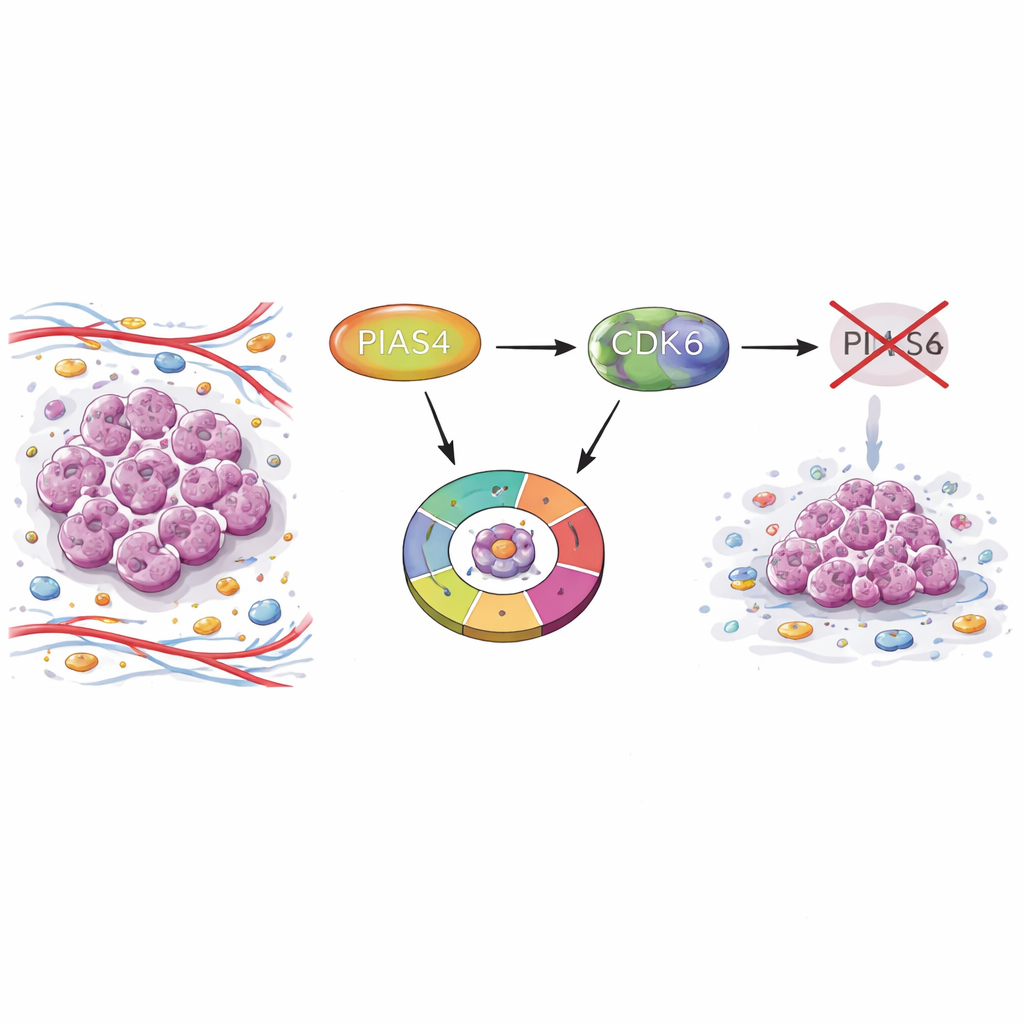
Ein verborgener Schalter in Brusttumoren
Die Forschenden begannen mit dem Vergleich von Tumorproben und normalem Brustgewebe mithilfe groß angelegter Krebsdatenbanken und Gewebemikroarrays von Patientinnen. Sie fanden heraus, dass PIAS4 in Brusttumoren durchgehend höher exprimiert war als im gesunden Gewebe. Patientinnen mit Tumoren, die mehr PIAS4 produzierten, hatten eine schlechtere Überlebensprognose, was darauf hindeutet, dass dieses Protein mit aggressivem Krankheitsverlauf verbunden ist. Wichtig ist, dass PIAS4-Spiegel nicht stark mit üblichen diagnostischen Markern wie Östrogen-, Progesteron- oder HER2-Rezeptoren korrelierten, was darauf schließen lässt, dass seine Rolle mehrere Brustkrebsuntertypen überspannen könnte.
Wie PIAS4 Zellen durch den Zyklus treibt
Krebszellen wachsen, indem sie wiederholt einen Zyklus von Phasen durchlaufen; eine frühe G1-Kontrollstation entscheidet, ob eine Zelle ihre DNA kopiert und erneut teilt. In Zellkulturmodellen reduzierten die Forschenden PIAS4 in Brustkrebs- und Mauszellen. In allen Systemen verlangsamte die Herunterregulierung von PIAS4 das Zellwachstum und führte dazu, dass viele Zellen in der G1-Phase anhäuften und nicht in die DNA-Replikation übergingen. Die Wissenschaftler bestätigten diesen Stillstand durch Durchflusszytometrie und DNA-Markierungsassays, die zeigten, dass weniger Zellen in die Replikationsphase eintraten, wenn PIAS4 blockiert war.
Die Partnerschaft zwischen PIAS4, CDK6 und dem Wächter RB1
Um den Mechanismus zu verstehen, konzentrierte sich das Team auf die molekulare Maschinerie, die die G1-Kontrolle steuert, insbesondere auf die Proteinkinase CDK6 und ihr bekanntes Ziel, den Tumorsuppressor RB1. Normalerweise fügt aktive CDK6 RB1 Phosphatgruppen hinzu, schaltet es aus und befreit so eine Familie von Transkriptionsfaktoren, die Gene für die DNA-Replikation aktivieren. Die Forschenden zeigten, dass PIAS4 im Zellkern physisch mit CDK6 assoziiert und CDK6 chemisch mit kleinen "SUMO"-Marken versieht. Diese Markierungen steigern die Fähigkeit von CDK6, RB1 zu modifizieren und die Expression von Zellzyklusgenen wie CDK1, E2F1, CCNE2 und CCNA2 zu fördern. Wenn PIAS4 blockiert wurde, nahm die Phosphorylierung von RB1 ab, RB1-Zielgene wurden herunterreguliert und der Zellzyklus verlangsamte sich.
Feinabstimmung von CDK6: chemische Anhänge und Partnerproteine
Die Gruppe ging noch weiter ins Detail: Sie kartierten spezifische Stellen auf CDK6, die SUMO-Markierungen erhalten, und erzeugten mutierte CDK6-Varianten, die nicht SUMO-modifiziert werden können. Diese Mutanten waren deutlich weniger wirksam bei der Aktivierung von RB1 oder beim Vorantreiben der Zellen durch die G1-Phase, was bestätigt, dass SUMO-Anhänge funktionell bedeutsam sind und nicht nur dekorativ. Gleichzeitig machte PIAS4-Reduktion CDK6 zwar stabiler, paradoxalerweise aber weniger aktiv: Eine inhibitorische Phosphorylierung auf CDK6 stieg an und seine Kooperation mit dem Aktivator Cyclin D1 schwächte sich. Biochemische Assays zeigten, dass trotz eines höheren CDK6-Proteinspiegels Zellen mit niedrigem PIAS4 eine geringere CDK6-Enzymaktivität aufwiesen—was unterstreicht, dass Modifikationen und Bindungspartner von CDK6 wichtiger sind als die bloße Menge.
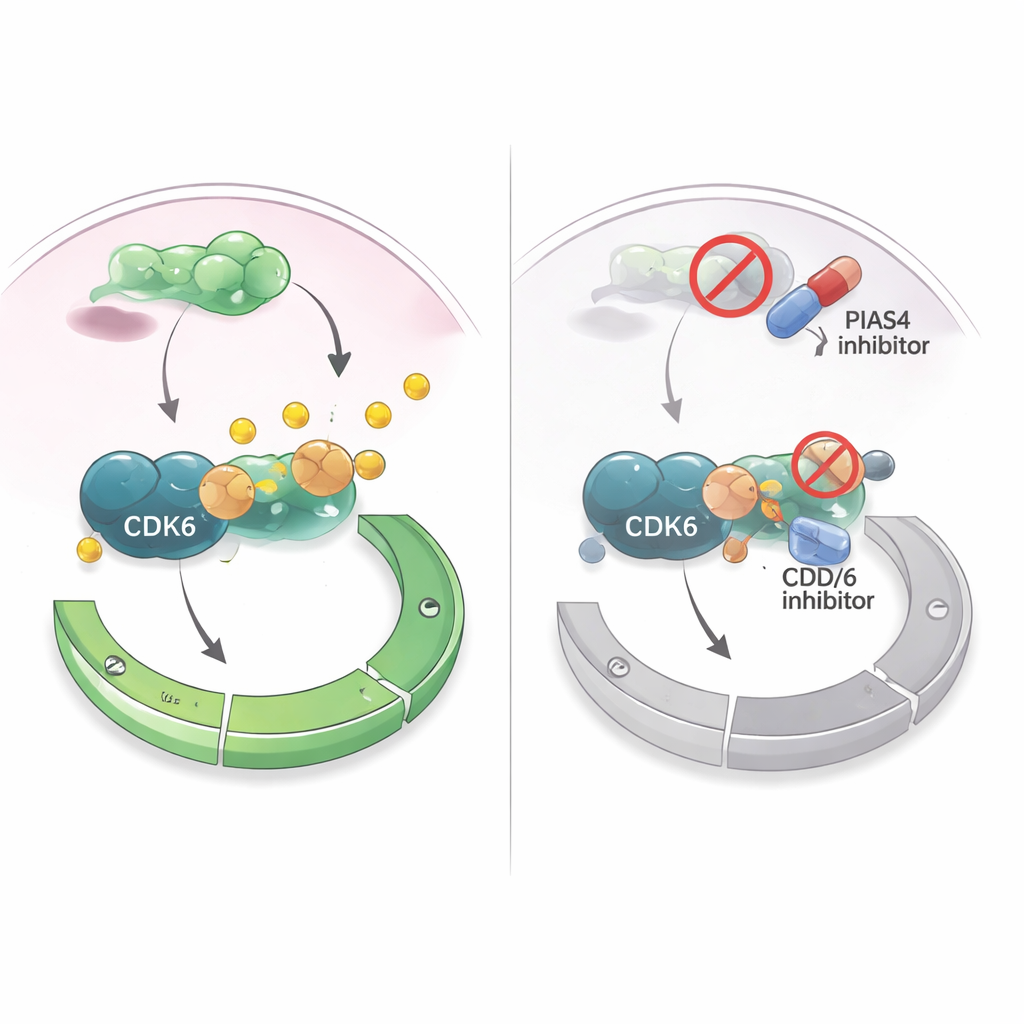
Eine Schwäche als Behandlungsstrategie nutzen
Da CDK4/6-Inhibitoren bereits weit verbreitet bei hormonsensitiven Brustkrebserkrankungen eingesetzt werden, fragten die Autorinnen und Autoren, ob die gezielte Beeinflussung von PIAS4 diese Therapien verstärken könnte. In kultivierten Brustkrebszellen machte ein Wirkstoff, der SUMO-Anhängungen (einschließlich der Aktivitäten von PIAS4) breitgreifend stört, CDK4/6-Inhibitoren wirkungsvoller bei der Wachstumshemmung. In Mausmodellen, in denen Brustkrebszellen in das Mammargewebe transplantiert wurden, führten die gleichzeitige Reduktion von PIAS4 und CDK6 zu stärkeren Tumorschrumpfungen als die Blockade von CDK6 allein, ohne offensichtliche Schäden bei den Tieren. Zusammengenommen deuten die Ergebnisse darauf hin, dass PIAS4 als interner Beschleuniger für CDK6 und die G1-Kontrolle fungiert und dass das Abschalten dieses Beschleunigers Tumoren für vorhandene Zellzyklusmedikamente sensibilisieren könnte. Für Patientinnen eröffnet dies die Aussicht, dass künftige Therapien, welche PIAS4- oder SUMO-Weg-Inhibitoren mit CDK4/6-Inhibitoren kombinieren, den Brustkrebs besser kontrollieren und Resistenzbildungen verzögern könnten.
Zitation: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Schlüsselwörter: Brustkrebs, Zellzyklus, CDK4/6-Inhibitoren, SUMOylierung, PIAS4