Clear Sky Science · ar
تثبيط PIAS4 يسبب توقّف دورة الخلية ويُظهر تأثيرًا تآزريًا عند الجمع مع مثبط CDK4/6 في علاج سرطان الثدي
لماذا هذه الدراسة مهمة للمرضى
يُعد سرطان الثدي من أكثر أنواع السرطان شيوعًا وخطورةً لدى النساء، وكثير من المرضى يتوقفون في نهاية المطاف عن الاستجابة للأدوية القياسية التي تبطئ انقسام الخلايا الورمية. تكشف هذه الدراسة عن بروتين مساعد داخل الخلايا السرطانية، يُدعى PIAS4، كان قليل التقدير سابقًا ولكنه يدفع الخلايا بهدوء عبر نقطة تحكم حاسمة في دورة نموها. من خلال إظهار أن حجب PIAS4 لا يبطئ خلايا سرطان الثدي فحسب، بل يجعل فئة موجودة من الأدوية أكثر فعالية، تشير النتائج إلى احتمال وجود تركيبة علاجية جديدة قد تُبقي الأورام تحت السيطرة لفترة أطول.
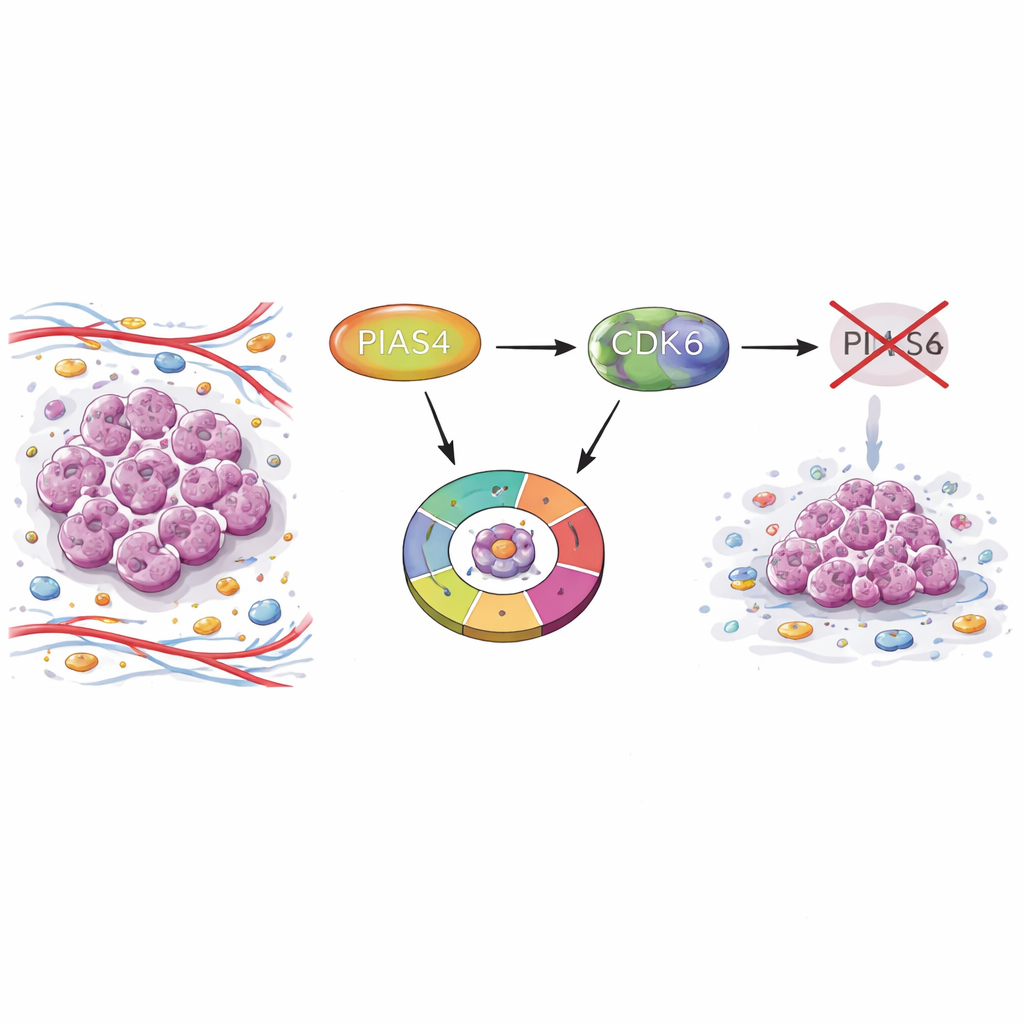
مفتاح مخفي في أورام الثدي
بدأ الباحثون بمقارنة عينات الأورام مع النسيج الثديي الطبيعي باستخدام قواعد بيانات سرطان واسعة الانتشار ومصفوفات أنسجة المرضى. وجدوا أن مستويات PIAS4 كانت أعلى بشكل ثابت في الأورام عن الأنسجة السليمة. كانت نتائج البقاء لدى المرضى الذين تُنتج أورامهم مزيدًا من PIAS4 أسوأ، مما يشير إلى ارتباط هذا البروتين بالشدة والعدوانية المرضية. ومن المهم أن مستويات PIAS4 لم تتبع بشكل قوي العلامات التشخيصية الشائعة مثل مستقبلات الإستروجين، البروجيستيرون، أو HER2، مما يدل على أن دوره قد يمتد عبر عدة أنواع فرعية من سرطان الثدي.
كيف يساعد PIAS4 الخلايا على التسارع عبر الدورة
تنمو الخلايا السرطانية عبر المرور المتكرر بدورة مكوّنة من مراحل، حيث يقرّر فحص مبكّر يُعرف بـ"G1" ما إذا كانت الخلية ستنسخ حمضها النووي وتنقسم مجددًا. باستخدام نماذج مزروعة للخلايا، خفّض الفريق مستوى PIAS4 في خلايا سرطان الثدي وفي خلايا فأر. عبر الأنظمة، أدى تقليل PIAS4 إلى إبطاء نمو الخلايا وتراكم كثير منها في طور G1، وفشلها في الانتقال إلى نسخ الحمض النووي. أكّد العلماء هذا التوقّف باستخدام معايرة تدفق الخلايا وتجارب وسم الحمض النووي، والتي أظهرت دخولًا أقل للخلايا في طور النسخ عند حجب PIAS4.
الشراكة بين PIAS4 وCDK6 والحارس RB1
لفهم الآلية، ركز الفريق على الماكينات الجزيئية التي تحرك فحص G1، لا سيما كيناز بروتيني يُدعى CDK6 وهدفه الشهير، المكبّح الورمي RB1. عادةً، يضيف CDK6 النشط مجموعات فوسفات إلى RB1، مما يعطّله ويحرر عائلة من عوامل النسخ لتشغيل جينات مطلوبة لنسخ الحمض النووي. أظهر الباحثون أن PIAS4 يرتبط جسديًا بـCDK6 داخل النواة ويزيّن CDK6 كيميائيًا بعلامات صغيرة تُسمى "SUMO". تعزز هذه العلامات قدرة CDK6 على تعديل RB1 وعلى تعزيز التعبير عن جينات دورة الخلية مثل CDK1 وE2F1 وCCNE2 وCCNA2. عندما تم حجب PIAS4، انخفض فسفرة RB1، وطُفئت جينات أهداف RB1، وتباطأت دورة الخلية.
ضبط CDK6 بدقة: علامات كيميائية وبروتينات شريكة
بالتعمق أكثر، خرّط الفريق مواقع محددة على CDK6 تستقبل علامات SUMO وأنشأ أشكالًا طفيلية من CDK6 لا يمكن تعديلها بـSUMO. كانت هذه الطفرات أقل فاعلية في تنشيط RB1 أو دفع الخلايا عبر G1، مؤكدة أن وسم SUMO ليس زخرفيًا فحسب بل ذا وظيفة مهمة. وفي الوقت نفسه، جعل خفض PIAS4 CDK6 أكثر استقرارًا لكنه — بشكل متناقض — أقل نشاطًا: ازداد وسم فوسفوري تثبيطي على CDK6، وضعُفت شراكته مع بروتين المنشط الخاص به، السيكلين D1. أظهرت اختبارات بيوكيميائية أنه بالرغم من ارتفاع كمية بروتين CDK6، كانت نشاطاته الإنزيمية أقل في الخلايا ذات PIAS4 المنخفض، مما يبرز أن كيفية تعديل CDK6 ومن يرتبط به أهم من الكمية نفسها.
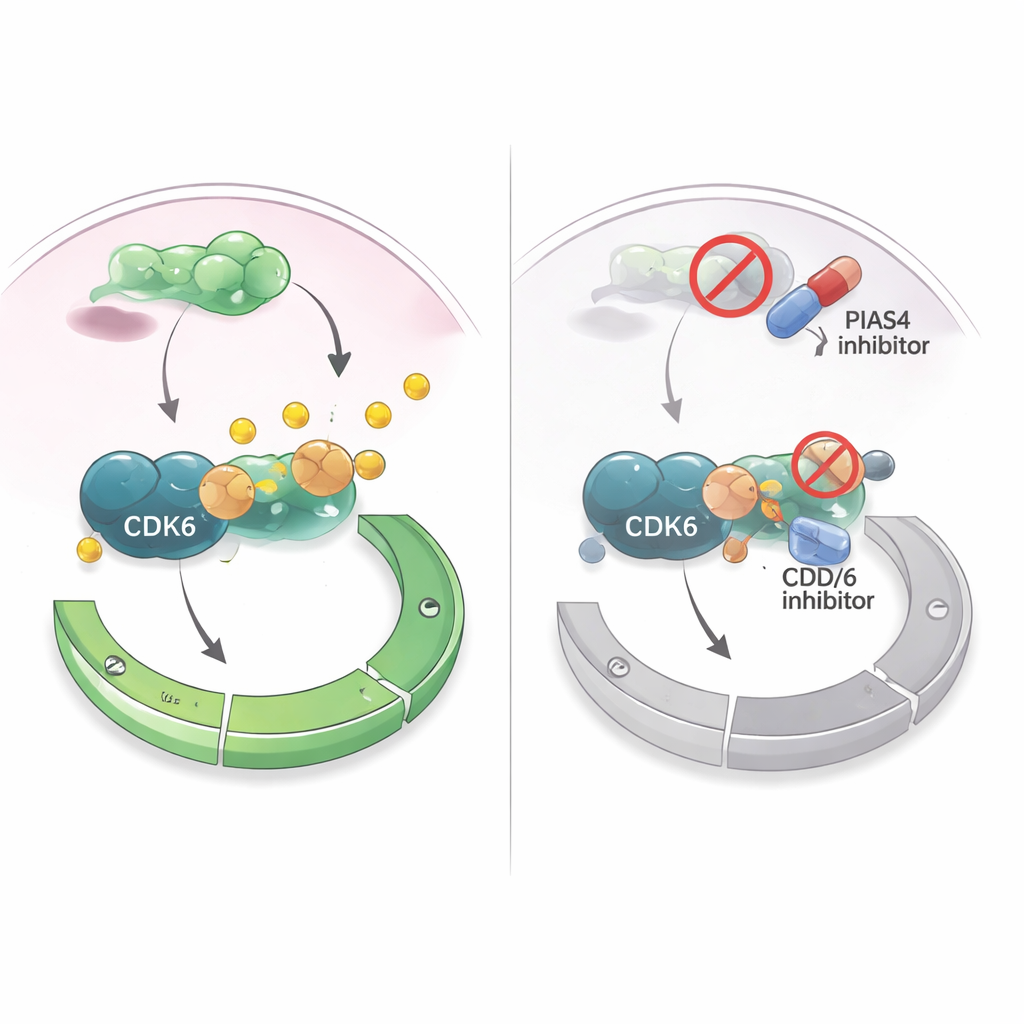
تحويل نقطة ضعف إلى استراتيجية علاجية
نظرًا لأن الأدوية التي تثبط CDK4/6 مستخدمة على نطاق واسع في سرطان الثدي موجب مستقبلات الهرمونات، تساءل الباحثون عما إذا كان استهداف PIAS4 يمكن أن يعزز هذه العلاجات. في خلايا سرطان الثدي المزروعة، جعل دواء يتداخل على نطاق واسع مع وسم SUMO (بما في ذلك أفعال PIAS4) مثبطات CDK4/6 أكثر فعالية في كبح نمو الخلايا. في نماذج فأرية حيث زُرعت خلايا سرطان الثدي في أنسجة الثدي، أدى تقليل PIAS4 وCDK6 معًا إلى تقلص الأورام أكثر من حجب CDK6 وحده، دون أضرار ظاهرة للحيوانات. توحي النتائج معًا بأن PIAS4 يعمل كمعجّل داخلي لـCDK6 وفحص G1، وأن تعطيل هذا المعجّل قد يجعل الأورام أكثر حساسية لأدوية دورة الخلية الموجودة. بالنسبة للمرضى، يفتح هذا الاحتمال بأن علاجات مستقبلية تجمع بين مثبطات PIAS4 أو مسارات SUMO مع مثبطات CDK4/6 قد تسيطر على سرطان الثدي بشكل أفضل وتؤخر ظهور المقاومة.
الاستشهاد: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
الكلمات المفتاحية: سرطان الثدي, دورة الخلية, مثبطات CDK4/6, SUMOylation, PIAS4