Clear Sky Science · sv
Hämning av PIAS4 inducerar cellcykelstopp och uppvisar en synergistisk effekt i kombination med CDK4/6-hämmare vid bröstcancerbehandling
Varför denna forskning är viktig för patienter
Bröstcancer är en av de vanligaste och dödligaste cancerformerna hos kvinnor, och många patienter slutar så småningom svara på standardläkemedel som bromsar tumörcellernas delning. Denna studie avslöjar ett tidigare undervärderat hjälpprotein inne i cancercellerna, kallat PIAS4, som diskret driver cellerna igenom en viktig kontrollpunkt i deras tillväxtcykel. Genom att visa att blockering av PIAS4 inte bara bromsar bröstcancerceller utan också gör en etablerad läkemedelsklass mer effektiv, pekar arbetet mot en potentiell ny kombinationsbehandling som skulle kunna hålla tumörer under kontroll längre.
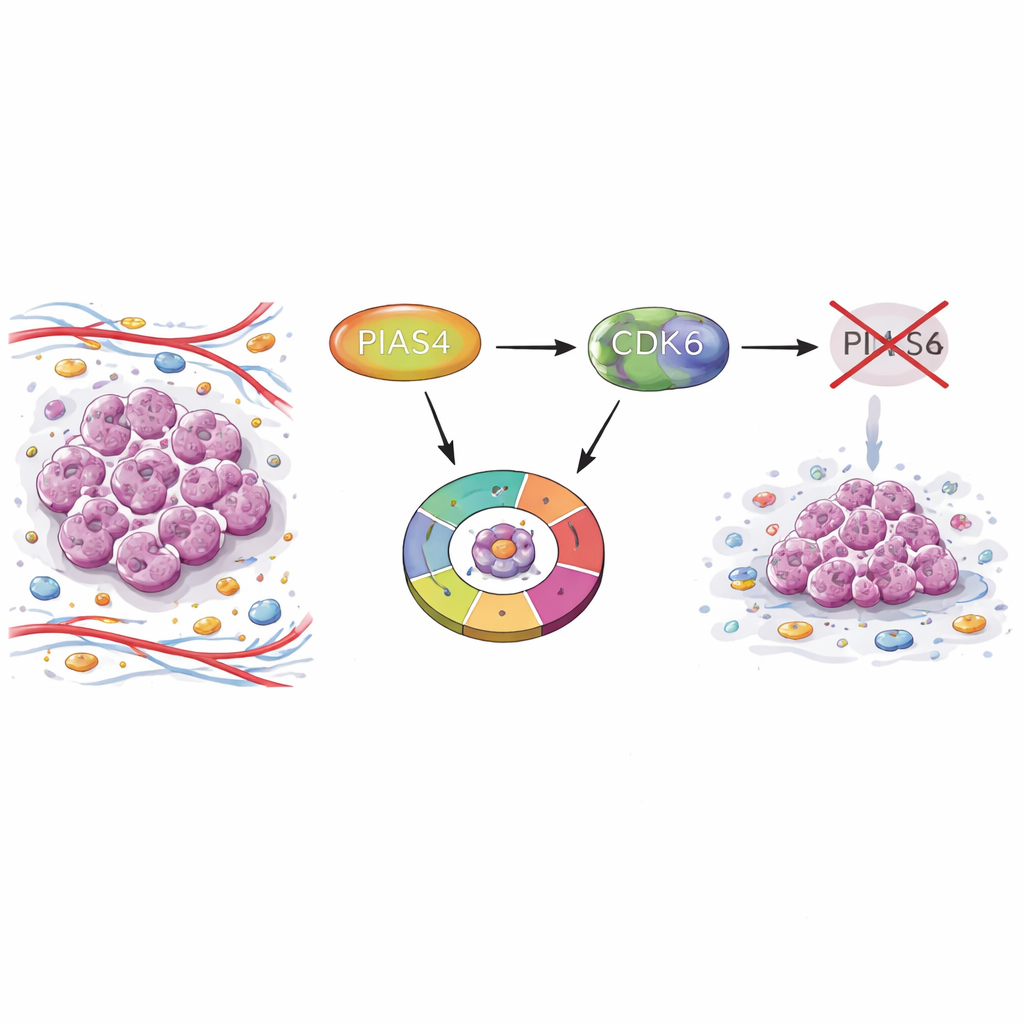
En dold strömbrytare i brösttumörer
Forskarna började med att jämföra tumörprover med normalt bröstvävnad med hjälp av storskaliga cancerdatabaser och patienttissue-mikromatriser. De fann att PIAS4-nivåerna konsekvent var högre i brösttumörer än i frisk vävnad. Patienter vars tumörer producerade mer PIAS4 hade sämre överlevnad, vilket tyder på att detta protein är kopplat till aggressiv sjukdom. Viktigt är att PIAS4-nivåerna inte starkt korrelerade med vanliga diagnostiska markörer som östrogen-, progesteron- eller HER2-receptorer, vilket antyder att dess roll kan sträcka sig över flera bröstcancersubtyper.
Hur PIAS4 hjälper celler att rusa genom cykeln
Cancerceller växer genom att upprepade gånger passera genom en cykel av faser, där en tidig "G1"-kontrollpunkt avgör om en cell ska kopiera sitt DNA och dela sig igen. Med hjälp av cellkulturmodeller minskade teamet PIAS4 i bröstcancerceller och i musceller. I olika system gjorde nedreglering av PIAS4 att celltillväxten avstannade och många celler ansamlades i G1-fasen, utan att gå vidare till DNA-replikation. Forskarna bekräftade detta stopp med flödescytometri och DNA-märkningsanalyser, som visade färre celler som gick in i replikationsfasen när PIAS4 blockeredes.
Samarbetet mellan PIAS4, CDK6 och grindvakten RB1
För att förstå mekanismen fokuserade teamet på den molekylära maskineriet som driver G1-kontrollpunkten, särskilt ett proteinkinas kallat CDK6 och dess välkända mål, tumörsuppressorn RB1. Normalt adderar aktivt CDK6 fosfatgrupper till RB1, vilket inaktiverar det och frigör en familj transkriptionsfaktorer som sätter igång gener som behövs för DNA-kopiering. Forskarna visade att PIAS4 fysiskt associerar med CDK6 inne i nukleus och kemiskt märker CDK6 med små "SUMO"-märken. Dessa märken förbättrar CDK6:s förmåga att modifiera RB1 och att främja uttrycket av cellcykelgener såsom CDK1, E2F1, CCNE2 och CCNA2. När PIAS4 blockerades föll RB1-fosforylering, RB1-målgener nedreglerades och cellcykeln förlångsammades.
Finjustering av CDK6: kemiska märken och partnerproteiner
Genom att gå djupare kartlade teamet specifika platser på CDK6 som tar emot SUMO-märken och skapade mutanta former av CDK6 som inte kan SUMO-modifieras. Dessa mutanter var mycket mindre effektiva på att aktivera RB1 eller driva celler genom G1, vilket bekräftar att SUMO-märkningen inte bara är dekorativ utan funktionellt viktig. Samtidigt gjorde PIAS4-nedreglering CDK6 mer stabilt men paradoxalt nog mindre aktivt: en inhibitorisk fosforyleringsmarkering på CDK6 ökade och dess partnerskap med dess aktivatorprotein, cyklin D1, försvagades. Biokemiska analyser visade att trots att det fanns mer CDK6-protein hade celler med låg PIAS4 lägre CDK6-enzymaktivitet, vilket understryker att hur CDK6 modifieras och vilka det binder till är viktigare än ren mängd.
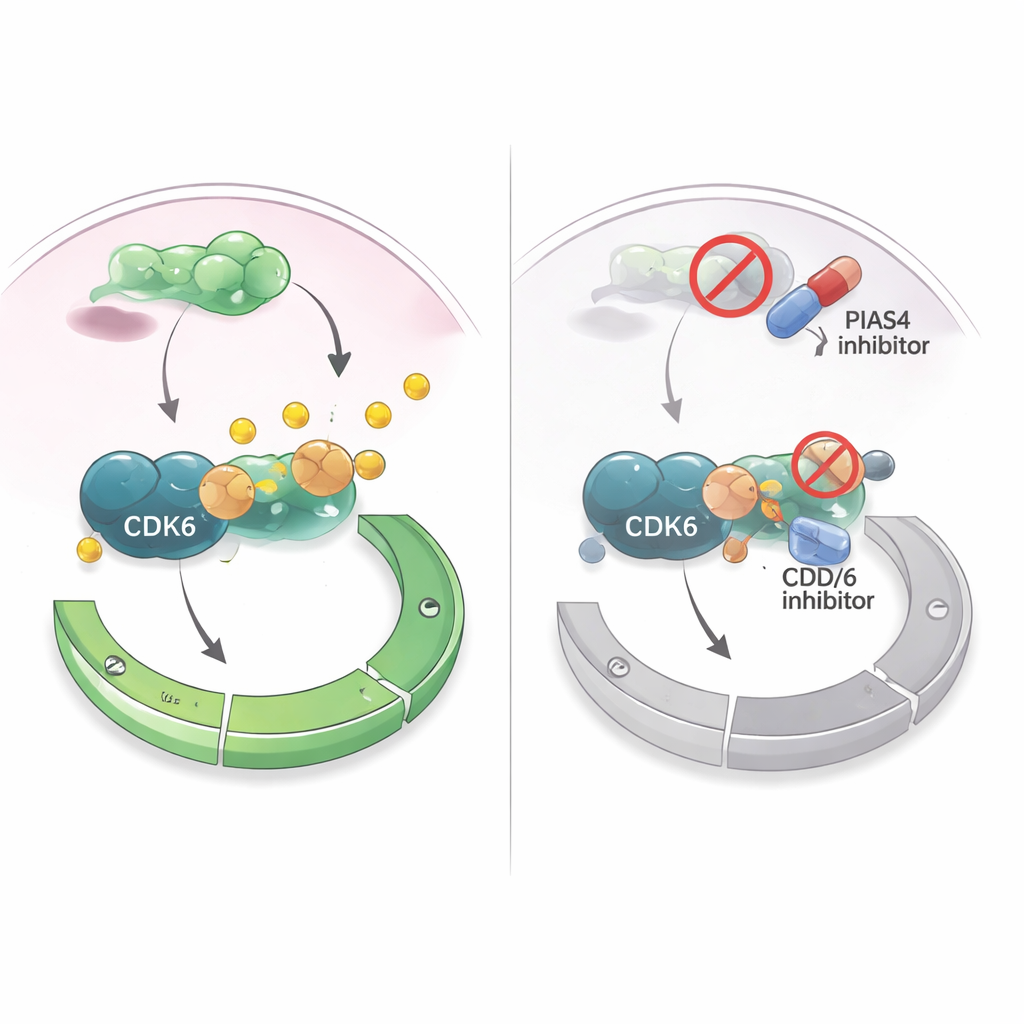
Att vända en svaghet till en behandlingsstrategi
Då läkemedel som hämmar CDK4/6 redan används i stor utsträckning vid hormonreceptorpositiv bröstcancer, frågade författarna om riktning mot PIAS4 kunde förstärka dessa behandlingar. I odlade bröstcancerceller gjorde ett läkemedel som brett stör SUMO-märkning (inklusive PIAS4:s åtgärder) CDK4/6-hämmare mer effektiva på att undertrycka celltillväxt. I musmodeller där bröstcancerceller implanterades i mammär vävnad krympte tumörer mer när PIAS4 och CDK6 samtidigt reducerades än vid enbart CDK6-blockad, utan uppenbara skador på djuren. Tillsammans tyder fynden på att PIAS4 fungerar som en intern accelerator för CDK6 och G1-kontrollpunkten, och att avaktivering av denna accelerator kan göra tumörer känsligare för befintliga cellcykelriktade läkemedel. För patienter öppnar detta möjligheten att framtida terapier som kombinerar PIAS4- eller SUMO-vägsinhibitorer med CDK4/6-hämmare skulle kunna bättre kontrollera bröstcancer och fördröja uppkomst av resistens.
Citering: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Nyckelord: bröstcancer, cellcykel, CDK4/6-hämmare, SUMOylation, PIAS4