Clear Sky Science · fr
L’inhibition de PIAS4 provoque un arrêt du cycle cellulaire et montre un effet synergique en combinaison avec un inhibiteur CDK4/6 dans le traitement du cancer du sein
Pourquoi cette recherche compte pour les patients
Le cancer du sein est l’un des cancers les plus fréquents et les plus mortels chez les femmes, et de nombreux patients finissent par ne plus répondre aux traitements standards qui ralentissent la division tumorale. Cette étude met en lumière une protéine d’aide jusque-là sous-estimée à l’intérieur des cellules cancéreuses, appelée PIAS4, qui pousse discrètement les cellules à franchir un point de contrôle clé de leur cycle de croissance. En montrant que bloquer PIAS4 ralentit non seulement les cellules de cancer du sein mais renforce aussi l’action d’une classe de médicaments existante, ce travail ouvre la voie à une nouvelle stratégie de combinaison thérapeutique susceptible de maintenir les tumeurs sous contrôle plus longtemps.
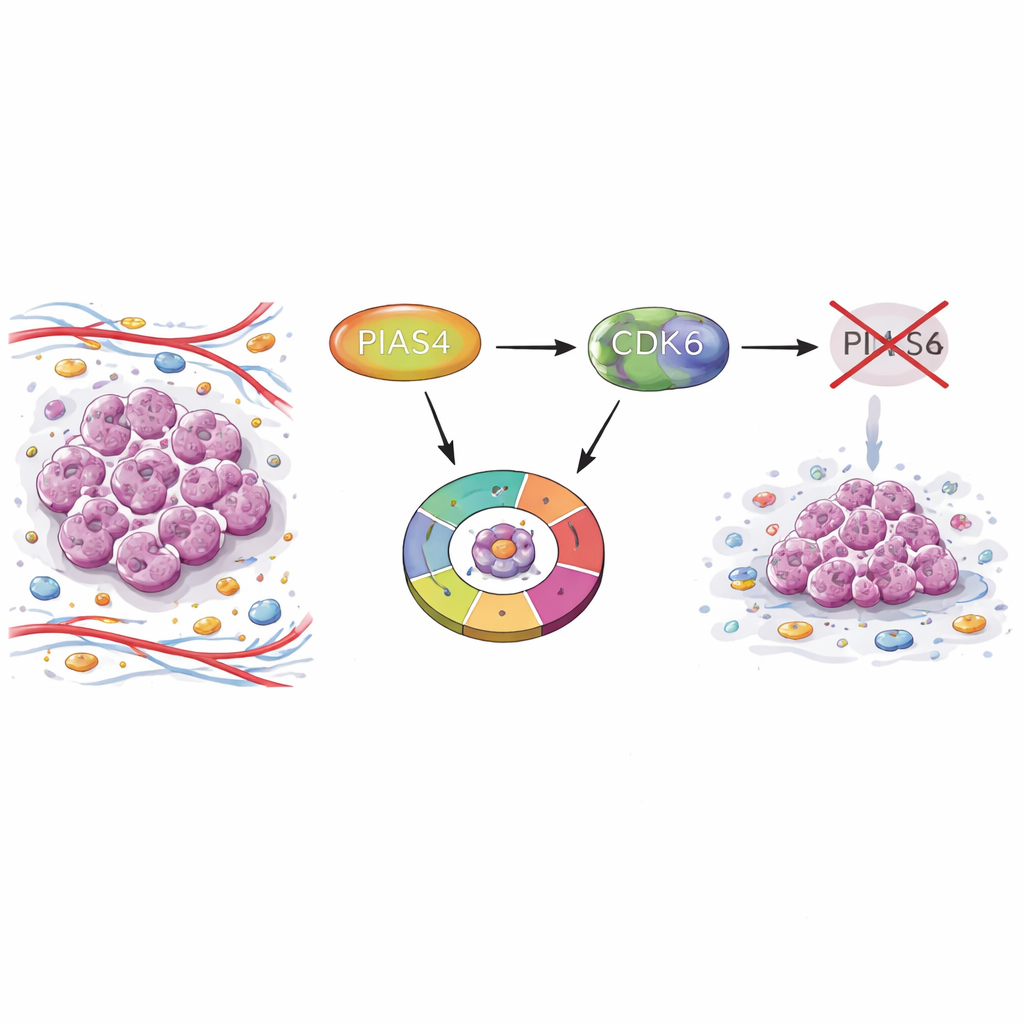
Un interrupteur caché dans les tumeurs mammaires
Les chercheurs ont commencé par comparer des échantillons tumoraux et du tissu mammaire normal en s’appuyant sur des bases de données cancérologiques à grande échelle et des microarrays de tissus de patients. Ils ont constaté que les niveaux de PIAS4 étaient systématiquement plus élevés dans les tumeurs mammaires que dans le tissu sain. Les patients dont les tumeurs exprimaient davantage de PIAS4 présentaient une survie moindre, suggérant que cette protéine est liée à une forme de maladie plus agressive. Fait important, l’expression de PIAS4 ne corrélait pas fortement avec des marqueurs diagnostiques courants comme les récepteurs aux œstrogènes, à la progestérone ou HER2, ce qui indique que son rôle pourrait traverser plusieurs sous-types de cancer du sein.
Comment PIAS4 aide les cellules à accélérer dans le cycle
Les cellules cancéreuses croissent en franchissant à répétition un cycle de phases, avec un point de contrôle précoce « G1 » qui décide si la cellule va copier son ADN et se diviser à nouveau. À l’aide de modèles en culture cellulaire, l’équipe a réduit PIAS4 dans des cellules de cancer du sein et dans des cellules de souris. Dans tous les systèmes, la diminution de PIAS4 ralentissait la croissance cellulaire et provoquait l’accumulation de nombreuses cellules en phase G1, incapables de passer à la réplication de l’ADN. Les scientifiques ont confirmé cet arrêt par cytométrie en flux et des essais de marquage de l’ADN, qui montraient moins de cellules entrant en phase de réplication lorsque PIAS4 était bloqué.
Le partenariat entre PIAS4, CDK6 et le gardien RB1
Pour comprendre le mécanisme, l’équipe s’est concentrée sur la machinerie moléculaire qui gouverne le point de contrôle G1, en particulier une kinase nommée CDK6 et sa cible bien connue, le suppresseur de tumeur RB1. Normalement, la CDK6 active ajoute des groupes phosphate sur RB1, l’inactivant et libérant une famille de facteurs de transcription pour activer les gènes nécessaires à la copie de l’ADN. Les chercheurs ont montré que PIAS4 s’associe physiquement à CDK6 dans le noyau et qu’elle modifie chimiquement CDK6 par des petites étiquettes « SUMO ». Ces étiquettes renforcent la capacité de CDK6 à modifier RB1 et à promouvoir l’expression de gènes du cycle cellulaire tels que CDK1, E2F1, CCNE2 et CCNA2. Lorsque PIAS4 était inhibée, la phosphorylation de RB1 diminuait, les gènes cibles de RB1 étaient réprimés et le cycle cellulaire ralentissait.
Affiner CDK6 : étiquettes chimiques et protéines partenaires
En approfondissant, l’équipe a cartographié des sites précis sur CDK6 recevant les étiquettes SUMO et créé des formes mutantes de CDK6 incapables d’être SUMO‑modifiées. Ces mutants étaient beaucoup moins efficaces pour activer RB1 ou faire progresser les cellules en G1, confirmant que la SUMOylation n’est pas seulement ornementale mais fonctionnellement importante. Parallèlement, l’abaissement de PIAS4 rendait CDK6 plus stable mais paradoxalement moins actif : une marque phosphate inhibitrice sur CDK6 augmentait, et son association avec sa protéine activatrice, la cycline D1, s’affaiblissait. Des essais biochimiques ont montré que, malgré une quantité accrue de protéine CDK6, les cellules à faible PIAS4 présentaient une moindre activité enzymatique de CDK6, soulignant que la manière dont CDK6 est modifiée et ses partenaires d’association importent plus que la quantité brute.
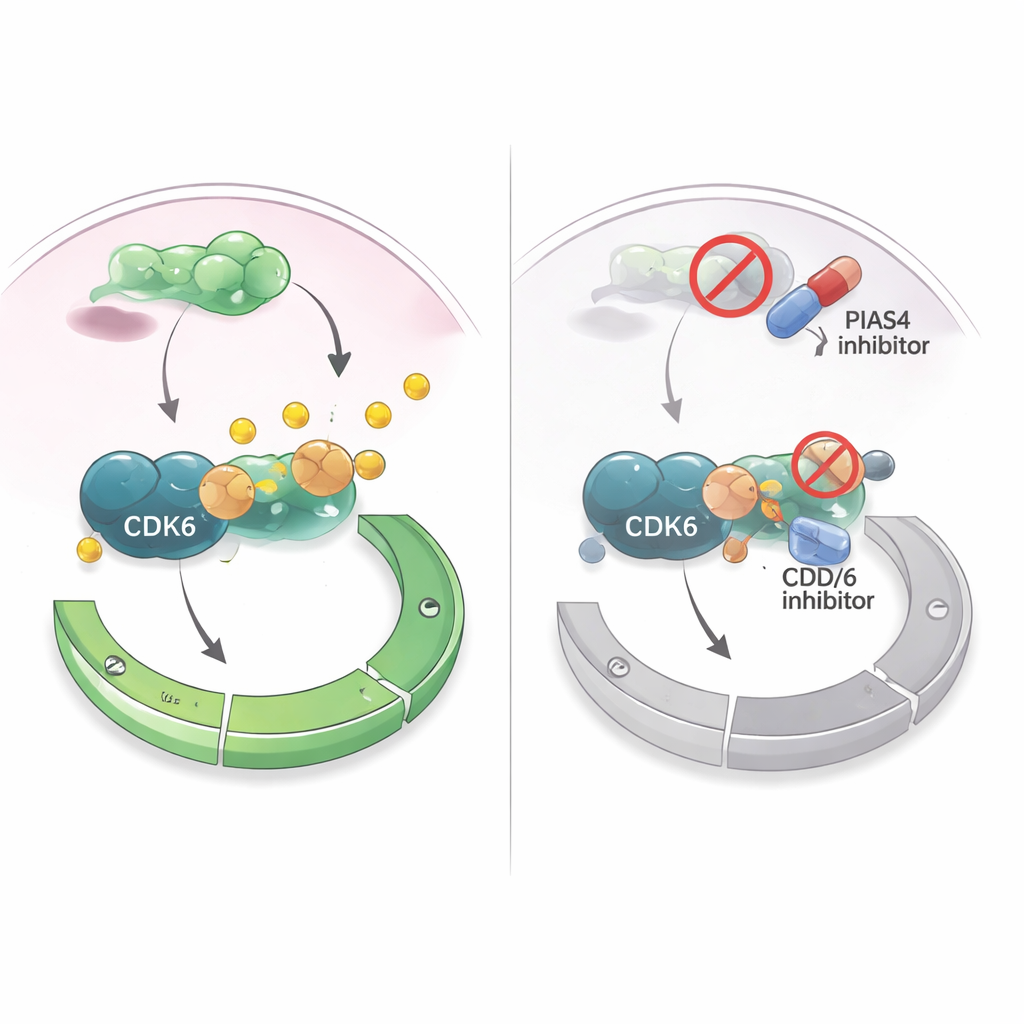
Transformer une faiblesse en stratégie thérapeutique
Étant donné que des médicaments inhibant CDK4/6 sont déjà largement utilisés dans le cancer du sein récepteur hormonal–positif, les auteurs ont testé si cibler PIAS4 pouvait renforcer ces traitements. Dans des cultures de cellules de cancer du sein, un médicament qui interfère de façon générale avec la SUMOylation (y compris l’action de PIAS4) rendait les inhibiteurs de CDK4/6 plus efficaces pour supprimer la croissance cellulaire. Dans des modèles murins où des cellules de cancer du sein étaient implantées dans le tissu mammaire, la réduction simultanée de PIAS4 et de CDK6 a réduit les tumeurs davantage que le blocage de CDK6 seul, sans effets nocifs évidents sur les animaux. Ensemble, ces résultats suggèrent que PIAS4 agit comme un accélérateur interne de CDK6 et du point de contrôle G1, et que désactiver cet accélérateur pourrait sensibiliser les tumeurs aux médicaments existants ciblant le cycle cellulaire. Pour les patients, cela ouvre la perspective que des thérapies futures combinant des inhibiteurs de PIAS4 ou de la voie SUMO avec des inhibiteurs CDK4/6 pourraient mieux contrôler le cancer du sein et retarder l’apparition de résistances.
Citation: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Mots-clés: cancer du sein, cycle cellulaire, inhibiteurs CDK4/6, SUMOylation, PIAS4