Clear Sky Science · he
עיכוב PIAS4 גורם לעצירת מחזור התא ומפגין אפקט סינרגי בשילוב עם מעכבי CDK4/6 בטיפול בסרטן השד
מדוע המחקר הזה חשוב עבור מטופלים
סרטן השד הוא אחד הגידולים השכיחים והקטלניים ביותר בנשים, ורבים מהמטופלים בסופו של דבר מפסיקים להגיב לתרופות הסטנדרטיות שמעכבות חלוקת תאי הגידול. במחקר זה זוהה חלבון עזקרתי בתוך תאי הסרטן, PIAS4, שלמעשה דוחף את התאים לעבור נקודת ביקורת חשובה במחזור הגדילה. ההדגמה כי חסימת PIAS4 לא רק מאיטה תאי סרטן שד אלא גם מחזקת קבוצה קיימת של תרופות מצביעה על אפשרות לשילוב טיפולי חדש שעשוי לשמור על הפקת הגידול תחת שליטה לפרק זמן ארוך יותר.
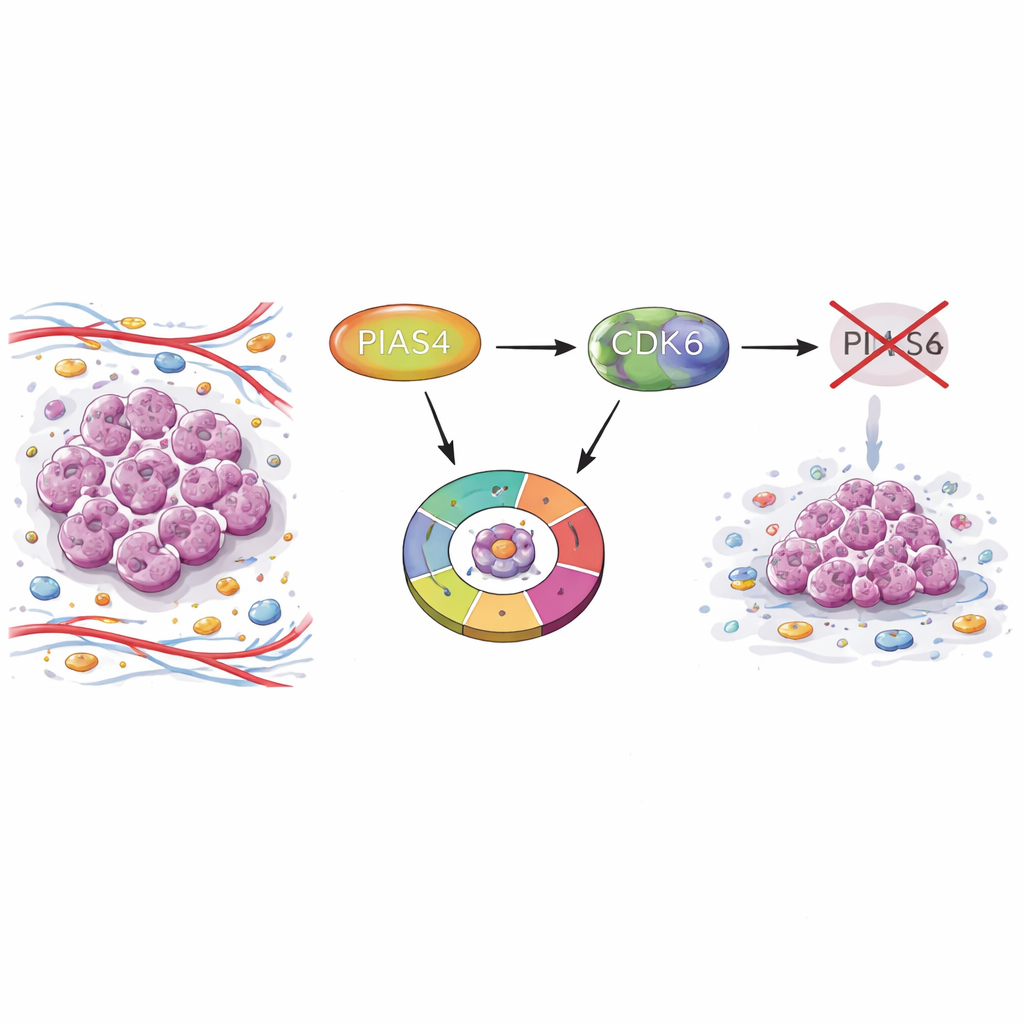
מחליף נסתר בגידולי השד
החוקרים התחילו בהשוואת דגימות גידול לעומת רקמת שד תקינה באמצעות מאגרי מידע רחבי היקף ומיקרו־אריות מרקמות מטופלים. הם מצאו שרמות PIAS4 גבוהות בעקביות בגידולי שד בהשוואה לרקמה הבריאה. מטופלים שבהם הגידול ביטא יותר PIAS4 חיו פחות זמן, מה שמרמז שחלבון זה מקושר למחלה אגרסיבית. באופן מעניין, רמות PIAS4 לא נקשרו בחוזקה לסמנים דיאגנוסטיים נפוצים כמו קולטני אסטרוגן, פרוגסטרון או HER2, דבר שמרמז שהתפקיד שלו עשוי לחצות כמה תתי־סוגים של סרטן השד.
כיצד PIAS4 מסייע לתאים לעבור במהירות את המחזור
תאי סרטן גדלים על ידי מעבר חוזר שלבי מחזור התא, כאשר נקודת הביקורת המוקדמת «G1» קובעת האם תא יארוז את ה־DNA שלו ויחלק שוב. במודלים של תרבית תאים הקטין הצוות את רמות PIAS4 בתאי סרטן השד ובתאים של עכבר. בכל המערכות, הורדת PIAS4 האטה את גדילת התאים וגרמה להצטברות רבה של תאים בשלב G1, כשהם נכשלו להמשיך לשכפול ה־DNA. המדענים אישרו את העיכוב באמצעות ציטומטריית זרימה ובדיקות תיוג DNA, שהראו פחות תאים שנכנסו לשלב השכפול כאשר PIAS4 נחסם.
השותפות בין PIAS4, CDK6 והשומר RB1
כדי להבין את המנגנון, התרכזו החוקרים במכונה המולקולרית שמניעה את נקודת הביקורת G1, במיוחד קינאזת חלבון בשם CDK6 והמטרה המפורסמת שלה, מדכא הגידול RB1. בדרך כלל CDK6 פעיל מוסיף קבוצות פוספט ל‑RB1, מדכא אותו ומשחרר משפחת גורמי שעתוק להפעיל גנים הנחוצים לשכפול ה‑DNA. החוקרים הראו כי PIAS4 מתחבר פיזית ל‑CDK6 בגרעין ומייצר על CDK6 סימוני «SUMO» קטנים. סימונים אלה משפרים את יכולת CDK6 לשנות את RB1 ולקדם ביטוי של גנים במחזור התא כגון CDK1, E2F1, CCNE2 ו‑CCNA2. כאשר PIAS4 נחסם, זיהום־הפוספט על RB1 ירד, גני היעד של RB1 דוכאו ומחזור התא האט.
כיוונון עדין של CDK6: תגיות כימיות וחלבונים שותפים
בהעמקה נוספת מיפו החוקרים את אתרי היעד על CDK6 שמקבלים תגי SUMO ויצרו צורות מוטנטיות של CDK6 שאינן ניתנות ל‑SUMOיילציה. המוטנטים הללו היו פחות יעילים בהפעלת RB1 או בקידום תאים דרך G1, וכך הראו שסימון ה‑SUMO אינו קישוט בלבד אלא חשוב תפקודית. במקביל, דיכוי PIAS4 הפך את CDK6 ליציב יותר אך פארדוקסלית פחות פעיל: סימן פוספט מעכב על CDK6 עלה, והשותפות שלו עם חלבון המפעיל שלו, ציקלין D1, נחלשה. אסודות ביוכימיות הראו שבכל זאת, אף על פי שהיה יותר חלבון CDK6, לתאים עם PIAS4 נמוך הייתה פעילות אנזימטית נמוכה יותר של CDK6, מה שמדגיש כי האופן שבו CDK6 מותאם ומי הוא השותף שלו חשובים יותר מכמותו הגולמית.
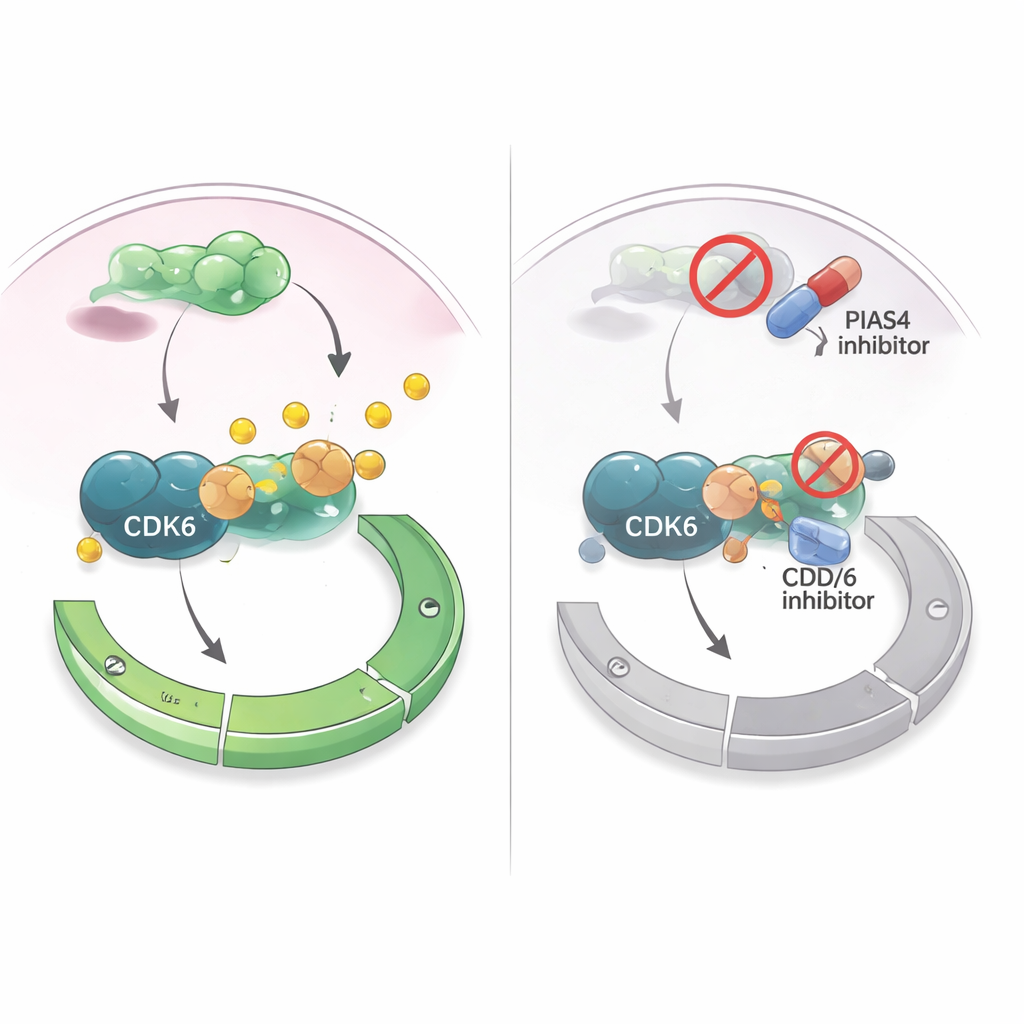
הפיכת חולשה לאסטרטגיית טיפול
מכיוון שתרופות המעכבות CDK4/6 כבר נמצאות בשימוש נרחב בסרטן השד חיובי לקולטנים הורמונליים, בדקו המחברים האם מיקוד ב‑PIAS4 יכול להגביר טיפולים אלה. בתאי סרטן שד בתרבית, תרופה שמתערבת באופן רחב בסימון SUMO (כולל פעולות PIAS4) הפכה את מעכבי CDK4/6 ליעילים יותר בעיכוב גדילת התאים. במודלי עכבר שבהם שתלו תאי סרטן השד ברקמת השד, הקטנת PIAS4 במקביל ל‑CDK6 הקטינה את הגידולים יותר מאשר חסימת CDK6 לבדה, ללא פגיעה בולטת בבעלי החיים. יחד, הממצאים מצביעים על כך ש‑PIAS4 פועל כמאיץ פנימי של CDK6 ונקודת הביקורת G1, וכי השתקת המאיץ הזה עשויה לחזק גידולים כלפי תרופות למחזור התא הקיימות. עבור מטופלים, הדבר מעלה את האפשרות שטיפולים עתידיים המשלבים מעכבי PIAS4 או מעכבי מסלול SUMO עם מעכבי CDK4/6 עשויים לשלוט טוב יותר בסרטן השד ולדחות את הופעת העמידות.
ציטוט: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
מילות מפתח: סרטן השד, מחזור התא, מעכבי CDK4/6, SUMOילציה, PIAS4