Clear Sky Science · tr
PIAS4 inhibisyonu hücre döngüsü duraklaması tetikler ve meme kanseri tedavisinde CDK4/6 inhibitörü ile kombinasyonda sinerjik etki gösterir
Bu araştırma hastalar için neden önemli
Meme kanseri, kadınlarda en yaygın ve ölümcül kanserlerden biridir ve birçok hasta nihayetinde tümör hücrelerinin bölünmesini yavaşlatan standart ilaçlara cevap vermeyi bırakır. Bu çalışma, kanser hücreleri içinde daha önce yeterince fark edilmeyen bir yardımcı protein olan PIAS4’ü ortaya koyuyor; bu protein, hücrelerin büyüme döngüsündeki önemli bir kontrol noktasından sessizce geçmelerini sağlar. PIAS4’ü engellemenin sadece meme kanseri hücrelerini yavaşlatmakla kalmayıp mevcut bir ilaç sınıfını da güçlendirdiğini göstererek, çalışma tümörleri daha uzun süre kontrol altında tutabilecek potansiyel yeni bir kombinasyon tedavisine işaret ediyor.
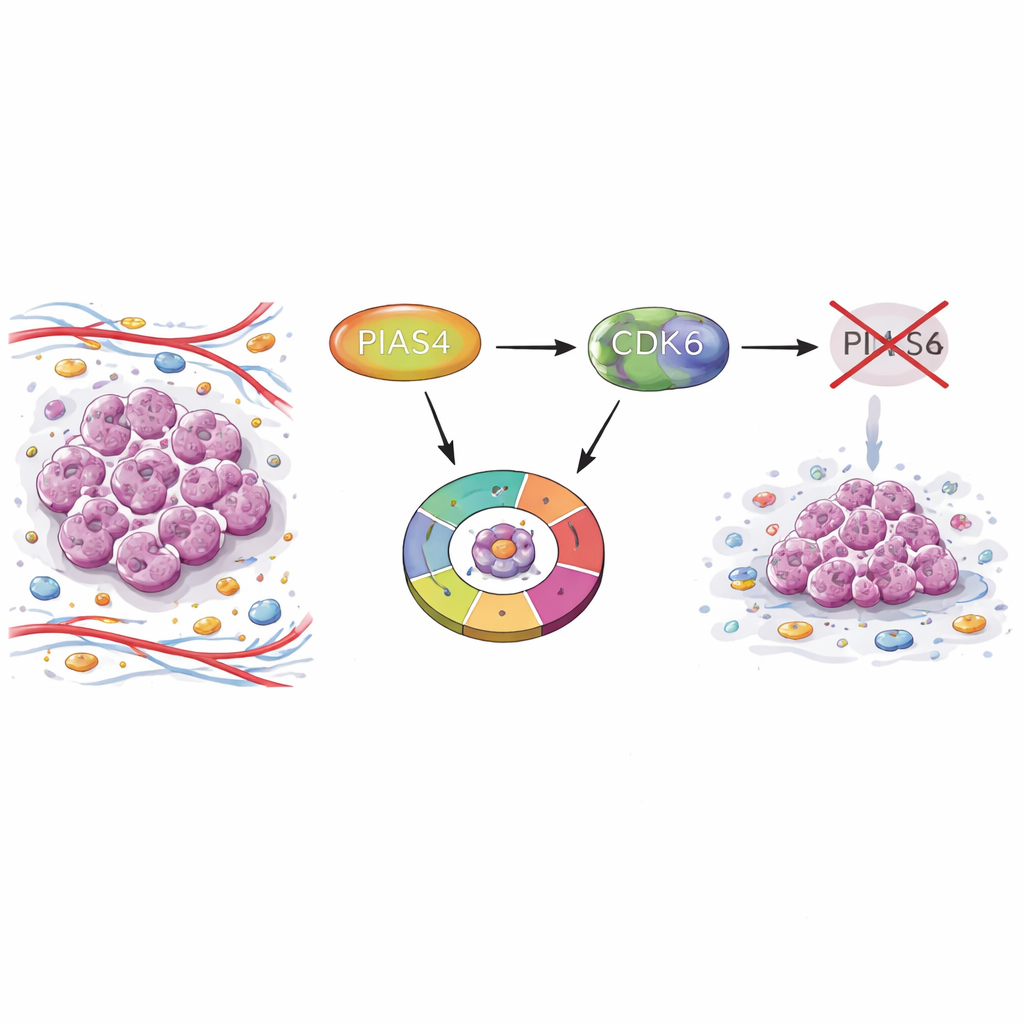
Meme tümörlerinde gizli bir anahtar
Araştırmacılar, büyük ölçekli kanser veritabanları ve hasta doku mikroarray’leri kullanarak tümör örneklerini normal meme dokusuyla karşılaştırmakla başladılar. PIAS4 seviyelerinin sağlıklı dokuya göre meme tümörlerinde tutarlı şekilde daha yüksek olduğunu buldular. Tümörü daha fazla PIAS4 üreten hastaların daha kötü sağkalıma sahip olması, bu proteinin agresif hastalıkla ilişkili olduğunu düşündürüyor. Önemli olarak, PIAS4 seviyeleri östrojen, progesteron veya HER2 reseptörleri gibi yaygın tanısal belirteçlerle güçlü bir şekilde örtüşmedi; bu da rolünün birkaç meme kanseri alt tipini kesebileceğini gösteriyor.
PIAS4’ün hücrelerin döngüde hızlanmasına nasıl yardımcı olduğu
Kanser hücreleri, tekrar tekrar bir dizi evreden geçerek büyür; erken bir "G1" kontrol noktası, bir hücrenin DNA’sını kopyalayıp yeniden bölünüp bölünmeyeceğine karar verir. Hücre kültürü modelleri kullanarak ekip, meme kanseri hücrelerinde ve fare hücrelerinde PIAS4’ü azalttı. Sistemler arasında PIAS4’ün azaltılması hücre büyümesini yavaşlattı ve birçok hücrenin G1 fazında birikmesine, DNA replikasyonuna ilerleyememesine neden oldu. Bilim insanları, akış sitometrisi ve DNA etiketleme testleri kullanarak bu duraklamayı doğruladılar; PIAS4 bloke edildiğinde replikasyon fazına giren hücre sayısının azaldığını gösterdiler.
PIAS4, CDK6 ve bekçi RB1 arasındaki iş birliği
Mekanizmayı anlamak için ekip, özellikle bir protein kinaz olan CDK6 ve onun ünlü hedefi tümör baskılayıcı RB1 olmak üzere G1 kontrol noktasını yöneten moleküler makineye odaklandı. Normalde aktif CDK6, RB1’e fosfat grupları ekleyerek onu kapatır ve böylece bir grup transkripsiyon faktörünün DNA kopyalanması için gerekli genleri açmasına izin verir. Araştırmacılar, PIAS4’ün çekirdek içinde CDK6 ile fiziksel olarak ilişkili olduğunu ve CDK6’yı küçük “SUMO” etiketleriyle kimyasal olarak süslediğini gösterdiler. Bu etiketler CDK6’nın RB1’i değiştirme yeteneğini ve CDK1, E2F1, CCNE2 ve CCNA2 gibi hücre döngüsü genlerinin ifadesini artırıyor. PIAS4 bloke edildiğinde RB1 fosforilasyonu düştü, RB1 hedef genleri aşağı yönlü düzenlendi ve hücre döngüsü yavaşladı.
CDK6’yı ince ayarlama: kimyasal etiketler ve ortak proteinler
Daha derine inen ekip, SUMO etiketlerini alan CDK6 üzerindeki belirli bölgeleri haritaladı ve SUMO ile modifiye edilemeyen CDK6 mutant formları oluşturdu. Bu mutantlar RB1’i aktifleştirme veya hücreleri G1’den geçirme konusunda çok daha az etkiliydi; bu da SUMO etiketlemenin sadece süsleyici değil, işlevsel olarak önemli olduğunu doğruladı. Aynı zamanda, PIAS4ün susturulması CDK6’yı daha kararlı hale getirdi ancak paradoksal olarak daha az aktif yaptı: CDK6 üzerinde inhibe edici bir fosfat işareti arttı ve aktivatör protein olan siklin D1 ile ortaklığı zayıfladı. Biyokimyasal testler, daha fazla CDK6 proteini bulunmasına rağmen, düşük PIAS4’e sahip hücrelerin daha düşük CDK6 enzim aktivitesine sahip olduğunu gösterdi; bu da CDK6’nın nasıl modifiye edildiğinin ve kiminle bağlandığının salt miktardan daha önemli olduğunu vurguluyor.
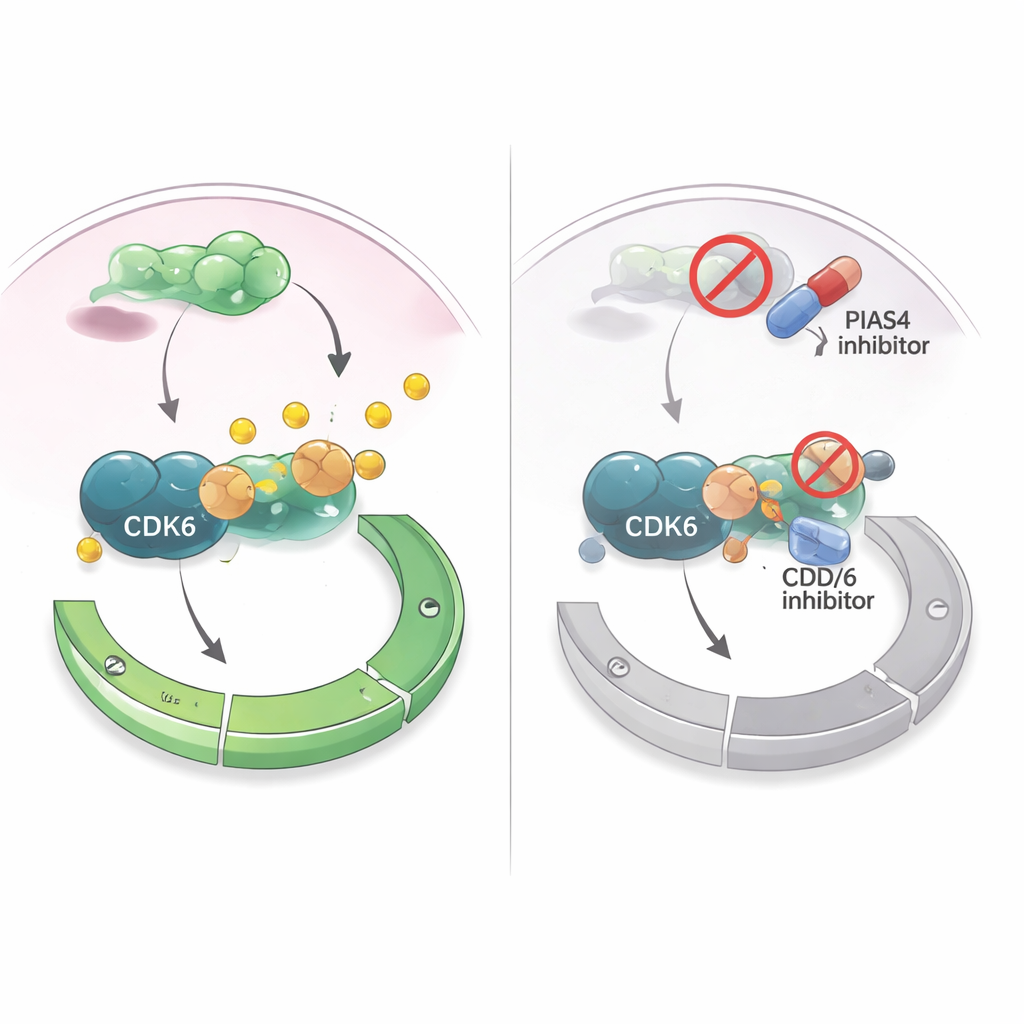
Zayıflığı bir tedavi stratejisine dönüştürmek
CDK4/6’yı inhibe eden ilaçlar halihazırda hormon reseptör–pozitif meme kanserinde yaygın olarak kullanıldığından, yazarlar PIAS4’ü hedeflemenin bu tedavileri güçlendirip güçlendiremeyeceğini sordular. Kültürdeki meme kanseri hücrelerinde, SUMO etiketlemeyi geniş ölçüde engelleyen (PIAS4’ün eylemlerini de içeren) bir ilaç, CDK4/6 inhibitörlerini hücre büyümesini baskılama konusunda daha etkili kıldı. Meme kanseri hücrelerinin meme dokusuna nakledildiği fare modellerinde, eşzamanlı olarak PIAS4 ve CDK6’nın azaltılması, yalnızca CDK6’yı engellemekten daha fazla tümör küçülmesi sağladı ve hayvanlara bariz bir zarar vermedi. Birlikte, bulgular PIAS4’ün CDK6 ve G1 kontrol noktası için içsel bir hızlandırıcı olarak işlediğini ve bu hızlandırıcı devre dışı bırakıldığında tümörlerin mevcut hücre döngüsü ilaçlarına duyarlı hale gelebileceğini öne sürüyor. Hastalar için bu, gelecekte PIAS4 veya SUMO yolu inhibitörlerinin CDK4/6 inhibitörleriyle kombinasyonunun meme kanserini daha iyi kontrol edebileceği ve direnç gelişimini geciktirebileceği olasılığını gündeme getiriyor.
Atıf: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Anahtar kelimeler: meme kanseri, hücre döngüsü, CDK4/6 inhibitörleri, SUMOylasyon, PIAS4