Clear Sky Science · it
L'inibizione di PIAS4 induce l'arresto del ciclo cellulare e mostra un effetto sinergico in combinazione con un inibitore CDK4/6 nel trattamento del cancro al seno
Perché questa ricerca è importante per i pazienti
Il cancro al seno è uno dei tumori più comuni e letali nelle donne, e molti pazienti finiscono col perdere la risposta ai farmaci standard che rallentano la divisione delle cellule tumorali. Questo studio mette in luce una proteina ausiliaria finora poco considerata all'interno delle cellule cancerose, chiamata PIAS4, che spinge silenziosamente le cellule oltre un punto di controllo chiave del loro ciclo di crescita. Mostrando che bloccare PIAS4 non soltanto rallenta le cellule del cancro al seno ma rende anche più efficace una classe di farmaci già esistente, il lavoro indica una possibile nuova terapia combinata che potrebbe mantenere i tumori sotto controllo più a lungo.
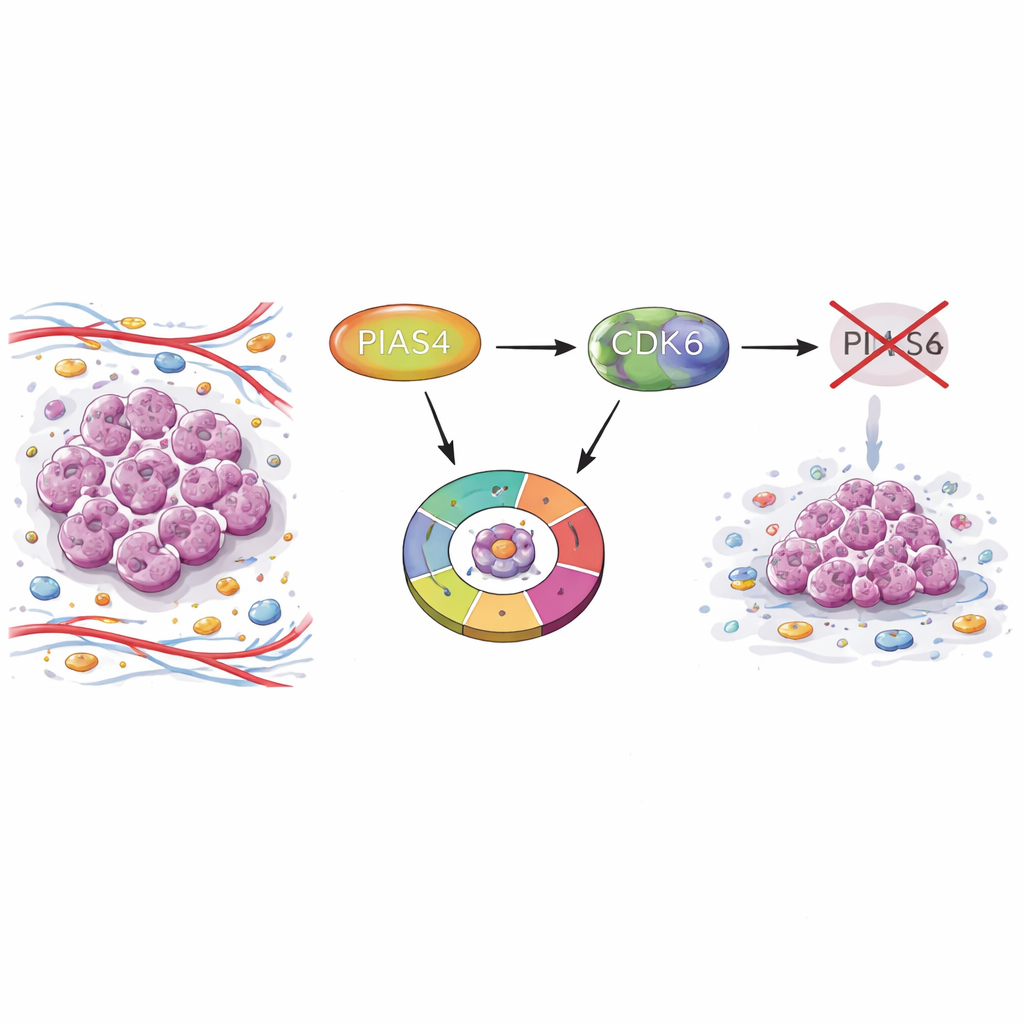
Un interruttore nascosto nei tumori mammari
I ricercatori hanno cominciato confrontando campioni tumorali con tessuto mammario normale usando banche dati oncologiche su larga scala e microarray di tessuto di pazienti. Hanno riscontrato che i livelli di PIAS4 erano costantemente più alti nei tumori mammari rispetto al tessuto sano. I pazienti i cui tumori esprimevano più PIAS4 avevano una sopravvivenza peggiore, suggerendo che questa proteina sia legata a una malattia più aggressiva. È importante sottolineare che i livelli di PIAS4 non si correlavano fortemente con marcatori diagnostici comuni come i recettori per estrogeni, progesterone o HER2, indicando che il suo ruolo potrebbe attraversare diversi sottotipi di cancro al seno.
Come PIAS4 aiuta le cellule a correre attraverso il ciclo
Le cellule tumorali crescono passando ripetutamente attraverso un ciclo di fasi, con un punto di controllo iniziale “G1” che decide se una cellula copierà il suo DNA e si dividerà di nuovo. Utilizzando modelli in coltura cellulare, il gruppo ha ridotto PIAS4 in cellule di cancro al seno e in cellule murine. In tutti i sistemi, l'abbassamento di PIAS4 ha rallentato la crescita cellulare e fatto accumulare molte cellule nella fase G1, impedendo il passaggio alla replicazione del DNA. Gli scienziati hanno confermato questo stallo con citometria a flusso e saggi di marcatura del DNA, che hanno mostrato meno cellule che entravano nella fase di replicazione quando PIAS4 era bloccata.
La collaborazione tra PIAS4, CDK6 e il guardiano RB1
Per comprendere il meccanismo, il team si è concentrato sulla macchina molecolare che guida il controllo G1, in particolare su una chinasi proteica chiamata CDK6 e sul suo noto bersaglio, il soppressore tumorale RB1. Normalmente, CDK6 attivo aggiunge gruppi fosfato a RB1, inattivandolo e liberando una famiglia di fattori di trascrizione che attivano i geni necessari per la copia del DNA. I ricercatori hanno dimostrato che PIAS4 si associa fisicamente a CDK6 nel nucleo e ne decora chimicamente CDK6 con piccoli tag “SUMO”. Questi tag aumentano la capacità di CDK6 di modificare RB1 e di promuovere l'espressione di geni del ciclo cellulare come CDK1, E2F1, CCNE2 e CCNA2. Quando PIAS4 è stata bloccata, la fosforilazione di RB1 è diminuita, i geni bersaglio di RB1 sono stati downregolati e il ciclo cellulare ha rallentato.
Regolazione fine di CDK6: tag chimici e proteine partner
Approfondendo, il gruppo ha mappato siti specifici su CDK6 che ricevono i tag SUMO e ha creato forme mutanti di CDK6 che non possono essere SUMOilate. Questi mutanti erano molto meno efficaci nell'attivare RB1 o nel spingere le cellule attraverso la fase G1, confermando che la SUMOilazione non è solo decorativa ma funzionalmente importante. Allo stesso tempo, il silenziamento di PIAS4 rendeva CDK6 più stabile ma paradossalmente meno attivo: un marcatore fosforilico inibitorio su CDK6 aumentava e la sua associazione con la proteina attivatrice ciclina D1 si indeboliva. Saggi biochimici hanno mostrato che, nonostante una maggiore quantità di proteina CDK6, le cellule con basso PIAS4 avevano una minore attività enzimatica di CDK6, sottolineando che come CDK6 viene modificato e con chi si lega conta più della sua semplice quantità.
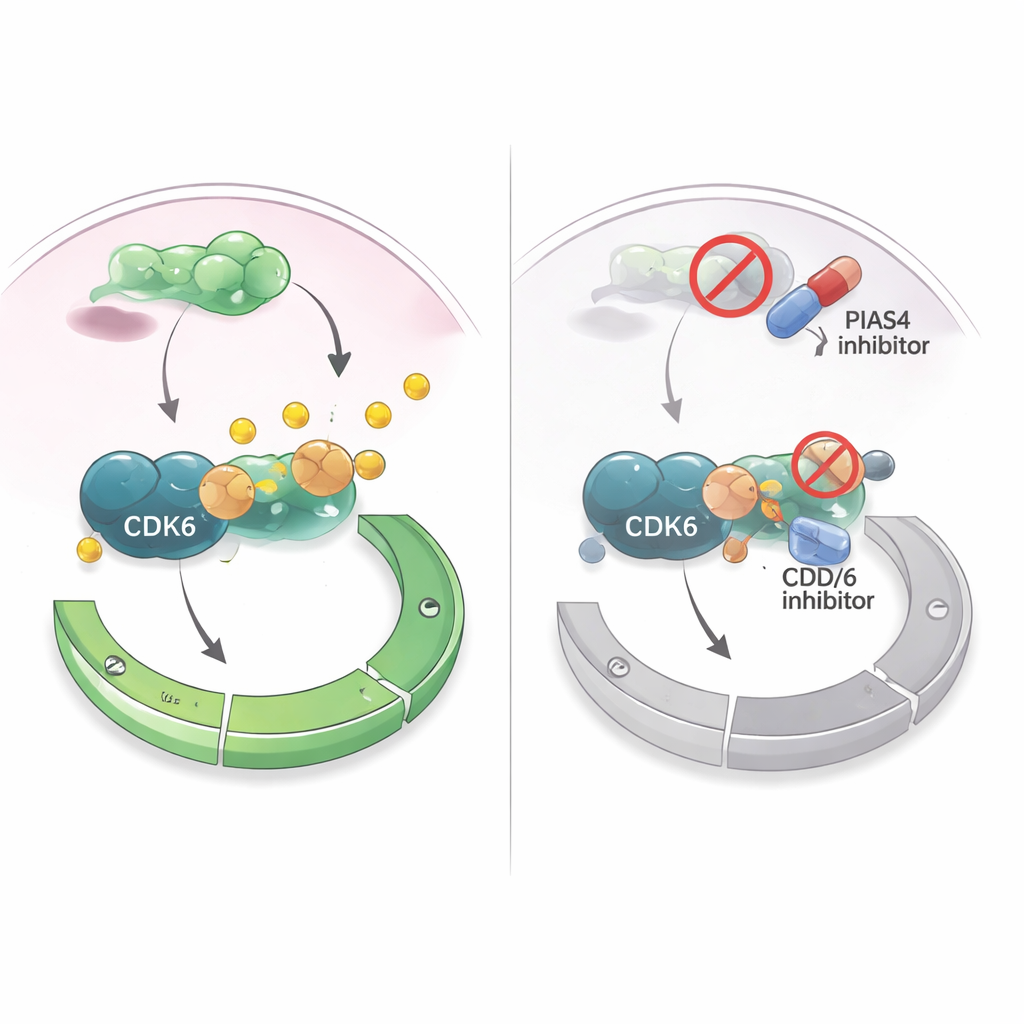
Trasformare una debolezza in una strategia terapeutica
Poiché i farmaci che inibiscono CDK4/6 sono già ampiamente usati nel cancro al seno positivo per recettori ormonali, gli autori si sono chiesti se mirare a PIAS4 potesse potenziare questi trattamenti. In cellule di cancro al seno in coltura, un farmaco che interferisce in modo ampio con la SUMOilazione (compresa l'azione di PIAS4) ha reso gli inibitori di CDK4/6 più efficaci nel sopprimere la crescita cellulare. In modelli murini in cui cellule tumorali mammarie sono state impiantate nel tessuto mammario, la riduzione contemporanea di PIAS4 e CDK6 ha ridotto i tumori più di quanto facesse il blocco di CDK6 da solo, senza danni evidenti agli animali. Nel complesso, i risultati suggeriscono che PIAS4 agisce come un acceleratore interno per CDK6 e il controllo G1, e che disabilitare questo acceleratore potrebbe sensibilizzare i tumori agli attuali farmaci sul ciclo cellulare. Per i pazienti, ciò apre la prospettiva che future terapie che combinino inibitori di PIAS4 o della via SUMO con inibitori di CDK4/6 possano controllare meglio il cancro al seno e ritardare l'insorgere di resistenze.
Citazione: Chen, H., Hu, X., Feng, L. et al. PIAS4 inhibition induces cell cycle arrest and exhibits a synergistic effect in combination with CDK4/6 inhibitor in breast cancer treatment. Oncogene 45, 1756–1770 (2026). https://doi.org/10.1038/s41388-026-03753-5
Parole chiave: cancro al seno, ciclo cellulare, inibitori CDK4/6, SUMOilazione, PIAS4