Clear Sky Science · zh
一张 Perturb-seq 分化枢纽图揭示 KMT2A 重排急性髓性白血病的协同脆弱性
这项白血病研究的重要性
急性髓性白血病是一种进展迅速的血液癌症,常对现有的靶向药物产生耐受。许多新疗法试图关闭单一的致癌驱动,但疾病常通过适应性变化复发。该研究提出了对患者及其家庭至关重要的问题:与其一次按下一个开关,是否可以绘制出将白血病细胞困在未成熟状态的整个控制面板,并找到联合疗法可发挥远超单药效果的薄弱环节?
那些拒绝成熟的癌细胞
在这项工作中,科学家聚焦于一种高危的急性髓性白血病亚型,其特征是名为 KMT2A 的基因发生重排。在这些癌症中,造血干细胞被锁定在未成熟阶段,未能成熟为抵抗感染的白细胞。早期针对单个表观遗传调控因子的药物(这些因子类似于 DNA 包装上的化学标签)虽然显示出希望,但很少带来长期缓解。研究团队的推理是,白血病细胞之所以存活,是因为多个表观遗传系统协同工作,仅阻断其中一项通常会被其他系统弥补。为真正理解这种协作,他们需要一种方法来观察在成千上万单个细胞中逐一关闭关键调控因子时发生了什么。
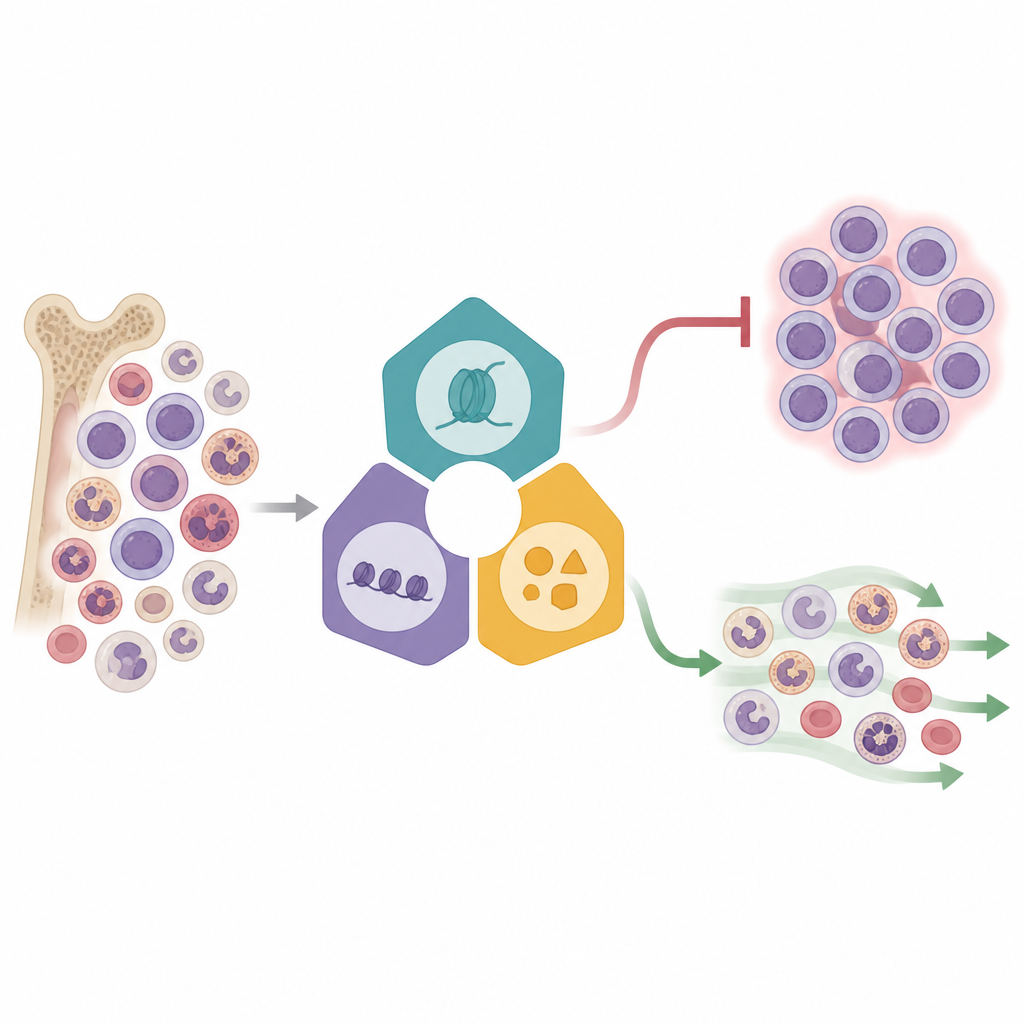
一次读取数千个细胞
研究人员使用了一种名为 Perturb-seq 的强大方法,将基因编辑与单细胞 RNA 测序结合。在一条 KMT2A 重排的白血病细胞系中,他们扰动了来自三大主要复合体的 16 个选定的表观遗传调控因子,这些复合体共同控制基因的开启或关闭。每个被编辑的细胞携带一个遗传条形码,使团队能够将特定编辑与该细胞的基因活性谱相连。通过在降维的二维空间中映射超过 31,000 个细胞,他们观察到细胞按受影响的复合体分组,显示出独特的响应模式。一些因子,尤其与 Menin—KMT2A 融合及相关酶相关的因子,引起了基因活性的大范围转变,而其他因子影响较为微妙,暗示白血病网络内部存在不同层次的控制。
有利于患者生存的隐性程序
借助计算建模,团队将复杂数据提炼为 17 个基因程序,每个程序代表一种协调的基因活性模式。其中一个程序尤为突出:一组与髓系分化相关的基因,即未成熟细胞向完全功能性白细胞分化的过程。作者将其称为“髓系程序”。该程序在接近成熟的正常骨髓细胞中最为活跃,并与定义白血病干细胞的基因呈负相关。研究者在大型患者数据集中发现,髓系程序的基线活性越高,与总体生存期更好一致性越强,特别是在那些对标准治疗通常有更好反应的患者中。这表明即使在侵袭性癌症中,也存在部分细胞更接近“准备成熟”的状态,这与较好的预后相关。
一个三部分控制枢纽及其薄弱点
分析揭示,三种调控因子 Menin、DOT1L 和 KAT6A 组成了一个功能性枢纽,协同抑制髓系程序。当这三者中的任一基因被扰动时,分化程序都会被部分激活,但只是片段式地。随后团队测试了针对每个成员的抑制剂,发现显著的协同效应。将 Menin 抑制剂与 KAT6A 抑制剂配对,或将 DOT1L 抑制剂与 KAT6A 抑制剂联用,均显著抑制了白血病细胞增殖,并相比单药强烈提高了髓系程序基因的表达。与此同时,他们还发现另一个包含 PCGF1 的复合体具有相反影响。失去 PCGF1 会使白血病细胞对 DOT1L 抑制不那么敏感,凸显出某些表观遗传因子能够削弱靶向药物的效果并促成耐药。
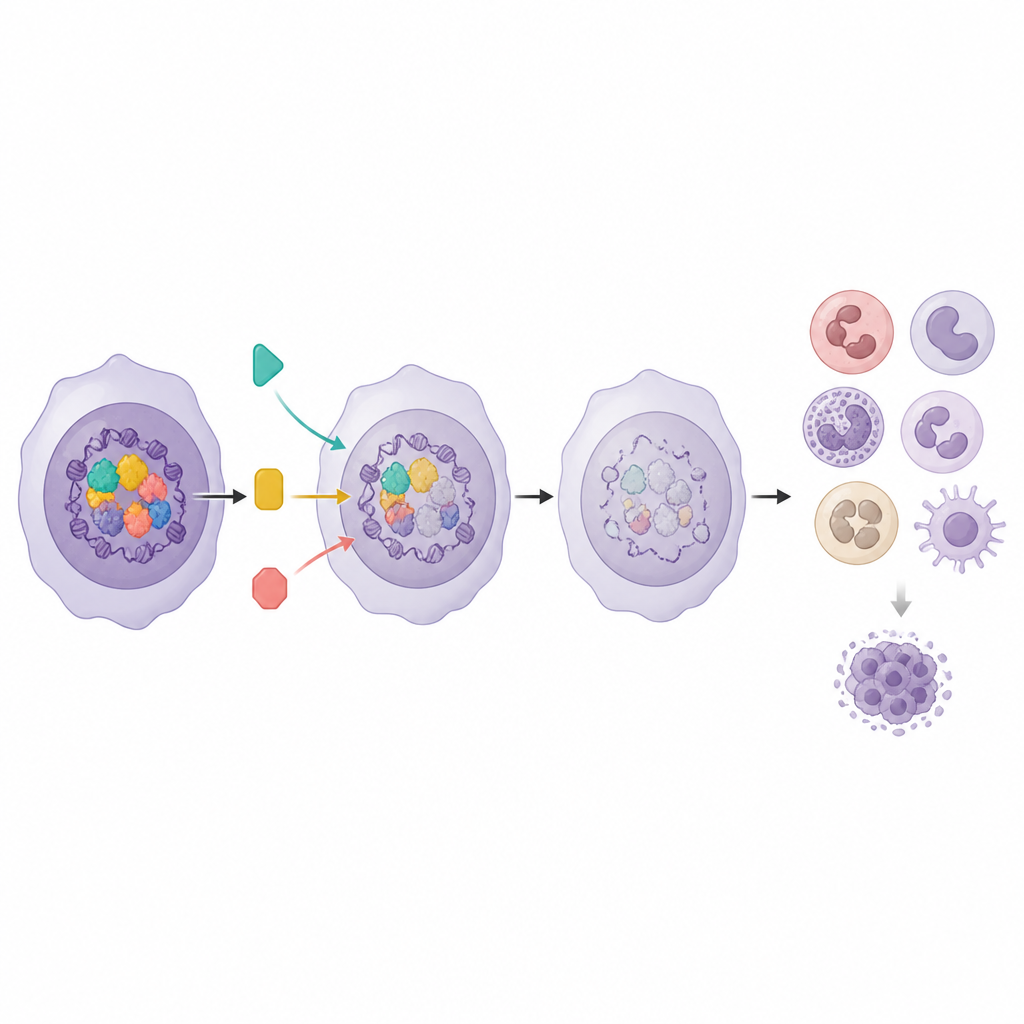
用基因活性指导智能组合用药
由于髓系程序既与细胞成熟相关又与患者生存相关,研究者进一步探问其活性是否也能预测哪些药物最有效。在患者样本中,髓系程序评分较高的白血病对若干信号通路抑制剂更为敏感,尤其是靶向 MEK、AKT 和 mTOR 的抑制剂。当团队在细胞模型中将可提升髓系程序的 Menin 抑制剂与这些通路抑制剂联合使用时,药物组合表现出明显协同,并降低了抑制白血病细胞生长所需的剂量。相同的基因程序还帮助区分出真正协作的组合与那些仅将细胞推向一种通用分化状态的组合。
这对未来白血病治疗意味着什么
对普通读者来说,关键结论是:这项研究超越了寻找单一“神奇子弹”的思路,转而绘制了多种表观遗传调控因子如何协同将白血病细胞困在有害的未成熟状态的全景图。通过识别出既能预测更好生存又能提示药物敏感性的核心髓系程序,并指出抑制该程序的三部分 Menin—KAT6A—DOT1L 枢纽,研究为合理的组合疗法提供了蓝图。长期来看,在患者体内测量髓系程序的活性可能帮助医生选择既能解除分化阻滞又能利用癌症新脆弱点的药物组合,从而有望带来更持久、更个体化的急性髓性白血病治疗策略。
引用: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
关键词: 急性髓性白血病, 表观遗传治疗, 细胞分化, 药物协同, 单细胞基因组学