Clear Sky Science · pt
Um mapa Perturb-seq de um centro de diferenciação revela vulnerabilidades sinérgicas na leucemia mieloide aguda com rearranjo de KMT2A
Por que este estudo sobre leucemia importa
A leucemia mieloide aguda é um câncer sanguíneo de progressão rápida que frequentemente resiste aos medicamentos-alvo modernos. Muitas terapias novas tentam desligar um único motor do câncer, apenas para ver a doença se adaptar e retornar. Este estudo aborda uma questão crucial para pacientes e famílias: em vez de apertar um único botão por vez, podemos mapear todo o painel de controle que mantém as células leucêmicas em um estado imaturo e então encontrar pontos fracos onde terapias combinadas funcionam muito melhor do que qualquer droga isolada?
As células cancerosas que se recusam a amadurecer
Neste trabalho, os cientistas concentram-se em uma forma de alto risco de leucemia mieloide aguda marcada por alterações em um gene chamado KMT2A. Nesses cânceres, células-tronco sanguíneas ficam congeladas em uma fase imatura em vez de amadurecer em glóbulos brancos que combatem infecções. Drogas anteriores que miravam reguladores epigenéticos individuais — que atuam como marcas químicas na embalagem do DNA — mostraram potencial, mas raramente conduziram a remissões duradouras. A equipe supôs que as células leucêmicas sobrevivem porque vários sistemas epigenéticos cooperam, de modo que bloquear apenas um deixa outros para compensar. Para compreender verdadeiramente essa cooperação, era necessário um método para observar o que acontece dentro de milhares de células individuais quando reguladores-chave são desligados uma a uma.
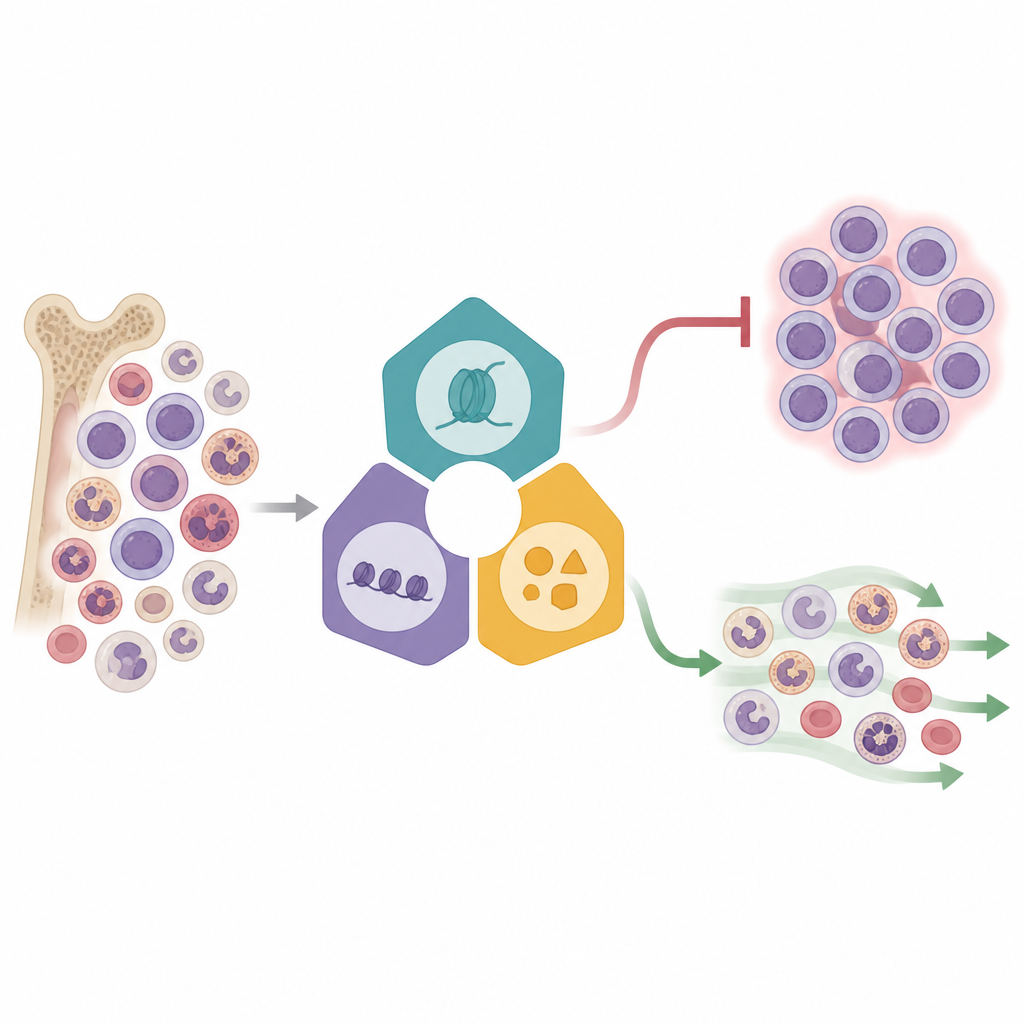
Lendo milhares de células ao mesmo tempo
Os pesquisadores usaram um método potente chamado Perturb-seq, que combina edição gênica com sequenciamento de RNA de célula única. Em uma linhagem celular de leucemia com rearranjo de KMT2A, eles perturbara m 16 reguladores epigenéticos escolhidos a partir de três complexos principais que controlam quais genes são ativados ou silenciados. Cada célula editada carregava um código de barras genético, permitindo à equipe ligar uma alteração específica ao perfil de atividade gênica daquela célula. Ao mapear mais de 31.000 células em um espaço bidimensional reduzido, observaram que as células se agrupavam conforme qual complexo havia sido atingido, revelando padrões distintos de resposta. Alguns fatores, especialmente os ligados à fusão Menin–KMT2A e enzimas relacionadas, provocaram mudanças amplas na atividade gênica, enquanto outros tiveram efeitos mais sutis, sugerindo níveis diferentes de controle dentro da rede leucêmica.
Um programa oculto que favorece a sobrevivência do paciente
Usando modelagem computacional, a equipe destilou os dados complexos em 17 programas gênicos, cada um representando um padrão coordenado de atividade gênica. Um programa sobressaiu: um conjunto de genes ligado à diferenciação mieloide, o processo pelo qual células imaturas tornam-se glóbulos brancos completamente funcionais. Os autores chamam isso de Programa Mieloide. Ele estava mais ativo em células da medula óssea normais próximas da maturação plena e mostrou uma ligação inversa com genes que definem células-tronco leucêmicas. Quando os pesquisadores examinaram grandes conjuntos de dados de pacientes, maior atividade basal do Programa Mieloide esteve consistentemente associada a melhor sobrevida global, especialmente em pacientes cuja leucemia tende a responder bem ao tratamento padrão. Isso sugere que, mesmo dentro de um câncer agressivo, algumas células estão mais próximas de um estado “pronto para maturar” associado a melhores desfechos.
Um centro de controle em três partes e seus pontos fracos
A análise revelou que três reguladores — Menin, DOT1L e KAT6A — formam um eixo funcional que, conjuntamente, mantém o Programa Mieloide reprimido. Quando qualquer um desses genes foi perturbado, o programa de diferenciação tornou-se mais ativo, mas apenas parcialmente. A equipe então testou drogas que inibem cada parceiro e descobriu sinergia marcante. Combinar um inibidor de Menin com um inibidor de KAT6A, ou um inibidor de DOT1L com um de KAT6A, reduziu fortemente o crescimento das células leucêmicas e aumentou vigorosamente a expressão dos genes do Programa Mieloide em comparação com drogas isoladas. Ao mesmo tempo, eles identificaram uma influência oposta de outro complexo contendo PCGF1. A perda de PCGF1 tornou as células leucêmicas menos sensíveis à inibição de DOT1L, destacando como alguns fatores epigenéticos podem atenuar o efeito de drogas direcionadas e contribuir para resistência.
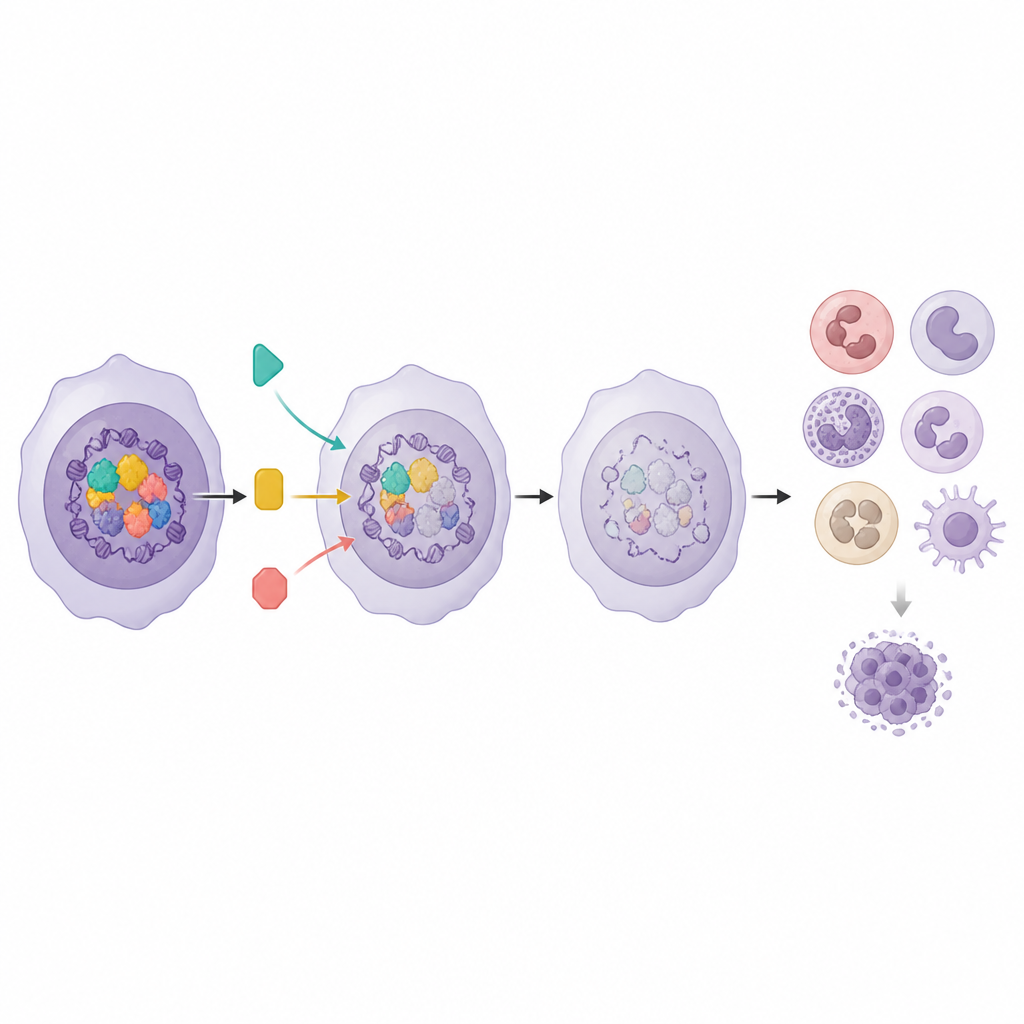
Usando atividade gênica para orientar combinações inteligentes
Porque o Programa Mieloide se relaciona tanto à maturação celular quanto à sobrevida do paciente, os pesquisadores perguntaram se sua atividade também poderia prever quais drogas funcionariam melhor. Em amostras de pacientes, leucemias com escores mais altos no Programa Mieloide foram mais sensíveis a vários inibidores de vias de sinalização, notadamente os que miram MEK, AKT e mTOR. Quando a equipe combinou um inibidor de Menin, que eleva o Programa Mieloide, com esses inibidores de vias em modelos celulares, os pares de drogas mostraram sinergia clara e reduziram as doses necessárias para controlar o crescimento das células leucêmicas. O mesmo programa gênico também ajudou a distinguir combinações que realmente cooperam daquelas que apenas empurram as células para um estado diferenciado genérico.
O que isso significa para o cuidado futuro da leucemia
Para um leitor leigo, a mensagem principal é que este estudo vai além da busca por uma única “bala de prata” e, em vez disso, mapeia como conjuntos de reguladores epigenéticos prendem conjuntamente as células leucêmicas em um estado imaturo e nocivo. Ao identificar um Programa Mieloide central que prevê tanto melhor sobrevida quanto maior sensibilidade a drogas, e ao apontar um eixo tríplice Menin–KAT6A–DOT1L que suprime esse programa, o trabalho fornece um roteiro para terapias combinadas racionais. A longo prazo, medir a atividade do Programa Mieloide em pacientes poderia ajudar médicos a escolher pares de fármacos que tanto liberem o bloqueio de maturação quanto explorem novas vulnerabilidades no câncer, potencialmente levando a tratamentos mais duradouros e personalizados para a leucemia mieloide aguda.
Citação: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Palavras-chave: leucemia mieloide aguda, terapia epigenética, diferenciação celular, sinergia medicamentosa, genômica de célula única