Clear Sky Science · ja
KMT2A再配列急性骨髄性白血病における分化ハブのPerturb‑seqマップが示す相乗的脆弱性
この白血病研究が重要な理由
急性骨髄性白血病は進行の早い血液がんで、現代の標的療法に対して耐性を示すことが多いです。多くの新薬は単一のがんドライバーを狙いますが、病態は適応して再発することが少なくありません。本研究は患者とその家族にとって重要な問いを投げかけます:ひとつずつスイッチを押すのではなく、白血病細胞を未熟な状態に閉じ込めている制御パネル全体をマップし、組み合わせ療法が単剤よりはるかに効果的に働く弱点を見つけられるか?
成長を拒むがん細胞
本研究では、KMT2Aという遺伝子の再配列で特徴づけられる高リスク型の急性骨髄性白血病に着目しています。このタイプのがんでは、造血幹細胞が感染と戦う成熟した白血球へと分化せず、未熟な段階に停滞します。DNAのパッケージに付く化学的な目印として働く個々のエピジェネティックな調節因子を標的にした先行薬は有望性を示しましたが、持続的な寛解には至ることがまれでした。研究チームは、白血病細胞が生き残るのは複数のエピジェネティックなシステムが協調しているためで、ひとつを遮断しても他が代償するからだと考えました。この協調を真に理解するには、主要な調節因子を一つずつ無効化したときに、何千もの個々の細胞内で何が起きるかを観察する方法が必要でした。
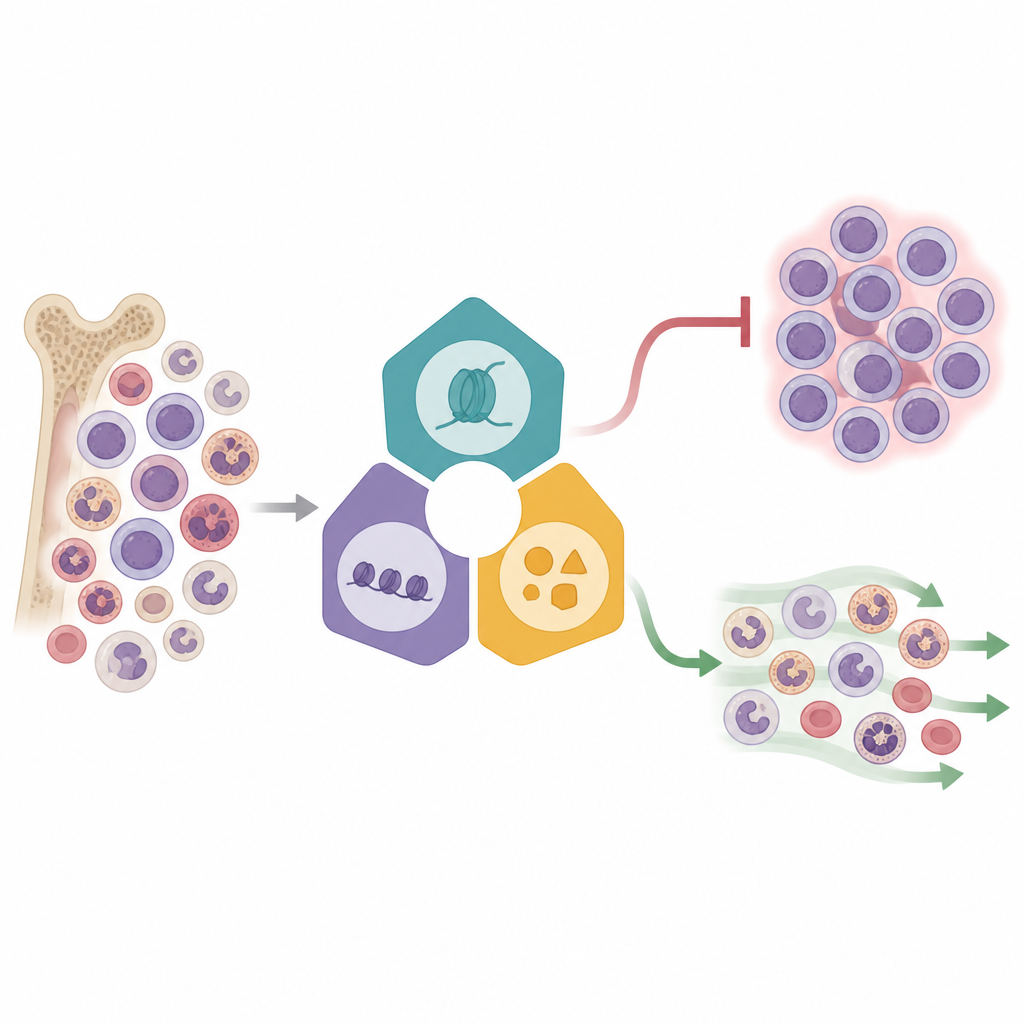
何千もの細胞を一度に読む
研究者たちは、遺伝子編集と単一細胞RNAシーケンスを組み合わせた強力な手法、Perturb‑seqを用いました。KMT2A再配列を持つ白血病細胞株で、彼らは3つの主要複合体に属する16のエピジェネティック調節因子を標的に破壊しました。各編集細胞には遺伝的バーコードが付けられ、特定の改変がその細胞の遺伝子発現プロファイルに結び付けられます。3万1千以上の細胞を2次元空間に縮約してマップすると、どの複合体が標的になったかに応じて細胞がグループ化され、反応の明確なパターンが見えました。Menin‑KMT2A融合や関連酵素に結び付く因子のいくつかは遺伝子発現に大規模な変動を引き起こした一方で、他の因子はより微妙な影響にとどまり、白血病ネットワーク内の制御に階層があることを示唆しました。
患者生存に有利に働く隠れたプログラム
計算モデルを用いて、チームは複雑なデータを17の遺伝子プログラムに集約しました。それぞれが協調した遺伝子発現のパターンを表します。その中で際立っていたのは、未熟細胞が完全に機能する白血球へと分化する過程に関連する遺伝子群、いわゆる「骨髄系プログラム(Myeloid Program)」でした。このプログラムは、成熟に近い正常骨髄細胞で最も活性化しており、白血病幹細胞を特徴づける遺伝子群とは逆相関を示しました。大規模な患者データセットを調べると、骨髄系プログラムのベースライン活性が高いことは一貫して全生存率の改善と関連し、特に標準治療に反応しやすいタイプの患者で顕著でした。これは、攻撃的ながんの中でも一部の細胞は“成熟する準備ができている”状態に近く、それがより良い転帰につながる可能性を示唆します。
三者からなる制御ハブとその弱点
解析により、Menin、DOT1L、KAT6Aの三つの調節因子が機能的ハブを形成し、骨髄系プログラムを共同で抑制していることが明らかになりました。どれか一つを破壊すると分化プログラムは活性化しますが、部分的にしか復帰しません。そこでチームは各パートナーを阻害する薬を試し、顕著な相乗効果を発見しました。Menin阻害剤とKAT6A阻害剤、あるいはDOT1L阻害剤とKAT6A阻害剤の組み合わせは、単剤に比べて白血病細胞の増殖を大きく抑え、骨髄系プログラム遺伝子の発現を強く上げました。同時に、PCGF1を含む別の複合体が逆に影響を与えることも明らかになりました。PCGF1の喪失はDOT1L阻害への感受性を低下させ、いくつかのエピジェネティック因子が標的薬の効果を鈍らせて耐性に寄与しうることを示しています。
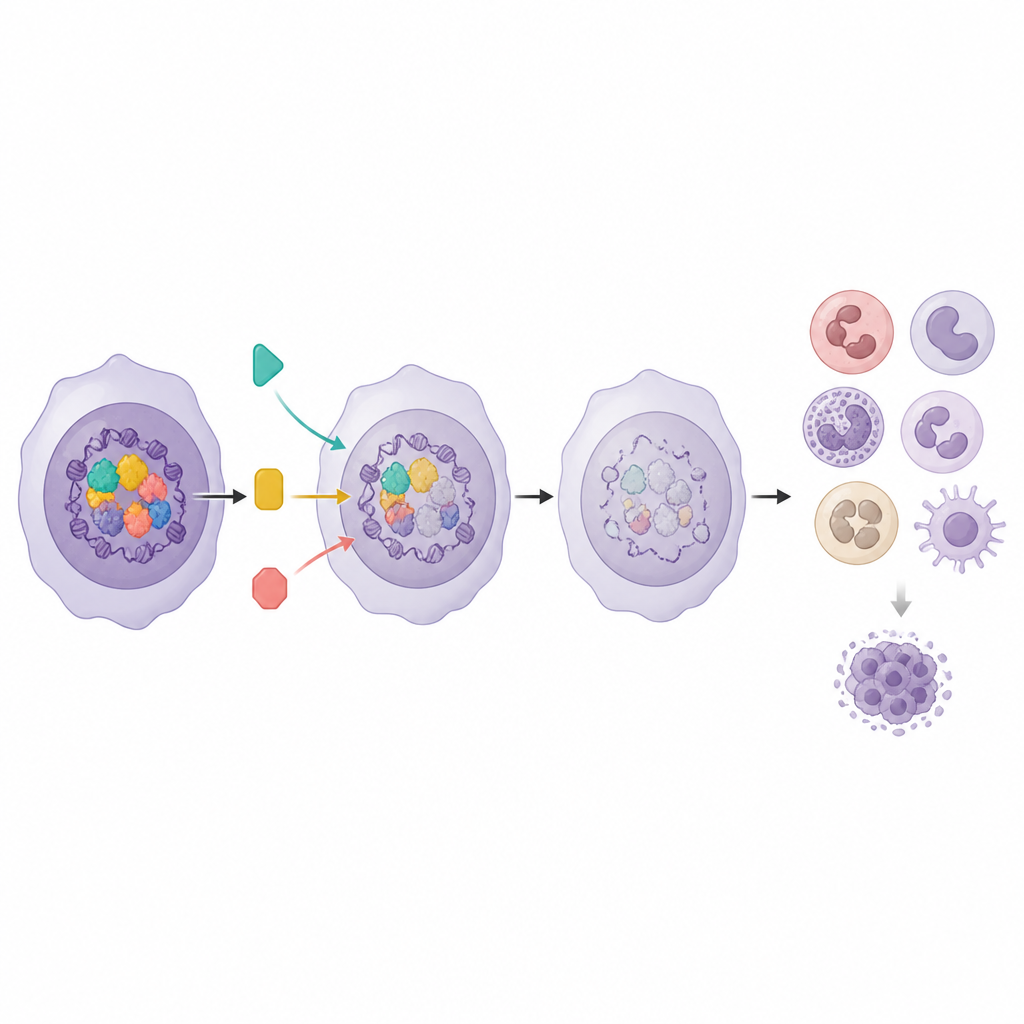
遺伝子活性を手がかりに賢い併用を選ぶ
骨髄系プログラムが細胞の成熟と患者生存の両方に結びつくことから、研究者たちはこのプログラムの活性がどの薬が最も効くかの予測に使えるかを検討しました。患者サンプルでは、骨髄系プログラムスコアが高い白血病はMEK、AKT、mTORを標的とするシグナル伝達経路阻害剤など、いくつかの阻害剤により感受性が高いことが分かりました。チームがMenin阻害剤(骨髄系プログラムを上げる)をこれらの経路阻害剤と細胞モデルで組み合わせると、薬剤の組み合わせは明瞭な相乗効果を示し、白血病細胞増殖を抑えるために必要な用量を下げました。さらに同じ遺伝子プログラムは、真に協調する組み合わせと単に細胞を一般的な分化状態へ押しやるだけの組み合わせとを見分けるのにも役立ちました。
将来の白血病治療に向けての意義
一般読者への要点は、本研究が単一の“魔法の弾丸”探索を超え、複数のエピジェネティック調節因子が協調して白血病細胞を未熟で有害な状態に閉じ込める仕組みをマップしたことです。生存と薬剤感受性の両方を予測する核となる骨髄系プログラムを特定し、このプログラムを抑えるMenin‑KAT6A‑DOT1Lの三者ハブを示したことで、合理的な併用療法の設計に向けた設計図が得られました。長期的には、患者で骨髄系プログラムの活性を測定することが、成熟ブロックを解除しつつがんの新たな脆弱性を突く薬剤ペアを医師が選ぶ手助けとなり、急性骨髄性白血病に対するより持続的で個別化された治療につながる可能性があります。
引用: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
キーワード: 急性骨髄性白血病, エピジェネティック療法, 細胞分化, 薬物相乗, 単一細胞ゲノミクス