Clear Sky Science · it
Una mappa Perturb-seq di un hub di differenziazione rivela vulnerabilità sinergiche nella leucemia mieloide acuta con riarrangiamento KMT2A
Perché questo studio sulla leucemia è importante
La leucemia mieloide acuta è un tumore del sangue ad evoluzione rapida che spesso resiste ai farmaci mirati moderni. Molti trattamenti nuovi cercano di spegnere singoli driver del cancro, per poi vedere la malattia adattarsi e tornare. Questo studio pone una domanda cruciale per pazienti e famiglie: invece di agire su un interruttore alla volta, possiamo mappare l’intero pannello di controllo che mantiene le cellule leucemiche in uno stato immaturo e identificare punti deboli dove le terapie combinate funzionano molto meglio di un singolo farmaco?
Le cellule tumorali che si rifiutano di crescere
In questo lavoro, gli scienziati si concentrano su una forma ad alto rischio di leucemia mieloide acuta caratterizzata da alterazioni in un gene chiamato KMT2A. In questi tumori, le cellule staminali ematiche restano congelate in una fase immatura invece di maturare in globuli bianchi capaci di combattere le infezioni. Farmaci precedenti che miravano a singoli regolatori epigenetici, che agiscono come marcatori chimici sull’impacchettamento del DNA, avevano mostrato potenziale ma raramente portavano a remissioni durature. Il gruppo ha ipotizzato che le cellule leucemiche sopravvivano perché diversi sistemi epigenetici cooperano: bloccarne uno lascia gli altri a compensare. Per comprendere davvero questa cooperazione serviva un modo per osservare cosa succede all’interno di migliaia di singole cellule quando i regolatori chiave vengono spenti uno per uno.
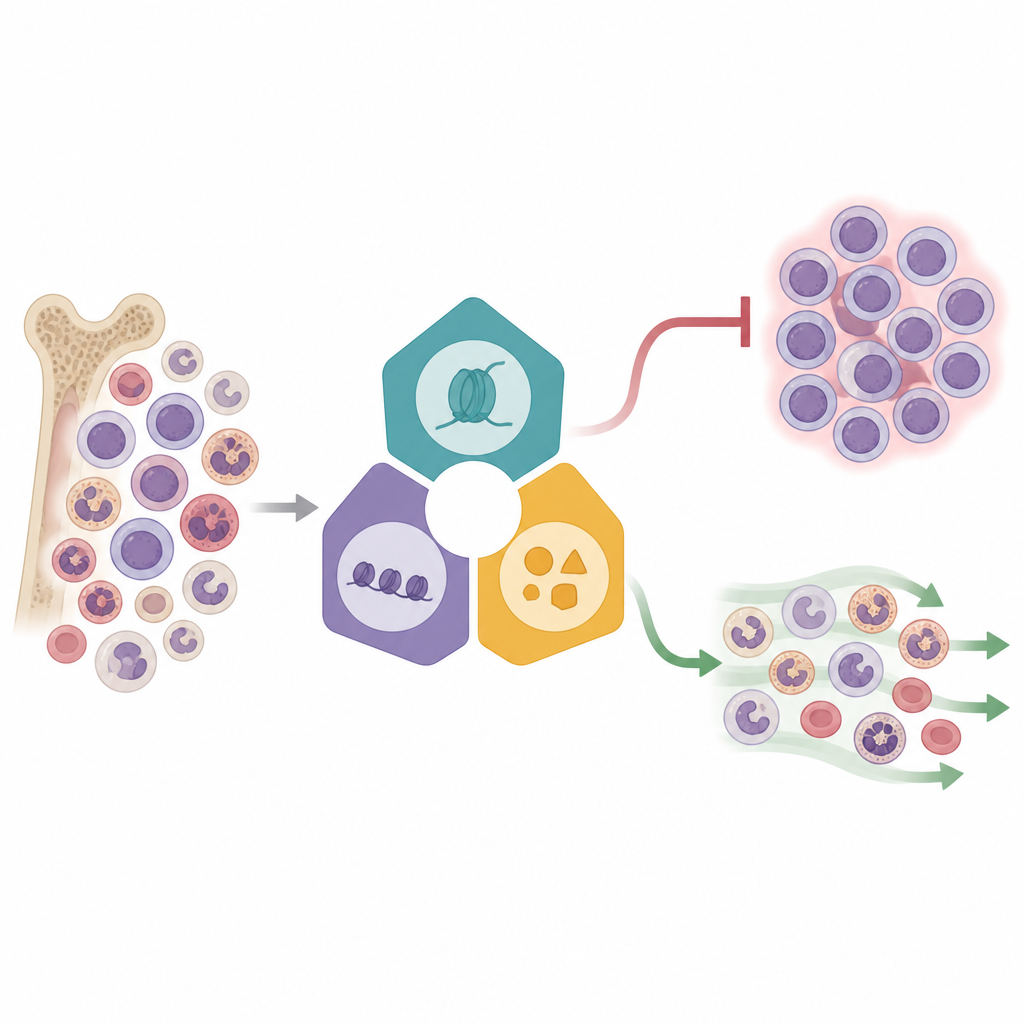
Leggere migliaia di cellule contemporaneamente
I ricercatori hanno utilizzato un metodo potente chiamato Perturb-seq, che combina editing genico con sequenziamento dell’RNA a cellula singola. In una linea cellulare leucemica con riarrangiamento KMT2A hanno perturbato 16 regolatori epigenetici scelti, provenienti da tre complessi principali che controllano l’attivazione genica. Ogni cellula modificata portava un codice a barre genetico, permettendo al team di collegare una specifica modifica al profilo di attività genica di quella cellula. Mappando oltre 31.000 cellule in uno spazio bidimensionale ridotto, hanno osservato che le cellule si raggruppavano in base al complesso colpito, rivelando distinti pattern di risposta. Alcuni fattori, in particolare quelli legati alla fusione Menin–KMT2A e agli enzimi correlati, causarono ampie variazioni nell’attività genica, mentre altri produssero effetti più sfumati, suggerendo livelli diversi di controllo nella rete leucemica.
Un programma nascosto che favorisce la sopravvivenza del paziente
Attraverso la modellizzazione computazionale, il gruppo ha distillato i dati complessi in 17 programmi genici, ciascuno rappresentante un pattern coordinato di attività genica. Un programma è emerso in modo particolare: un insieme di geni collegati alla differenziazione mieloide, il processo mediante il quale le cellule immature diventano globuli bianchi pienamente funzionali. Gli autori lo definiscono Programma Mieloide. Era più attivo nel midollo osseo normale vicino alla piena maturazione e mostrava una correlazione inversa con i geni che definiscono le cellule staminali leucemiche. Nell’analisi di grandi dataset di pazienti, un’attività di base più elevata del Programma Mieloide risultava costantemente associata a una migliore sopravvivenza complessiva, soprattutto nei pazienti la cui leucemia tende a rispondere bene al trattamento standard. Ciò suggerisce che, anche all’interno di un tumore aggressivo, alcune cellule si trovano più vicine a uno stato “pronto a maturare” collegato a esiti migliori.
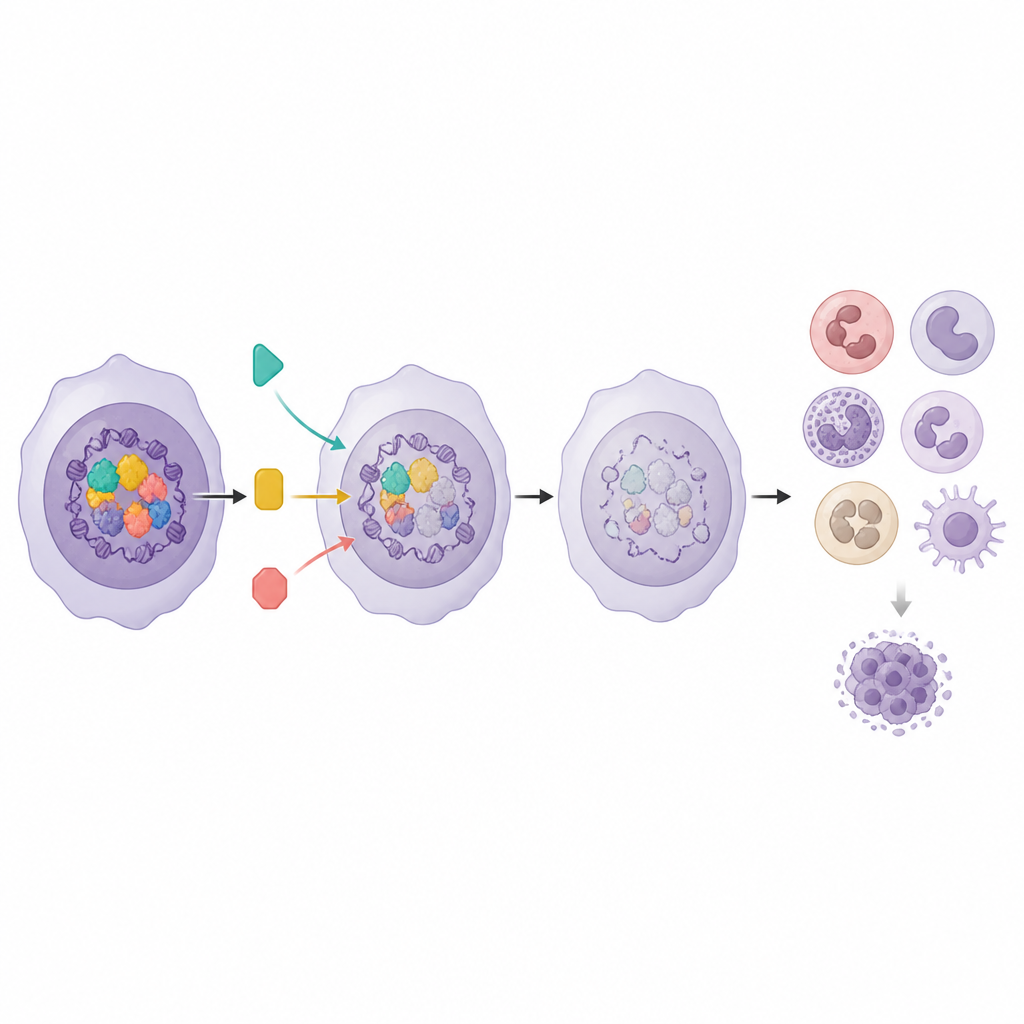
Un hub di controllo in tre parti e i suoi punti deboli
L’analisi ha rivelato che tre regolatori — Menin, DOT1L e KAT6A — formano un hub funzionale che congiuntamente mantiene il Programma Mieloide soppresso. Quando uno qualsiasi di questi geni veniva perturbato, il programma di differenziazione aumentava, ma solo parzialmente. Il team ha quindi testato farmaci che inibiscono ciascun partner e ha scoperto una sinergia notevole. L’associazione di un inibitore di Menin con un inibitore di KAT6A, oppure di un inibitore di DOT1L con un inibitore di KAT6A, riduceva nettamente la crescita delle cellule leucemiche e aumentava fortemente l’espressione dei geni del Programma Mieloide rispetto ai farmaci singoli. Allo stesso tempo è stata rilevata un’influenza opposta da un altro complesso contenente PCGF1: la perdita di PCGF1 rendeva le cellule leucemiche meno sensibili all’inibizione di DOT1L, evidenziando come alcuni fattori epigenetici possano attenuare l’effetto dei farmaci mirati e contribuire alla resistenza.
Usare l’attività genica per guidare combinazioni intelligenti
Poiché il Programma Mieloide è legato sia alla maturazione cellulare sia alla sopravvivenza dei pazienti, i ricercatori si sono chiesti se la sua attività potesse anche prevedere quali farmaci sarebbero risultati più efficaci. Nei campioni di pazienti, le leucemie con punteggi più alti del Programma Mieloide erano più sensibili a diversi inibitori di percorsi di segnalazione, in particolare quelli che prendono di mira MEK, AKT e mTOR. Quando il team combinò un inibitore di Menin, che aumenta il Programma Mieloide, con questi inibitori di percorso nei modelli cellulari, le coppie di farmaci mostrarono chiara sinergia e ridussero le dosi necessarie per contenere la crescita leucemica. Lo stesso programma genico ha anche aiutato a distinguere le combinazioni che cooperano realmente da quelle che semplicemente spingono le cellule verso uno stato differenziato generico.
Cosa significa per la cura futura della leucemia
Per il lettore non specialista, il messaggio chiave è che questo studio va oltre la ricerca di un singolo “proiettile magico” e mappa invece come gruppi di regolatori epigenetici congiuntamente intrappolino le cellule leucemiche in uno stato immaturo e dannoso. Identificando un nucleo Programma Mieloide che predice sia una migliore sopravvivenza sia una maggiore sensibilità ai farmaci, e individuando un hub tripartito Menin–KAT6A–DOT1L che sopprime questo programma, il lavoro fornisce un progetto per terapie combinate razionali. A lungo termine, misurare l’attività del Programma Mieloide nei pazienti potrebbe aiutare i medici a scegliere coppie di farmaci che rilasciano il blocco della maturazione e sfruttano nuove debolezze del tumore, portando potenzialmente a trattamenti più duraturi e personalizzati per la leucemia mieloide acuta.
Citazione: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Parole chiave: leucemia mieloide acuta, terapia epigenetica, differenziazione cellulare, sinergia farmacologica, genomica a cellula singola