Clear Sky Science · fr
Une carte Perturb‑seq d’un centre de différenciation révèle des vulnérabilités synergiques dans la leucémie myéloïde aiguë à réarrangement KMT2A
Pourquoi cette étude sur la leucémie est importante
La leucémie myéloïde aiguë est un cancer du sang rapidement évolutif qui résiste fréquemment aux médicaments ciblés modernes. De nombreux nouveaux traitements visent à fermer un unique levier oncogénique, pour voir ensuite la maladie s’adapter et récidiver. Cette étude pose une question cruciale pour les patients et leurs proches : au lieu d’actionner un interrupteur à la fois, peut‑on cartographier tout le tableau de contrôle qui maintient les cellules leucémiques dans un état immature, puis trouver des points faibles où des thérapies combinées fonctionnent bien mieux que n’importe quel médicament isolé ?
Les cellules cancéreuses qui refusent de grandir
Dans ce travail, les scientifiques se concentrent sur une forme à haut risque de leucémie myéloïde aiguë marquée par des altérations du gène KMT2A. Dans ces cancers, les cellules souches sanguines restent figées dans une phase immature au lieu de devenir des globules blancs capables de combattre les infections. Des médicaments antérieurs ciblant des régulateurs épigénétiques isolés — des « étiquettes chimiques » sur l’emballage de l’ADN — ont montré des signes d’espoir mais ont rarement entraîné des rémissions durables. L’équipe a émis l’hypothèse que les cellules leucémiques survivent parce que plusieurs systèmes épigénétiques coopèrent, de sorte que bloquer un seul élément laisse les autres compenser. Pour comprendre véritablement cette coopération, il leur fallait un moyen d’observer ce qui se passe à l’intérieur de milliers de cellules individuelles lorsque des régulateurs clés sont désactivés l’un après l’autre.
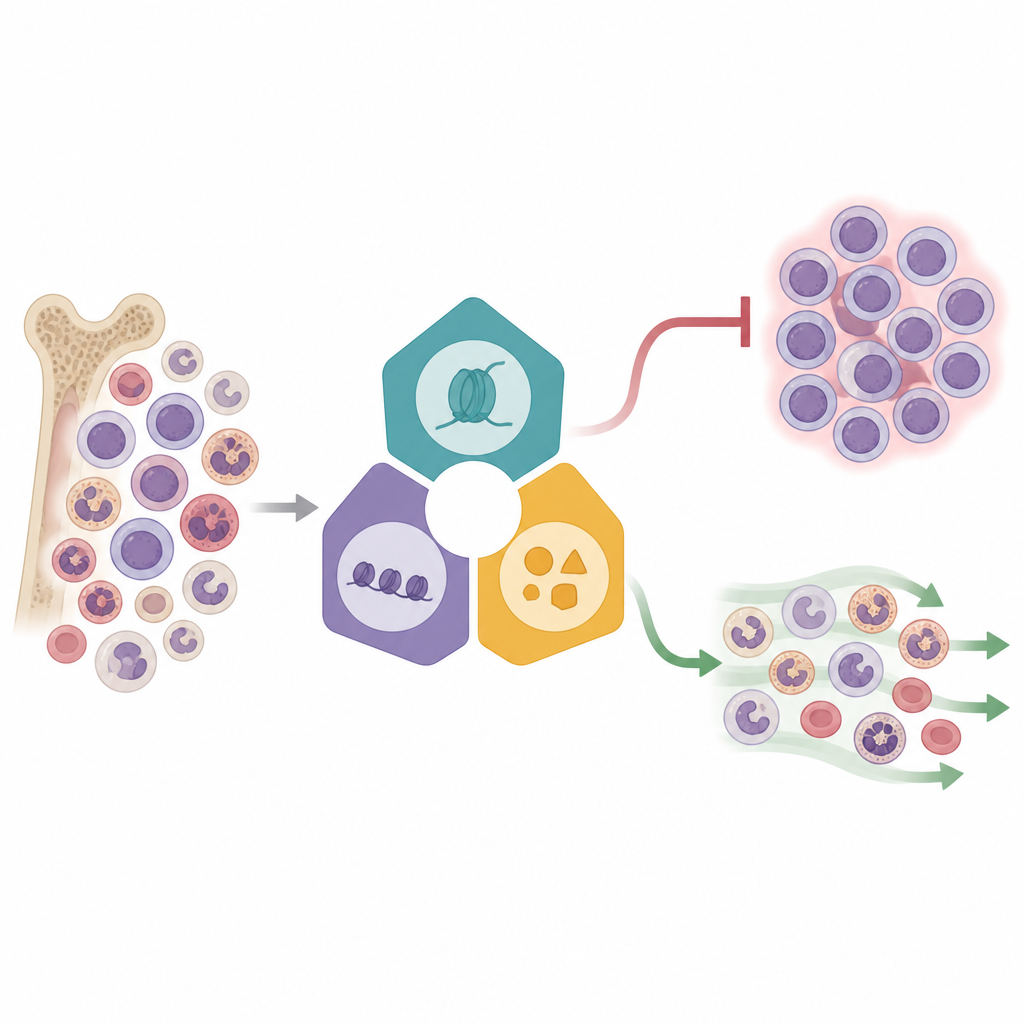
Lire des milliers de cellules en même temps
Les chercheurs ont utilisé une méthode puissante appelée Perturb‑seq, qui combine édition génique et séquençage ARN unicellulaire. Dans une lignée cellulaire leucémique avec réarrangement KMT2A, ils ont perturbé 16 régulateurs épigénétiques choisis, issus de trois complexes majeurs qui contrôlent l’activation ou la répression des gènes. Chaque cellule éditée portait un code‑barre génétique, ce qui a permis de relier une modification précise au profil d’activité génique de cette cellule. En cartographiant plus de 31 000 cellules dans un espace réduit en deux dimensions, ils ont observé que les cellules se regroupaient en fonction du complexe ciblé, révélant des schémas de réponse distincts. Certains facteurs, en particulier ceux liés à la fusion Menin–KMT2A et aux enzymes associées, provoquaient des changements massifs de l’activité génique, tandis que d’autres avaient des effets plus subtils, suggérant différents niveaux de contrôle au sein du réseau leucémique.
Un programme caché favorable à la survie des patients
À l’aide de modèles computationnels, l’équipe a distillé les données complexes en 17 programmes géniques, chacun représentant un motif coordonné d’activité génique. Un programme s’est démarqué : un ensemble de gènes liés à la différenciation myéloïde, le processus par lequel les cellules immatures deviennent des globules blancs pleinement fonctionnels. Les auteurs appellent cela le Programme Myéloïde. Il était le plus actif dans les cellules normales de la moelle osseuse proches de la maturation complète et montrait une corrélation inverse avec les gènes définissant les cellules souches leucémiques. En examinant de larges jeux de données de patients, une activité de base plus élevée du Programme Myéloïde s’associait de manière cohérente à une meilleure survie globale, notamment chez les patients dont la leucémie répond mieux aux traitements standards. Cela suggère que, même au sein d’un cancer agressif, certaines cellules sont plus proches d’un état « prêtes à maturer » lié à de meilleurs pronostics.
Un centre de contrôle en trois parties et ses points faibles
L’analyse a révélé que trois régulateurs — Menin, DOT1L et KAT6A — forment un hub fonctionnel qui réprime conjointement le Programme Myéloïde. Lorsque l’un de ces gènes était perturbé, le programme de différenciation s’activait davantage, mais seulement partiellement. L’équipe a ensuite testé des médicaments inhibiteurs de chaque partenaire et découvert une synergie marquée. L’association d’un inhibiteur de Menin avec un inhibiteur de KAT6A, ou d’un inhibiteur de DOT1L avec un inhibiteur de KAT6A, réduisait fortement la croissance des cellules leucémiques et augmentait nettement l’expression des gènes du Programme Myéloïde par rapport aux monothérapies. Parallèlement, ils ont mis au jour une influence opposée d’un autre complexe contenant PCGF1. La perte de PCGF1 rendait les cellules leucémiques moins sensibles à l’inhibition de DOT1L, soulignant comment certains facteurs épigénétiques peuvent atténuer l’effet des médicaments ciblés et contribuer à la résistance.
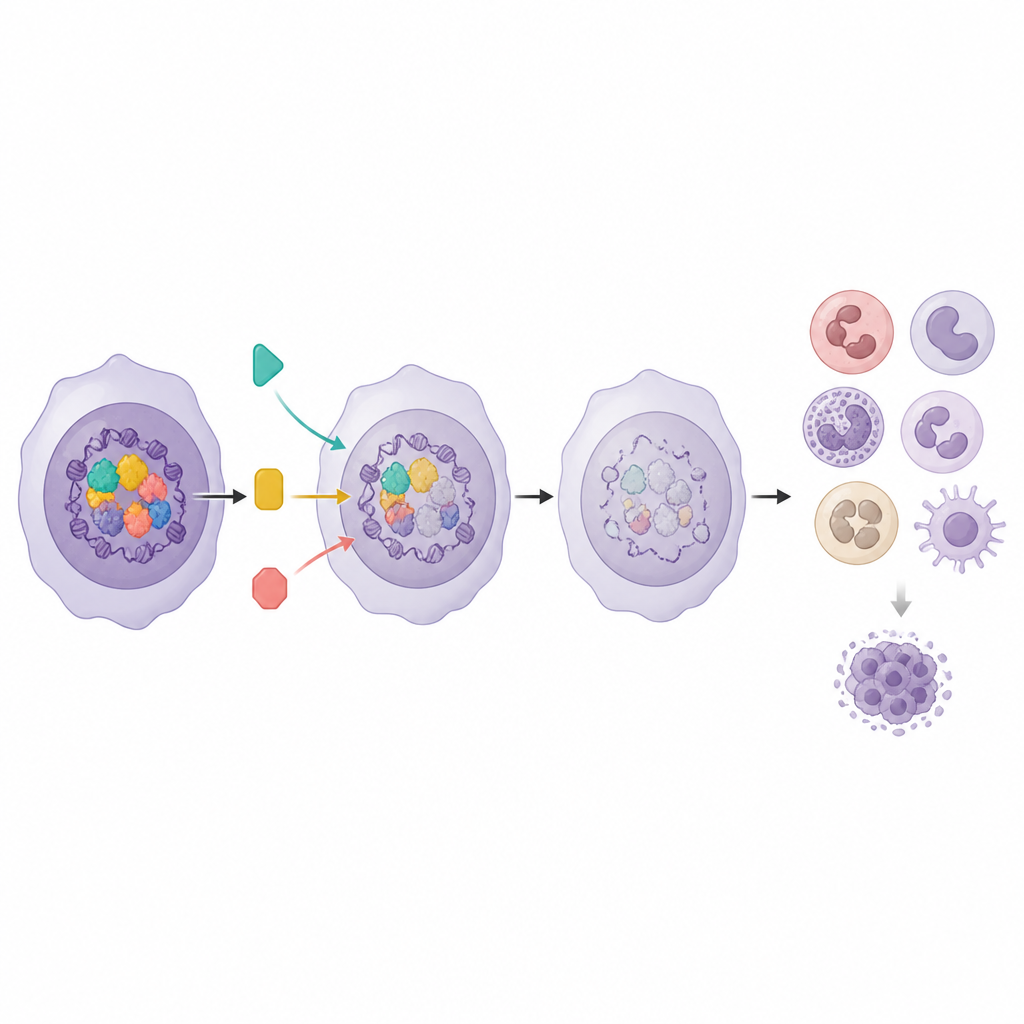
Utiliser l’activité génique pour guider des combinaisons intelligentes
Parce que le Programme Myéloïde relie maturation cellulaire et survie des patients, les chercheurs ont testé si son niveau d’activité pouvait aussi prédire quels médicaments seraient les plus efficaces. Dans des échantillons de patients, les leucémies avec des scores élevés du Programme Myéloïde étaient plus sensibles à plusieurs inhibiteurs de voies de signalisation, en particulier ceux ciblant MEK, AKT et mTOR. Lorsque l’équipe a combiné un inhibiteur de Menin, qui augmente le Programme Myéloïde, avec ces inhibiteurs de voies dans des modèles cellulaires, les paires médicamenteuses ont montré une synergie claire et ont permis de réduire les doses nécessaires pour freiner la croissance leucémique. Le même programme génique a aussi aidé à distinguer les combinaisons qui coopèrent réellement de celles qui se contentent de pousser les cellules vers un état différencié générique.
Ce que cela signifie pour la prise en charge future de la leucémie
Pour un lecteur non spécialiste, le message principal est que cette étude dépasse la quête d’une « balle magique » unique et cartographie plutôt la façon dont des groupes de régulateurs épigénétiques maintiennent conjointement les cellules leucémiques dans un état immature et nocif. En identifiant un Programme Myéloïde central qui prédit à la fois une meilleure survie et une sensibilité accrue aux médicaments, et en pinpointant un hub Menin–KAT6A–DOT1L en trois parties qui réprime ce programme, le travail fournit une feuille de route pour des thérapies combinées rationnelles. À terme, mesurer l’activité du Programme Myéloïde chez les patients pourrait aider les médecins à choisir des paires de médicaments qui libèrent le blocage de la maturation et exploitent de nouvelles faiblesses du cancer, menant potentiellement à des traitements plus durables et personnalisés pour la leucémie myéloïde aiguë.
Citation: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Mots-clés: leucémie myéloïde aiguë, thérapie épigénétique, différenciation cellulaire, synergie médicamenteuse, génomique unicellulaire