Clear Sky Science · de
Eine Perturb‑seq‑Karte eines Differenzierungs‑Zentrums legt synergetische Verwundbarkeiten bei KMT2A‑rearrangiertem akuten myeloischen Leukämie offen
Warum diese Leukämie‑Studie wichtig ist
Die akute myeloische Leukämie ist eine schnell verlaufende Blutkrebserkrankung, die oft modernen zielgerichteten Therapien widersteht. Viele neue Behandlungen zielen darauf ab, einzelne Krebs‑Treiber auszuschalten, doch die Erkrankung passt sich häufig an und kehrt zurück. Diese Studie stellt eine für Patienten und Angehörige entscheidende Frage: Anstatt einen Schalter nach dem anderen umzulegen, lässt sich das gesamte Bedienfeld kartieren, das Leukämiezellen in einem unreifen Zustand hält, und Schwachstellen finden, an denen Kombinationstherapien deutlich wirksamer sind als einzelne Wirkstoffe?
Die Krebszellen, die sich weigern, erwachsen zu werden
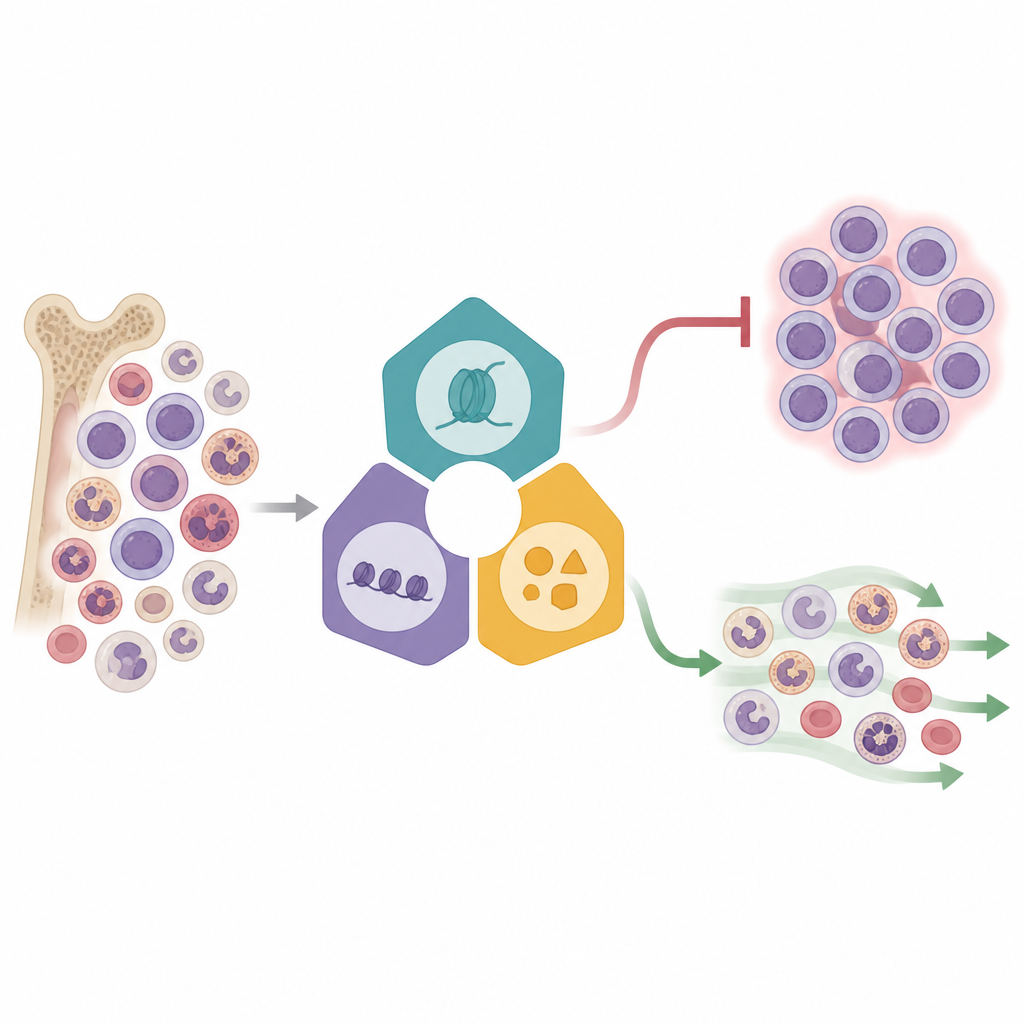
In dieser Arbeit konzentrieren sich die Wissenschaftler auf eine Hochrisiko‑Form der akuten myeloischen Leukämie, die durch Veränderungen im Gen KMT2A gekennzeichnet ist. In diesen Tumoren bleiben Blutstammzellen in einer unreifen Phase eingefroren, anstatt zu reifen und zu infektbekämpfenden weißen Blutkörperchen zu werden. Frühere Medikamente, die einzelne epigenetische Regulatoren — chemische Markierungen am DNA‑Packaging — anvisierten, zeigten vielversprechende Effekte, führten aber selten zu dauerhaften Remissionen. Das Team vermutete, dass die Leukämiezellen überleben, weil mehrere epigenetische Systeme zusammenarbeiten; das Blockieren nur eines Systems lässt die anderen die Funktion übernehmen. Um dieses Zusammenspiel wirklich zu verstehen, brauchten sie eine Methode, um zu beobachten, was in tausenden einzelnen Zellen passiert, wenn wichtige Regulatoren nacheinander ausgeschaltet werden.
Tausende Zellen auf einmal lesen
Die Forscher verwendeten eine leistungsfähige Methode namens Perturb‑seq, die Geneditierung mit Einzelzell‑RNA‑Sequenzierung kombiniert. In einer KMT2A‑rearrangierten Leukämiezelllinie störten sie 16 ausgewählte epigenetische Regulatoren aus drei großen Komplexen, die darüber entscheiden, welche Gene an‑ oder abgeschaltet werden. Jede editierte Zelle trug einen genetischen Barcode, sodass das Team eine bestimmte Veränderung mit dem Genaktivitätsprofil dieser Zelle verknüpfen konnte. Durch das Mapping von mehr als 31.000 Zellen in einem reduzierten zweidimensionalen Raum sahen sie, dass sich Zellen entsprechend dem getroffenen Komplex gruppierten und so unterschiedliche Antwortmuster offenbar wurden. Manche Faktoren, insbesondere solche im Zusammenhang mit der Menin‑KMT2A‑Fusionsachse und verwandten Enzymen, führten zu weitreichenden Verschiebungen der Genaktivität, während andere subtilere Effekte zeigten — ein Hinweis auf unterschiedliche Kontrollstufen im Leukämie‑Netzwerk.
Ein verborgenes Programm, das mit dem Überleben der Patienten zusammenhängt
Mithilfe computergestützter Modellierung reduzierte das Team die komplexen Daten auf 17 Genprogramme, von denen jedes ein koordiniertes Muster von Genaktivität repräsentiert. Eines stach hervor: eine Gruppe von Genen, die mit der myeloischen Differenzierung verknüpft sind, also dem Prozess, durch den unreife Zellen zu voll funktionsfähigen weißen Blutkörperchen werden. Die Autoren bezeichnen dies als das Myeloid‑Programm. Es war am aktivsten in normalem Knochenmark nahe der vollständigen Reifung und zeigte eine inverse Beziehung zu Genen, die Leukämie‑Stammzellen definieren. Bei der Auswertung großer Patientendatensätze war eine höhere Baseline‑Aktivität des Myeloid‑Programms konsequent mit besserem Gesamtüberleben verbunden, insbesondere bei Patientinnen und Patienten, deren Leukämie gut auf Standardtherapien anspricht. Das deutet darauf hin, dass selbst in einem aggressiven Tumor einige Zellen näher an einem „bereit zur Reifung“‑Zustand liegen, der mit besseren Ergebnissen verknüpft ist.
Ein dreiteiliges Kontrollzentrum und seine Schwachstellen
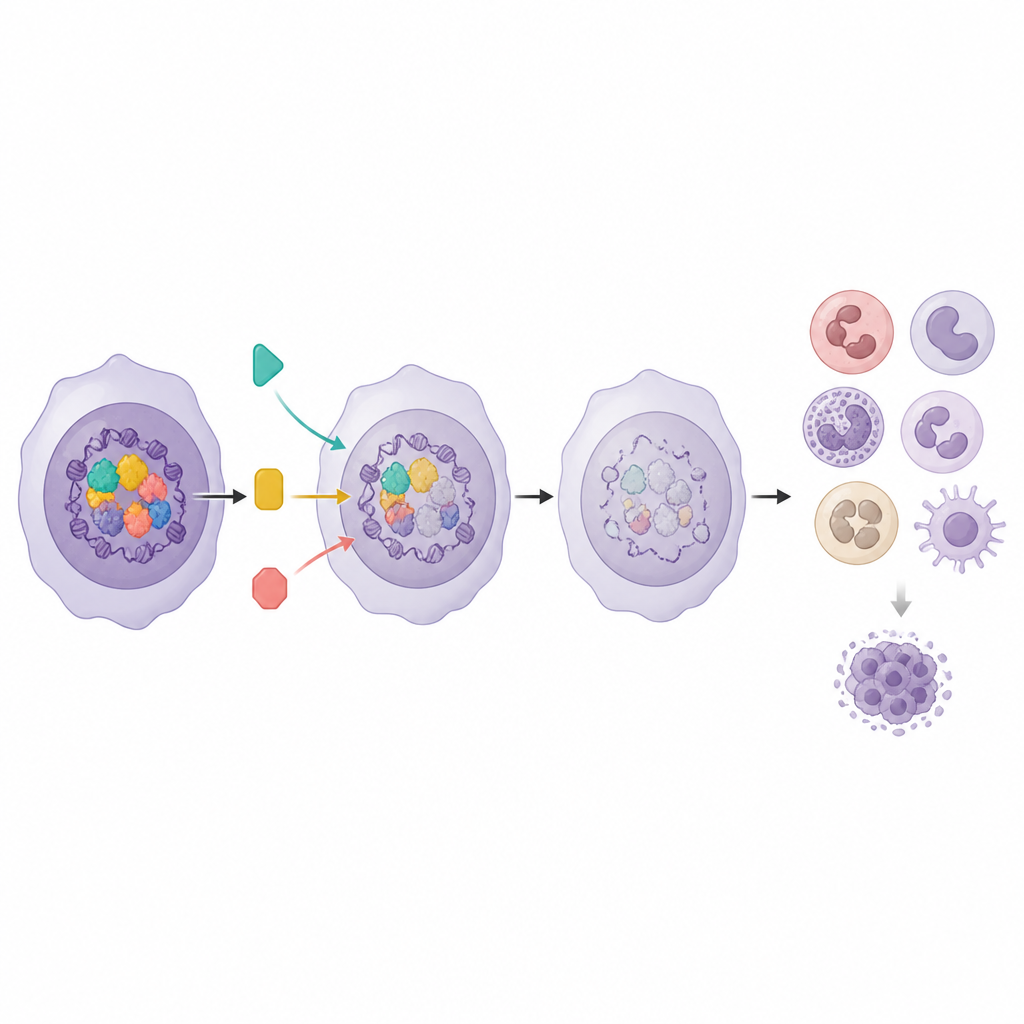
Die Analyse zeigte, dass drei Regulatoren — Menin, DOT1L und KAT6A — einen funktionellen Hub bilden, der gemeinsam das Myeloid‑Programm unterdrückt. Wenn eines dieser Gene gestört wurde, wurde das Differenzierungsprogramm aktiver, allerdings nur teilweise. Das Team testete daraufhin Wirkstoffe, die jeden Partner hemmen, und entdeckte eine auffällige Synergie. Die Kombination eines Menin‑Inhibitors mit einem KAT6A‑Inhibitor oder eines DOT1L‑Inhibitors mit einem KAT6A‑Inhibitor verringerte das Leukämiezellwachstum deutlich und steigerte die Expression der Myeloid‑Programm‑Gene stärker als Einzelwirkstoffe. Gleichzeitig fanden sie einen entgegengesetzten Einfluss eines weiteren Komplexes, der PCGF1 enthält. Der Verlust von PCGF1 machte Leukämiezellen weniger empfindlich gegenüber DOT1L‑Hemmern und zeigt, wie manche epigenetischen Faktoren die Wirkung zielgerichteter Arzneimittel abschwächen und zur Resistenz beitragen können.
Genaktivität nutzen, um kluge Kombinationen zu steuern
Weil das Myeloid‑Programm sowohl mit Zellreifung als auch mit Patient:innen‑Überleben verknüpft ist, fragten die Forscher, ob seine Aktivität auch vorhersagen könnte, welche Medikamente am besten wirken. In Patientenproben waren Leukämien mit höheren Myeloid‑Programm‑Werten empfindlicher gegenüber mehreren Inhibitoren von Signalwegen, vor allem solchen, die MEK, AKT und mTOR anvisieren. Wenn das Team in Zellmodellen einen Menin‑Inhibitor, der das Myeloid‑Programm anhebt, mit diesen Signalweg‑Inhibitoren kombinierte, zeigten die Wirkstoffpaare klare Synergien und senkten die benötigten Dosen, um das Leukämiezellwachstum zu hemmen. Dasselbe Genprogramm half dabei, Kombinationen zu unterscheiden, die wirklich kooperieren, von solchen, die Zellen nur in einen allgemein differenzierten Zustand treiben.
Was das für die zukünftige Leukämie‑Behandlung bedeutet
Für eine nicht‑fachliche Leserschaft lautet die Kernbotschaft: Diese Studie geht über die Suche nach einer einzelnen „Wunderwaffe“ hinaus und kartiert stattdessen, wie Gruppen epigenetischer Regulatoren gemeinsam Leukämiezellen in einem unreifen, schädlichen Zustand festhalten. Indem sie ein zentrales Myeloid‑Programm identifizieren, das sowohl besseres Überleben als auch erhöhte Wirkstoffsensitivität vorhersagt, und einen dreiteiligen Menin‑KAT6A‑DOT1L‑Hub, der dieses Programm unterdrückt, liefert die Arbeit eine Blaupause für rationale Kombinationstherapien. Langfristig könnte das Messen der Myeloid‑Programm‑Aktivität bei Patientinnen und Patienten Ärztinnen und Ärzten helfen, Wirkstoffpaare auszuwählen, die sowohl die Reifungsblockade lösen als auch neue Schwachstellen im Tumor ausnutzen — mit dem Ziel dauerhafterer und personalisierterer Behandlungen der akuten myeloischen Leukämie.
Zitation: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Schlüsselwörter: akute myeloische Leukämie, epigenetische Therapie, Zelldifferenzierung, Wirkstoffsynergie, Einzelzell‑Genomik