Clear Sky Science · pl
Mapa Perturb-seq centrali różnicowania ujawnia synergistyczne wrażliwości w ostrej białaczce szpikowej z rearanżacją KMT2A
Dlaczego to badanie białaczki ma znaczenie
Ostra białaczka szpikowa to szybko postępujący nowotwór krwi, który często opiera się współczesnym lekom ukierunkowanym. Wiele nowych terapii próbuje wyłączyć pojedyncze czynniki napędzające nowotwór, tylko po to, by choroba przystosowała się i powróciła. To badanie stawia kluczowe pytanie dla pacjentów i rodzin: zamiast naciskać pojedyncze przełączniki jeden po drugim, czy możemy zmapować cały panel sterujący, który utrzymuje komórki białaczkowe w stanie niedojrzałym, a następnie znaleźć słabe punkty, gdzie terapie skojarzone działają znacznie lepiej niż pojedynczy lek?
Komórki nowotworowe, które odmawiają dorastania
W tej pracy naukowcy koncentrują się na wysokiego ryzyka postaci ostrej białaczki szpikowej oznaczonej zmianami w genie KMT2A. W tych nowotworach komórki macierzyste krwi są zamrożone w niedojrzałej fazie zamiast dojrzewać do białych krwinek zwalczających infekcje. Wcześniejsze leki celujące pojedyncze regulatory epigenetyczne, które działają jak chemiczne znaczniki na opakowaniu DNA, dawały obiecujące wyniki, ale rzadko prowadziły do trwałych remisji. Zespół uznał, że komórki białaczkowe przetrwają, ponieważ kilka systemów epigenetycznych współpracuje, więc zablokowanie tylko jednego pozostawia pozostałym możliwość wyrównania. Aby naprawdę zrozumieć tę współpracę, potrzebowali sposobu obserwacji, co dzieje się wewnątrz tysięcy pojedynczych komórek, gdy kluczowe regulatory są wyłączane jeden po drugim.
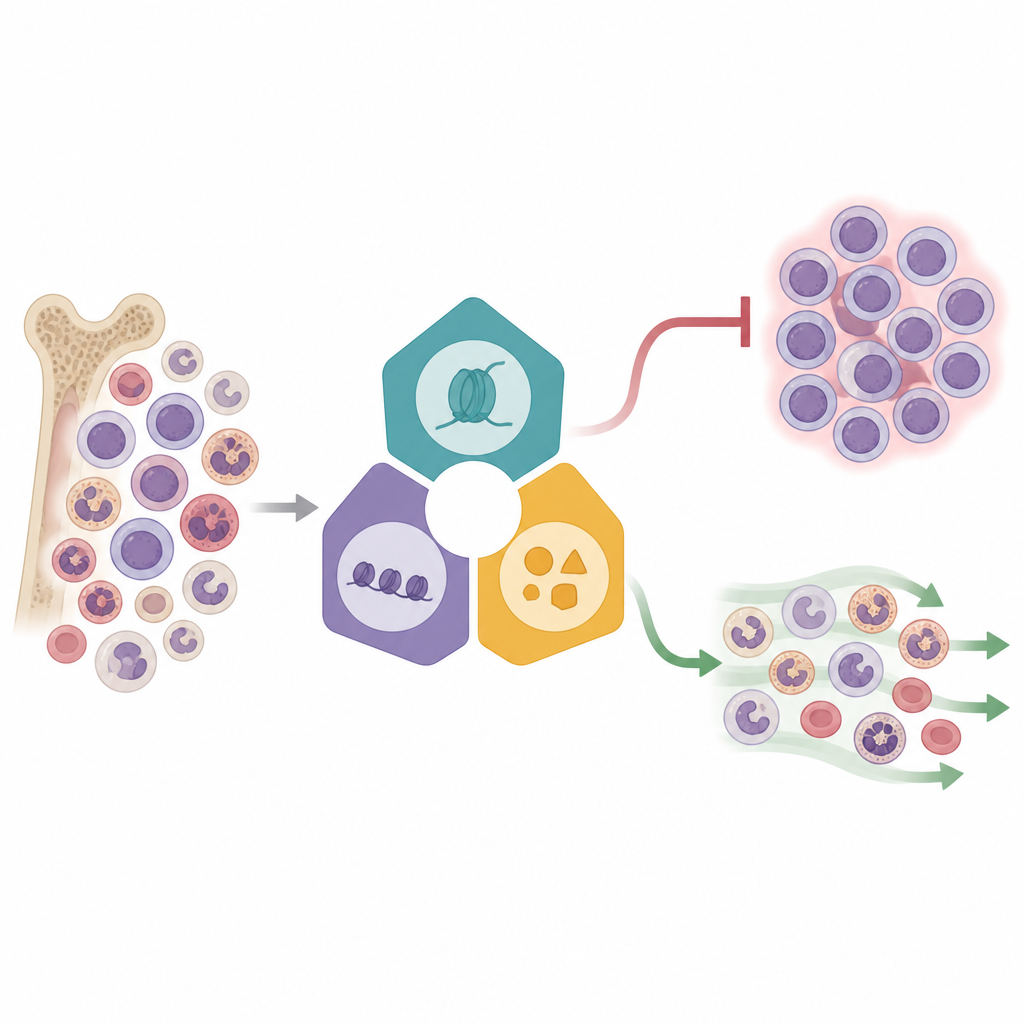
Odczytywanie tysięcy komórek naraz
Naukowcy użyli potężnej metody zwanej Perturb-seq, łączącej edycję genów z sekwencjonowaniem RNA pojedynczych komórek. W linii komórkowej białaczki z rearanżacją KMT2A wyłączyli 16 wybranych regulatorów epigenetycznych pochodzących z trzech głównych kompleksów kontrolujących, które geny są włączane lub wyłączane. Każda zmodyfikowana komórka niosła kod kreskowy genetyczny, co pozwoliło zespołowi powiązać konkretną modyfikację z profilem aktywności genów tej komórki. Mapując ponad 31 000 komórek w zredukowanej dwuwymiarowej przestrzeni, zaobserwowali, że komórki grupują się zgodnie z tym, który kompleks został uderzony, ujawniając odrębne wzorce odpowiedzi. Niektóre czynniki, zwłaszcza te związane z fuzją Menin–KMT2A i powiązanymi enzymami, powodowały szerokie przesunięcia w aktywności genów, podczas gdy inne miały subtelniejsze efekty, sugerując różne poziomy kontroli w sieci białaczkowej.
Ukryty program sprzyjający przeżyciu pacjenta
Za pomocą modelowania komputerowego zespół sprowadził złożone dane do 17 programów genowych, z których każdy reprezentował skoordynowany wzorzec aktywności genów. Jeden program wyróżniał się: zestaw genów powiązanych z różnicowaniem mieloidalnym, procesem, w którym niedojrzałe komórki stają się w pełni funkcjonalnymi białymi krwinkami. Autorzy nazywają to Programem Mieloidalnym. Był on najbardziej aktywny w normalnych komórkach szpiku kostnego bliskich pełnemu dojrzeniu i wykazywał odwrotną zależność z genami definiującymi komórki macierzyste białaczki. Gdy badacze przeanalizowali duże zbiory danych pacjentów, wyższa wyjściowa aktywność Programu Mieloidalnego konsekwentnie wiązała się z lepszym przeżyciem ogólnym, szczególnie u pacjentów, których białaczka zwykle odpowiada na standardowe leczenie. Sugeruje to, że nawet w agresywnym nowotworze niektóre komórki znajdują się bliżej stanu „gotowości do dojrzewania”, co wiąże się z lepszymi wynikami.
Trzyczęściowa centrala kontrolna i jej słabe punkty
Analiza wykazała, że trzej regulatorzy — Menin, DOT1L i KAT6A — tworzą funkcjonalną centralę, która wspólnie utrzymuje Program Mieloidalny stłumiony. Gdy którykolwiek z tych genów został wyłączony, program różnicowania stawał się bardziej aktywny, ale tylko częściowo. Zespół przetestował następnie leki hamujące każdego z partnerów i odkrył uderzającą synergię. Połączenie inhibitora Menin z inhibitorem KAT6A lub inhibitora DOT1L z inhibitorem KAT6A wyraźnie zmniejszało wzrost komórek białaczkowych i silnie zwiększało ekspresję genów Programu Mieloidalnego w porównaniu z pojedynczymi lekami. Równocześnie ujawnili przeciwstawny wpływ innego kompleksu zawierającego PCGF1. Utrata PCGF1 uczyniła komórki białaczkowe mniej wrażliwymi na inhibicję DOT1L, co podkreśla, jak niektóre czynniki epigenetyczne mogą łagodzić działanie leków celowanych i przyczyniać się do oporności.
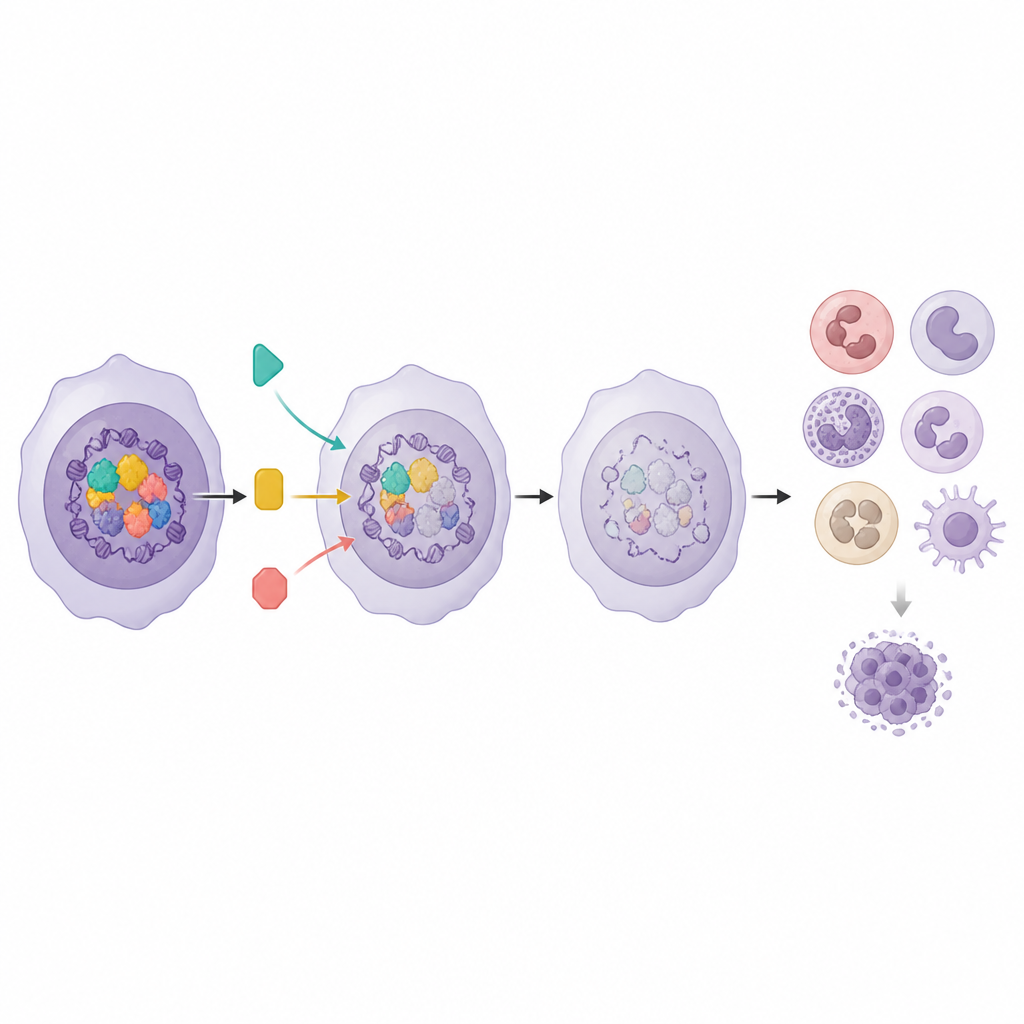
Wykorzystywanie aktywności genów do wyboru inteligentnych kombinacji
Ponieważ Program Mieloidalny wiąże się zarówno z dojrzewaniem komórek, jak i przeżyciem pacjentów, badacze zapytali, czy jego aktywność może również przewidzieć, które leki będą najskuteczniejsze. W próbkach pacjentów białaczki o wyższych wynikach Programu Mieloidalnego były bardziej wrażliwe na kilka inhibitorów szlaków sygnałowych, zwłaszcza ukierunkowanych na MEK, AKT i mTOR. Gdy zespół połączył inhibitor Menin, który podnosi aktywność Programu Mieloidalnego, z tymi inhibitorami szlaków w modelach komórkowych, pary leków wykazały wyraźną synergię i obniżyły dawki potrzebne do zahamowania wzrostu komórek białaczkowych. Ten sam program genowy pomógł też rozróżnić kombinacje, które rzeczywiście współpracują, od tych, które jedynie przesuwają komórki w kierunku ogólnego, niespecyficznego stanu zróżnicowania.
Co to oznacza dla przyszłej opieki nad białaczką
Dla czytelnika niezwiązanego z nauką kluczowe przesłanie jest takie: to badanie idzie dalej niż poszukiwanie pojedynczej „magic bullet” i zamiast tego mapuje, jak grupy regulatorów epigenetycznych wspólnie utrzymują komórki białaczkowe w niedojrzałym, szkodliwym stanie. Identyfikując rdzeniowy Program Mieloidalny, który przewiduje zarówno lepsze przeżycie, jak i zwiększoną wrażliwość na leki, oraz wskazując trzyczęściową centralę Menin–KAT6A–DOT1L tłumiącą ten program, praca dostarcza planu dla racjonalnych terapii skojarzonych. W dłuższej perspektywie mierzenie aktywności Programu Mieloidalnego u pacjentów mogłoby pomóc lekarzom w doborze par leków, które jednocześnie usuwają blokadę dojrzewania i wykorzystują nowe słabości nowotworu, co potencjalnie prowadzi do trwalszych i spersonalizowanych terapii ostrej białaczki szpikowej.
Cytowanie: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Słowa kluczowe: ostra białaczka szpikowa, terapia epigenetyczna, różnicowanie komórek, synergia leków, genomika pojedynczych komórek