Clear Sky Science · sv
En Perturb-seq-karta över en differentieringsnav avslöjar synergistiska sårbarheter i KMT2A-omlagrad akut myeloisk leukemi
Varför denna leukemistudie är viktig
Akut myeloisk leukemi är en snabbt framskridande blodcancer som ofta står emot moderna riktade läkemedel. Många nya behandlingar försöker stänga av enskilda cancerdrivare, för att se sjukdomen anpassa sig och återkomma. Denna studie ställer en avgörande fråga för patienter och familjer: i stället för att slå på en brytare i taget, kan vi kartlägga hela kontrollpanelen som håller leukemiceller fångade i ett omoget tillstånd, och sedan hitta svaga punkter där kombinationsterapier fungerar långt bättre än något enskilt läkemedel?
De cancerceller som vägrar växa upp
I detta arbete fokuserar forskarna på en högriskform av akut myeloisk leukemi som kännetecknas av förändringar i en gen kallad KMT2A. I dessa cancerformer är blodstamceller frysta i en omogen fas i stället för att mogna till infektionbekämpande vita blodkroppar. Tidigare läkemedel som riktar in sig på individuella epigenetiska regulatorer, som fungerar som kemiska markörer på DNA-packning, visade lovande resultat men led sällan till bestående remissioner. Gruppen antog att leukemicellerna överlever därför att flera epigenetiska system samarbetar, så att blockering av bara en lämnar andra att ta över. För att verkligen förstå detta samspel behövde de ett sätt att se vad som händer inne i tusentals enskilda celler när nyckelregulatorer slås av en efter en.
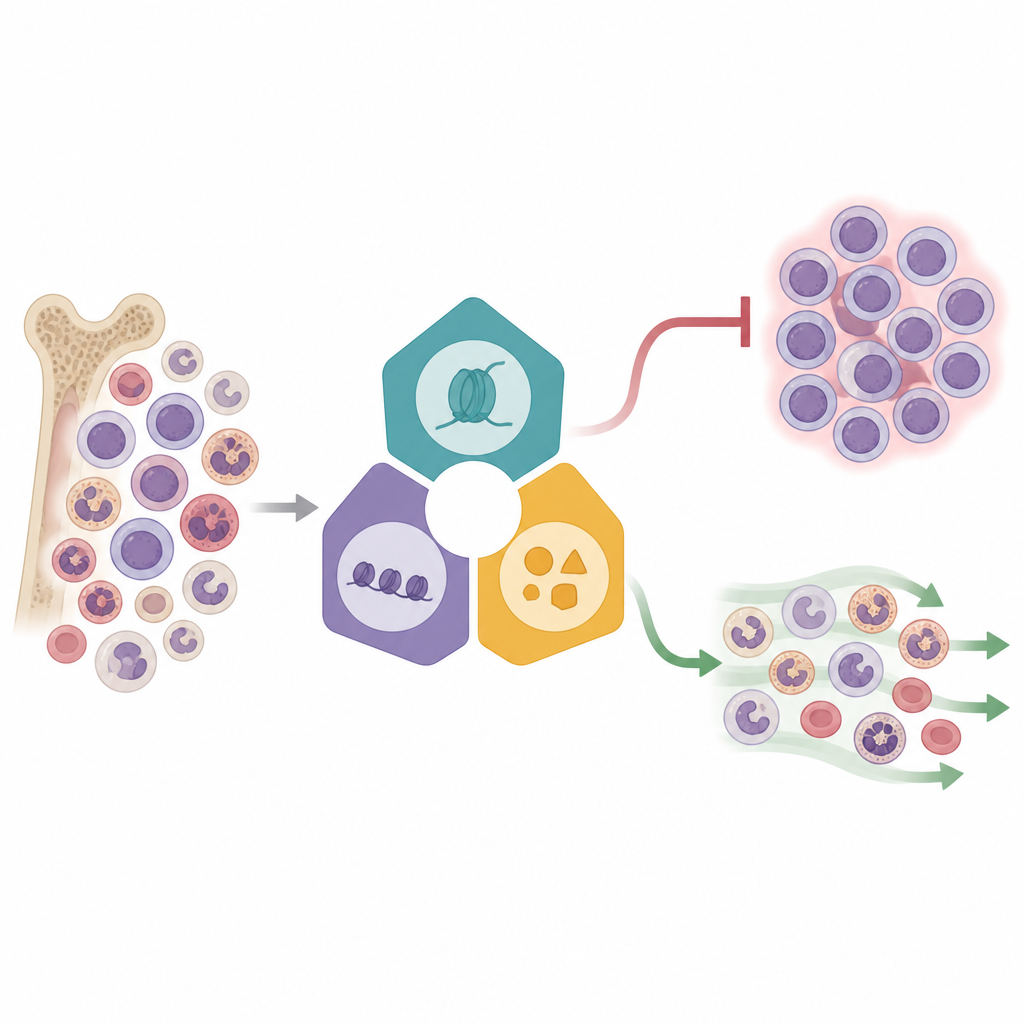
Läsa tusentals celler på en gång
Forskarna använde en kraftfull metod kallad Perturb-seq, som kombinerar genredigering med encells-RNA-sekvensering. I en KMT2A-omlagrad leukemicellinje störde de 16 utvalda epigenetiska regulatorer hämtade från tre stora komplex som styr vilka gener som är på eller av. Varje redigerad cell bar en genetisk streckkod, vilket gjorde det möjligt för teamet att koppla en specifik redigering till cellens genaktivitetsprofil. Genom att kartlägga mer än 31 000 celler i ett reducerat tvådimensionellt rum såg de att cellerna grupperade sig beroende på vilket komplex som slogs ut, vilket avslöjade distinkta responsmönster. Några faktorer, särskilt de kopplade till Menin–KMT2A-fusionen och relaterade enzymer, orsakade genomgripande skiftningar i genaktiviteten, medan andra hade mer subtila effekter, vilket antyder olika kontrollnivåer inom leukeminätverket.
Ett dolt program som gynnar patientöverlevnad
Med hjälp av beräkningsmodellering destillerade teamet de komplexa data till 17 genprogram, där varje program representerade ett samordnat mönster av genaktivitet. Ett program stack ut: en uppsättning gener kopplade till myeloid differentiering, processen där omogna celler blir fullt funktionella vita blodkroppar. Författarna kallar detta Myeloid Program. Det var mest aktivt i normal benmärgsceller som ligger nära full mognad och visade ett omvänt samband med gener som definierar leukemistamceller. När forskarna granskade stora patientdatamängder var högre basaktivitet i Myeloid Program konsekvent förknippad med bättre totalöverlevnad, särskilt hos patienter vars leukemi tenderar att svara väl på standardbehandling. Detta tyder på att även inom en aggressiv cancer finns celler som ligger närmare ett ”redo att mogna”-tillstånd som är kopplat till bättre utfall.
En treparts kontrollnav och dess svaga punkter
Analysen visade att tre regulatorer — Menin, DOT1L och KAT6A — bildar ett funktionellt nav som gemensamt håller Myeloid Program nedtonat. När någon av dessa gener stördes blev differentieringsprogrammet mer aktivt, men bara delvis. Teamet testade sedan läkemedel som hämmar varje partner och upptäckte en slående synergi. Kombinationen av en Menin-hämmare med en KAT6A-hämmare, eller en DOT1L-hämmare med en KAT6A-hämmare, minskade kraftigt leukemicellernas tillväxt och ökade uttrycket av Myeloid Program-gener jämfört med enskilda läkemedel. Samtidigt upptäckte de ett motsatt inflytande från ett annat komplex som innehåller PCGF1. Förlust av PCGF1 gjorde leukemiceller mindre känsliga för DOT1L-hämning, vilket framhäver hur vissa epigenetiska faktorer kan dämpa effekten av riktade läkemedel och bidra till resistens.
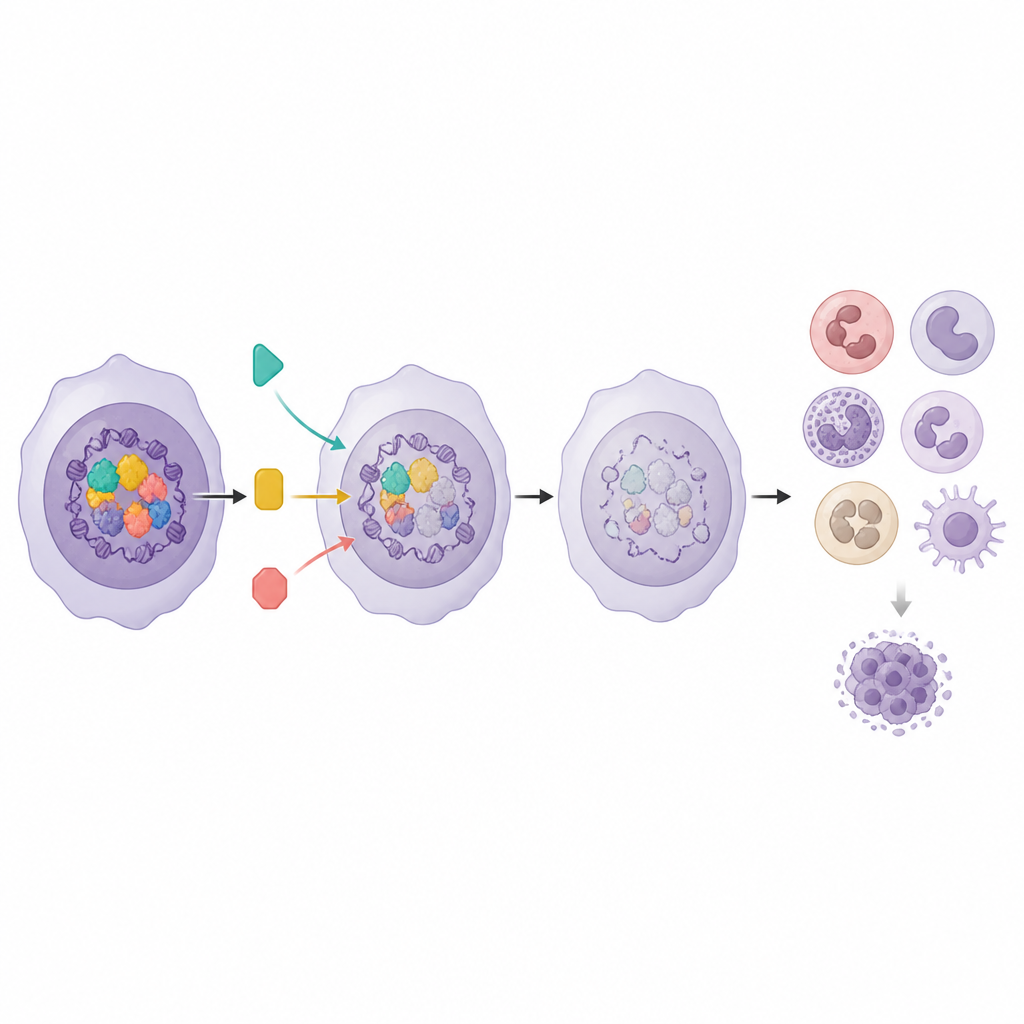
Använda genaktivitet för att vägleda smarta kombinationer
Eftersom Myeloid Program kopplas till både cellmognad och patientöverlevnad undrade forskarna om dess aktivitet också kunde förutse vilka läkemedel som skulle fungera bäst. I patientprover var leukemier med högre Myeloid Program-poäng mer känsliga för flera inhibitorer av signalvägar, framför allt de som riktar in sig på MEK, AKT och mTOR. När teamet kombinerade en Menin-hämmare, som höjer Myeloid Program, med dessa signalvägshämmare i cellmodeller visade läkemedelsparet tydlig synergi och minskade de doser som behövdes för att dämpa leukemicellernas tillväxt. Samma genprogram hjälpte också till att särskilja kombinationer som verkligen samverkar från dem som bara skjuter cellerna mot ett generellt differentierat tillstånd.
Vad detta betyder för framtida leukemivård
För en lekmannaläsare är huvudbudskapet att denna studie går bortom jakten på en enskild ”magisk kula” och i stället kartlägger hur grupper av epigenetiska regulatorer gemensamt håller leukemiceller fångade i ett omoget, skadligt tillstånd. Genom att identifiera ett kärn-Myeloid Program som förutspår både bättre överlevnad och ökad läkemedelskänslighet, och genom att peka ut ett treparts Menin–KAT6A–DOT1L-nav som undertrycker detta program, ger arbetet en ritning för rationella kombinationsterapier. På längre sikt skulle mätning av Myeloid Program-aktivitet hos patienter kunna hjälpa läkare att välja läkemedelspar som både släpper loss mognadsblocket och utnyttjar nya svagheter i cancern, vilket potentiellt kan leda till mer uthålliga och personligt anpassade behandlingar för akut myeloisk leukemi.
Citering: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Nyckelord: akut myeloisk leukemi, epigenetisk terapi, celldifferentiering, läkemedelssynergi, encellsgenomik