Clear Sky Science · ar
خريطة Perturb-seq لمركز تمايز تكشف نقاط ضعف تآزرية في سرطان الدم النخاعي الحاد مع إعادة ترتيب KMT2A
لماذا تُهم هذه الدراسة عن اللوكيميا
سرطان الدم النخاعي الحاد هو سرطان دم سريع الحركة يقاوم غالبًا الأدوية الموجهة الحديثة. تحاول العديد من العلاجات الجديدة إيقاف محفز سرطاني واحد، لكن المرض يتكيف ويعاود الظهور. تطرح هذه الدراسة سؤالًا حاسمًا للمرضى وعائلاتهم: بدلاً من الضغط على مفتاح واحد في كل مرة، هل يمكننا رسم لوحة التحكم الكاملة التي تحبس خلايا اللوكيميا في حالة غير ناضجة، ثم إيجاد نقاط ضعف حيث تعمل العلاجات المركبة أفضل بكثير من أي دواء منفرد؟
خلايا السرطان التي ترفض النضوج
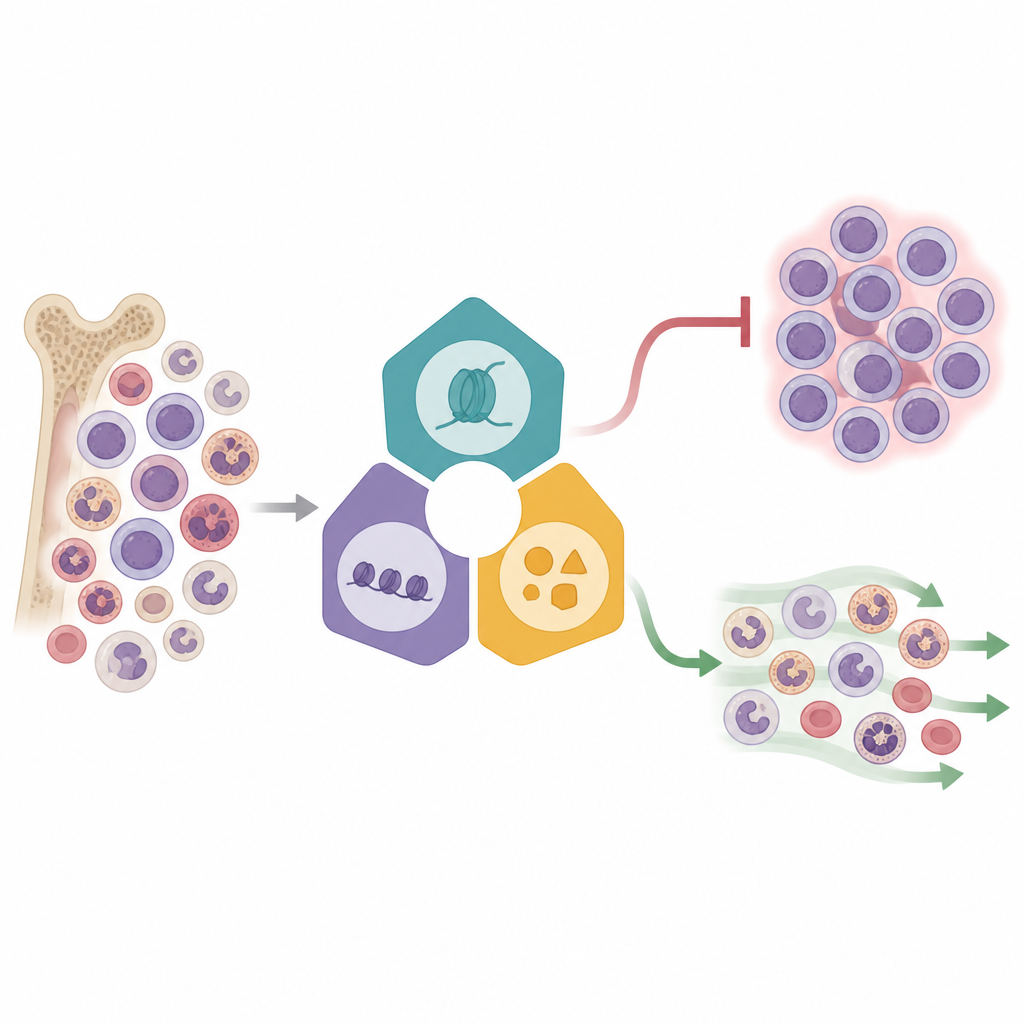
في هذا العمل يركز العلماء على شكل عالي الخطورة من سرطان الدم النخاعي الحاد يتميز بتغيرات في جين يسمى KMT2A. في هذه السرطانات، تتجمد خلايا جذع الدم في مرحلة غير ناضجة بدلاً من أن تنضج إلى خلايا بيضاء قاتلة للعدوى. أظهرت أدوية سابقة تستهدف منظمات إبجينية فردية، والتي تعمل كوسوم كيميائية على عبوة الحمض النووي، وعدًا لكنها نادرًا ما أدت إلى هجرات دائمة. استنتج الفريق أن خلايا اللوكيميا تبقى حية لأن عدة أنظمة إبجينية تتعاون، لذا فإن حجب واحد فقط يترك الآخرين ليتولوا المهمة. لفهم هذه التعاونات حقًا، احتاجوا إلى طريقة لمراقبة ما يحدث داخل آلاف الخلايا الفردية عندما تُعطل منظمات رئيسية واحدة تلو الأخرى.
قراءة آلاف الخلايا دفعة واحدة
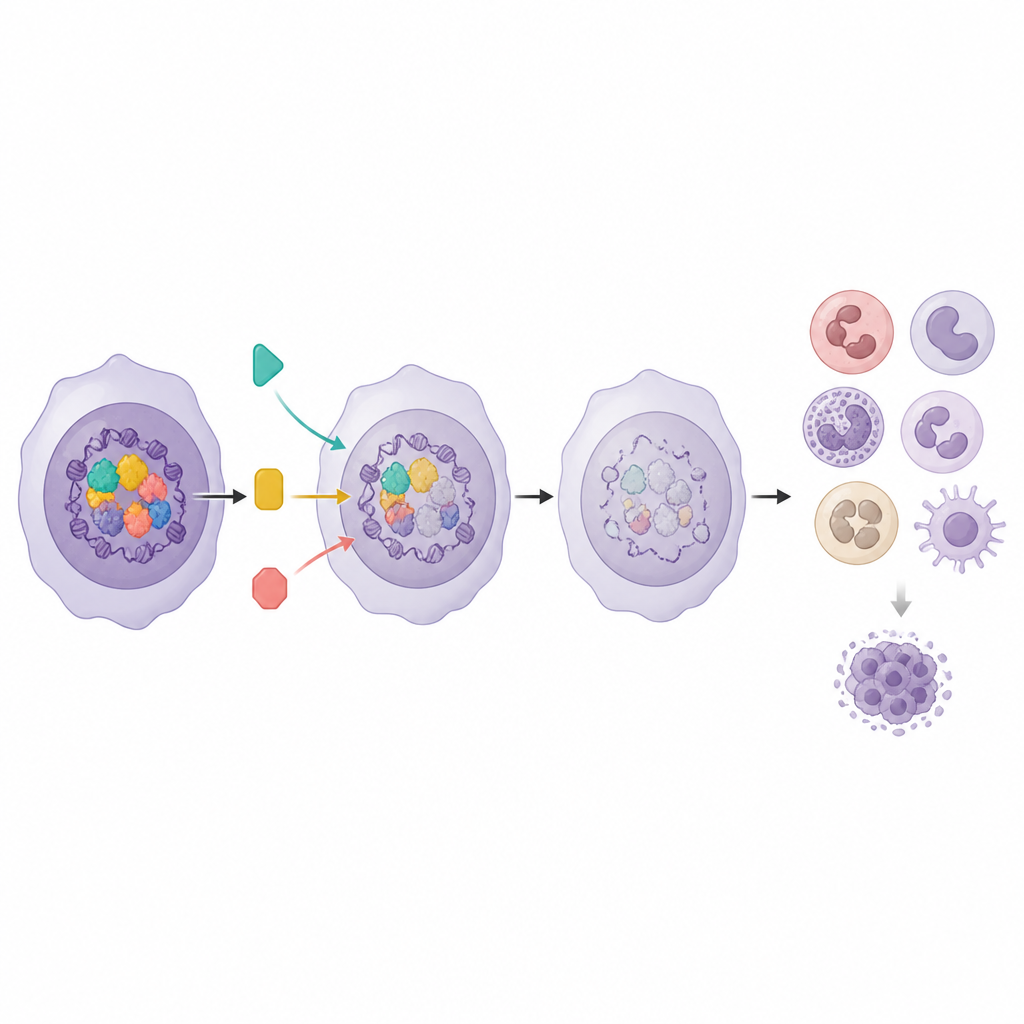
استخدم الباحثون طريقة قوية تسمى Perturb-seq، التي تجمع بين تحرير الجينات وتسلسل الحمض النووي الريبي أحادي الخلية. في خط خلايا اللوكيميا المعاد ترتيب KMT2A، عطلوا 16 منظمات إبجينية مختارة مأخوذة من ثلاثة مجمعات رئيسية تتحكم في تشغيل أو إيقاف الجينات. كل خلية معدَّلة حملت شِفرة شريطية جينية، مما سمح للفريق بربط تعديل محدد بنمط نشاط الجينات في تلك الخلية. من خلال رسم أكثر من 31,000 خلية في فضاء ثنائي الأبعاد مُختزل، رأوا أن الخلايا تتجمع وفقًا للمجمع الذي استُهدِف، كاشفةً أنماط استجابة مميزة. تسببت بعض العوامل، لا سيما المرتبطة بازدواجية Menin–KMT2A والإنزيمات المرتبطة، في تحولات واسعة في نشاط الجينات، بينما كان لآخرين تأثيرات أدق، مما يشير إلى مستويات مختلفة من التحكم داخل شبكة اللوكيميا.
برنامج خفي يفضّل بقاء المرضى
باستخدام النمذجة الحاسوبية، اختزل الفريق البيانات المعقدة إلى 17 برنامجًا جينيًا، يمثل كل منها نمطًا منسقًا لنشاط الجينات. برز برنامج واحد: مجموعة جينات مرتبطة بالتمايز النخاعي، وهي العملية التي تتحول بها الخلايا غير الناضجة إلى خلايا بيضاء وظيفية بالكامل. يسمي المؤلفون هذا "البرنامج النخاعي". كان أكثر نشاطًا في نخاع العظم الطبيعي القريب من النضج الكامل وأظهر ارتباطًا عكسيًا مع جينات تحدد خلايا جذع اللوكيميا. عند فحص مجموعات بيانات مرضى كبيرة، ارتبط النشاط الابتدائي الأعلى للبرنامج النخاعي باستمرار بتحسّن البقاء العام، خصوصًا في المرضى الذين يستجيب سرطانهم جيدًا للعلاج القياسي. يشير هذا إلى أنه حتى داخل سرطان عدواني، توجد خلايا أقرب إلى حالة "جاهزة للنضوج" ترتبط بنتائج أفضل.
محور تحكم ثلاثي ونقاط ضعفه
أظهر التحليل أن ثلاثة منظمات—Menin وDOT1L وKAT6A—تشكل محورًا وظيفيًا يحافظ معًا على قمع البرنامج النخاعي. عندما تعطَّل أي من هذه الجينات، أصبح برنامج التمايز أكثر نشاطًا، لكن بشكل جزئي فقط. اختبر الفريق بعد ذلك أدوية تُثبط كل شريك ووجد تآزرًا لافتًا. أقران مثبط Menin مع مثبط KAT6A، أو مثبط DOT1L مع مثبط KAT6A، قلَّلوا بشكل حاد من نمو خلايا اللوكيميا وعزَّزوا بقوة تعبير جينات البرنامج النخاعي مقارنة بالأدوية المفردة. في الوقت نفسه، اكتشفوا تأثيرًا معاكسًا من مجمع آخر يحتوي على PCGF1. جعل فقدان PCGF1 خلايا اللوكيميا أقل حساسية لمثبط DOT1L، مما يبرز كيف يمكن لبعض العوامل الإبجينية أن تخفف تأثير الأدوية الموجهة وتساهم في المقاومة.
استخدام نشاط الجينات لتوجيه التوليفات الذكية
نظرًا لأن البرنامج النخاعي يربط بين نضج الخلايا وبقاء المرضى، تساءل الباحثون ما إذا كان نشاطه يمكن أن يتنبأ أيضًا بالأدوية الأكثر فعالية. في عينات المرضى، كانت اللوكيميات ذات درجات أعلى في البرنامج النخاعي أكثر حساسية لعدة مثبطات لمسارات الإشارة، لا سيما تلك المستهدفة لـ MEK وAKT وmTOR. عندما جمع الفريق مثبط Menin، الذي يرفع البرنامج النخاعي، مع هذه المثبطات المسارية في نماذج خلوية، أظهرت أزواج الأدوية تآزرًا واضحًا وخفَّضت الجرعات المطلوبة لكبح نمو خلايا اللوكيميا. كما ساعد نفس البرنامج الجيني في التمييز بين التوليفات التي تتعاون فعلاً وتلك التي تدفع الخلايا فقط نحو حالة متمايزة عامة.
ماذا يعني هذا لرعاية اللوكيميا في المستقبل
للقارئ العادي، الرسالة الأساسية أن هذه الدراسة تتجاوز البحث عن "طلقة سحرية" واحدة وتعمل بدلًا من ذلك على رسم كيفية إحكام مجموعات من المنظمات الإبجينية قبضتها على خلايا اللوكيميا لتبقيها في حالة غير ناضجة ومضرة. من خلال تحديد برنامج نخاعي أساسي يتنبأ بكل من تحسّن البقاء وزيادة حساسية الدواء، وتحديد محور ثلاثي Menin–KAT6A–DOT1L الذي يقمع هذا البرنامج، يوفر العمل خارطة طريق للعلاجات المركبة المبنية على أسس منطقية. على المدى الطويل، قد يساعد قياس نشاط البرنامج النخاعي لدى المرضى الأطباء على اختيار أزواج أدوية ترفع حاجز النضج وتستغل نقاط ضعف جديدة في السرطان، مما قد يؤدي إلى علاجات أكثر ديمومة وتخصيصًا لسرطان الدم النخاعي الحاد.
الاستشهاد: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
الكلمات المفتاحية: سرطان الدم النخاعي الحاد, العلاج الإبجيني, تمايز الخلايا, تآزر دوائي, علم الجينوم أحادي الخلية