Clear Sky Science · nl
Een Perturb‑seq-kaart van een differentiatiehub onthult synergetische kwetsbaarheden in KMT2A‑gerangschikte acute myeloïde leukemie
Waarom deze leukemiestudie ertoe doet
Acute myeloïde leukemie is een snel voortschrijdende bloedkanker die vaak weerstand biedt tegen moderne gerichte medicijnen. Veel nieuwe behandelingen proberen één enkele kankerdrijver uit te schakelen, alleen om te zien dat de ziekte zich aanpast en terugkeert. Deze studie stelt een cruciale vraag voor patiënten en familie: in plaats van één schakelaar tegelijk om te zetten, kunnen we het hele bedieningspaneel in kaart brengen dat leukemiecellen in een onrijpe staat houdt, en vervolgens zwakke plekken vinden waar combinatiebehandelingen veel beter werken dan een enkel medicijn?
De kankercellen die weigeren volwassen te worden
In dit werk richten de onderzoekers zich op een hoogrisicovorm van acute myeloïde leukemie die wordt gekenmerkt door veranderingen in een gen genaamd KMT2A. Bij deze vormen van kanker blijven bloedstamcellen vastzitten in een onrijpe fase in plaats van uit te rijpen tot infectiebestrijdende witte bloedcellen. Eerdere middelen die individuele epigenetische regelaars targetten — die functioneren als chemische labels op het DNA‑pakkingmateriaal — lieten veelbelovende signalen zien maar leidden zelden tot blijvende remissies. Het team redeneerde dat leukemiecellen overleven omdat meerdere epigenetische systemen samenwerken, zodat het blokkeren van slechts één systeem anderen in staat laat zijn het werk over te nemen. Om deze samenwerking echt te begrijpen, hadden ze een manier nodig om te observeren wat er gebeurt in duizenden individuele cellen wanneer belangrijke regelaars één voor één worden uitgeschakeld.
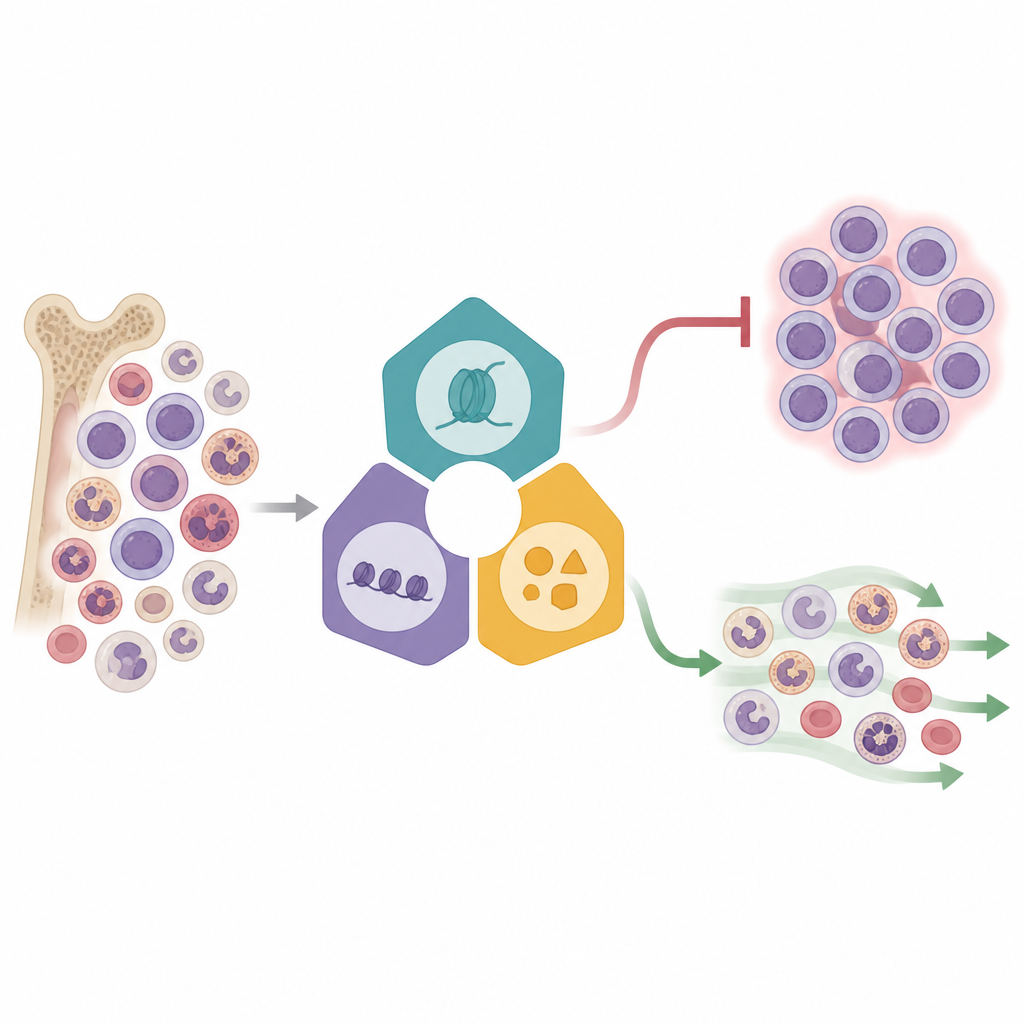
Duizenden cellen tegelijk lezen
De onderzoekers gebruikten een krachtige methode genaamd Perturb‑seq, die genbewerking combineert met single‑cell RNA‑sequencing. In een KMT2A‑gerangschikte leukemiecellenlijn verstoorden ze 16 geselecteerde epigenetische regelaars afkomstig uit drie belangrijke complexen die bepalen welke genen aan of uit staan. Elke bewerkte cel droeg een genetische barcode, waardoor het team een specifieke bewerking aan het genexpressieprofiel van die cel kon koppelen. Door meer dan 31.000 cellen in een gereduceerde tweedimensionale ruimte in kaart te brengen, zagen ze dat cellen zich groeperen op basis van welk complex werd geraakt, wat onderscheidende responspatronen onthulde. Sommige factoren, met name die verbonden met de Menin‑KMT2A fusie en gerelateerde enzymen, veroorzaakten ingrijpende verschuivingen in genexpressie, terwijl andere subtielere effecten hadden, wat wijst op verschillende niveaus van controle binnen het leukemienetwerk.
Een verborgen programma dat gunstig is voor overleving
Met behulp van computationele modellering destilleerde het team de complexe data tot 17 genprogramma’s, elk representatief voor een gecoördineerd patroon van genexpressie. Eén programma stak eruit: een set genen die gekoppeld zijn aan myeloïde differentiatie, het proces waarbij onrijpe cellen volledig functionele witte bloedcellen worden. De auteurs noemen dit het Myeloid Program. Het was het meest actief in normaal beenmerg dat dicht bij volledige rijping staat en toonde een omgekeerde relatie met genen die leukemiestamcellen definiëren. Bij analyse van grote patiëntendatasets hing een hogere basisactiviteit van het Myeloid Program consequent samen met betere totale overleving, vooral bij patiënten wier leukemie doorgaans goed reageert op standaardbehandeling. Dit suggereert dat zelfs binnen een agressieve kanker sommige cellen dichter bij een “klaar om te rijpen” toestand zitten, wat aan betere uitkomsten is gekoppeld.
Een driedelig regelcentrum en zijn zwakke plekken
De analyse toonde aan dat drie regelaars — Menin, DOT1L en KAT6A — een functionele hub vormen die gezamenlijk het Myeloid Program onderdrukt. Wanneer een van deze genen werd verstoord, werd het differentiatieprogramma actiever, maar slechts gedeeltelijk. Het team testte vervolgens medicijnen die elk van de partners remmen en ontdekte opvallende synergie. Het combineren van een Meninremmer met een KAT6A‑remmer, of een DOT1L‑remmer met een KAT6A‑remmer, verminderde de groei van leukemiecellen sterk en verhoogde de expressie van Myeloid Program‑genen vergeleken met enkelvoudige middelen. Tegelijkertijd vonden ze een tegengestelde invloed van een ander complex dat PCGF1 bevat. Verlies van PCGF1 maakte leukemiecellen minder gevoelig voor DOT1L‑remming, wat benadrukt hoe sommige epigenetische factoren het effect van gerichte medicijnen kunnen afzwakken en bijdragen aan resistentie.
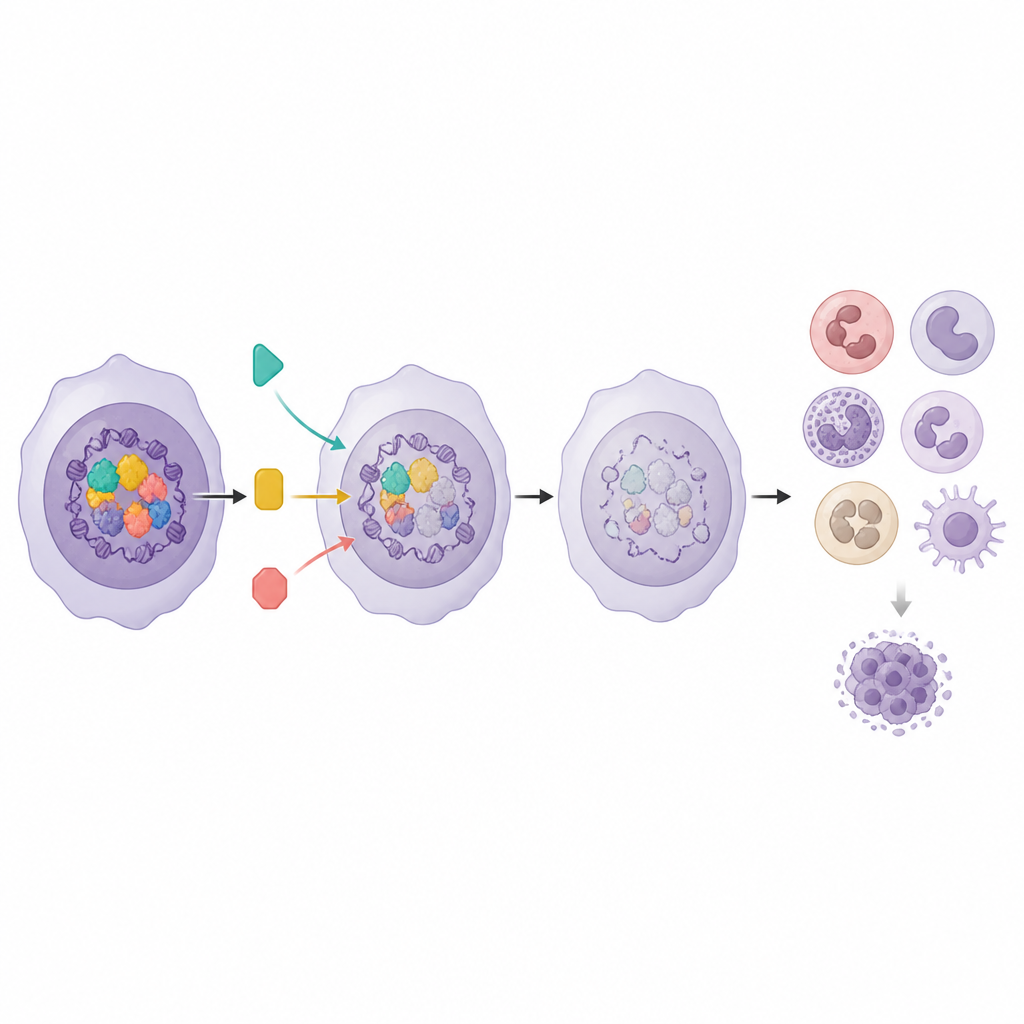
Genactiviteit gebruiken om slimme combinaties te sturen
Aangezien het Myeloid Program verbonden is met zowel celrijping als patiëntoverleving, vroegen de onderzoekers zich af of de activiteit ervan ook kon voorspellen welke medicijnen het beste zouden werken. In patiëntmonsters waren leukemieën met hogere Myeloid Program‑scores gevoeliger voor meerdere remmers van signaleringspaden, met name die gericht op MEK, AKT en mTOR. Toen het team een Meninremmer, die het Myeloid Program verhoogt, combineerde met deze padremmers in celmodellen, toonden de medicijnparen duidelijke synergie en verlaagden ze de benodigde doseringen om de groei van leukemiecellen te remmen. Hetzelfde genprogramma hielp ook om combinaties te onderscheiden die werkelijk samenwerken van die welke cellen slechts naar een algemene gedifferentieerde staat duwen.
Wat dit betekent voor toekomstige leukemiezorg
Voor een algemene lezer is de kernboodschap dat deze studie verder gaat dan de zoektocht naar een enkele “magische kogel” en in plaats daarvan in kaart brengt hoe groepen epigenetische regelaars gezamenlijk leukemiecellen in een onrijpe, schadelijke staat houden. Door een kern‑Myeloid Program te identificeren dat zowel betere overleving als verhoogde gevoeligheid voor medicijnen voorspelt, en door een driedelige Menin‑KAT6A‑DOT1L hub te lokaliseren die dit programma onderdrukt, biedt het werk een blauwdruk voor rationele combinatietherapieën. Op de lange termijn zou het meten van Myeloid Program‑activiteit bij patiënten artsen kunnen helpen bij het kiezen van medicijnparen die zowel het rijpingsblok opheffen als nieuwe zwakke plekken in de kanker exploiteren, wat mogelijk leidt tot duurzamere en meer gepersonaliseerde behandelingen voor acute myeloïde leukemie.
Bronvermelding: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Trefwoorden: acute myeloïde leukemie, epigenetische therapie, cel‑differentiatie, drugsynergie, single‑cell genomica