Clear Sky Science · es
Un mapa Perturb‑seq de un centro de diferenciación revela vulnerabilidades sinérgicas en la leucemia mieloide aguda con reordenamiento de KMT2A
Por qué importa este estudio sobre leucemia
La leucemia mieloide aguda es un cáncer sanguíneo de rápida evolución que con frecuencia resiste los fármacos dirigidos modernos. Muchos tratamientos nuevos intentan apagar conductores únicos del cáncer, solo para ver que la enfermedad se adapta y reaparece. Este estudio plantea una pregunta crucial para pacientes y familias: en lugar de accionar un interruptor a la vez, ¿podemos cartografiar todo el panel de control que mantiene a las células leucémicas en un estado inmaduro y luego encontrar puntos débiles donde las terapias combinadas funcionen mucho mejor que cualquier fármaco solo?
Las células cancerosas que se niegan a madurar
En este trabajo, los científicos se centran en una forma de alto riesgo de leucemia mieloide aguda marcada por alteraciones en un gen llamado KMT2A. En estos cánceres, las células madre sanguíneas quedan congeladas en una fase inmadura en lugar de madurar hacia glóbulos blancos capaces de combatir infecciones. Fármacos anteriores que apuntaban reguladores epigenéticos individuales, que actúan como etiquetas químicas sobre el empaquetamiento del ADN, mostraron promesa pero rara vez produjeron remisiones duraderas. El equipo razonó que las células leucémicas sobreviven porque varios sistemas epigenéticos cooperan, por lo que bloquear solo uno deja a los demás compensando. Para comprender verdaderamente esa cooperación, necesitaban una forma de observar lo que ocurre dentro de miles de células individuales cuando se apagan reguladores clave una por una.
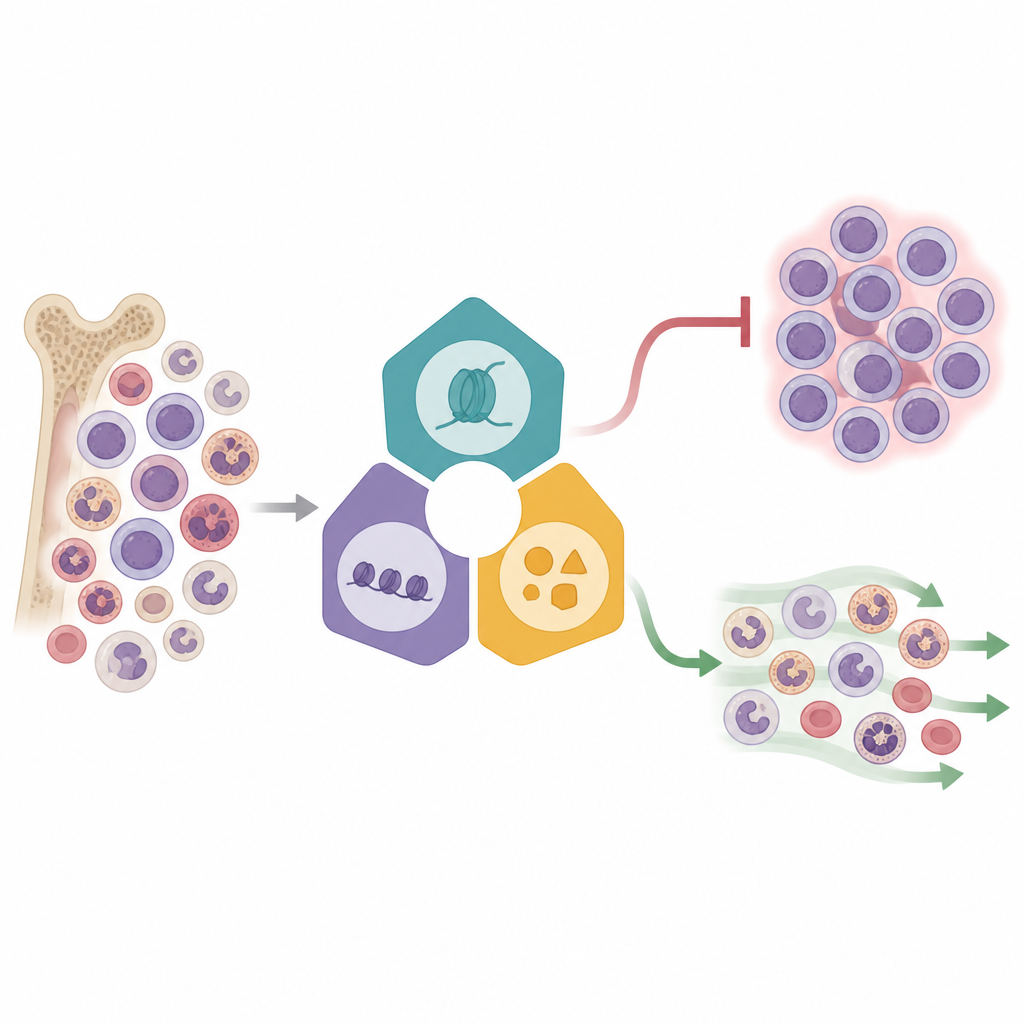
Leer miles de células a la vez
Los investigadores utilizaron un método potente llamado Perturb‑seq, que combina edición genética con secuenciación del ARN de célula única. En una línea celular de leucemia con reordenamiento de KMT2A, interrumpieron 16 reguladores epigenéticos seleccionados procedentes de tres complejos principales que controlan qué genes se activan o silencian. Cada célula editada llevaba un código de barras genético, lo que permitió al equipo vincular una edición específica al perfil de actividad génica de esa célula. Al mapear más de 31.000 células en un espacio reducido bidimensional, observaron que las células se agrupaban según qué complejo había sido afectado, revelando patrones de respuesta distintos. Algunos factores, especialmente los vinculados con la fusión Menin‑KMT2A y enzimas relacionadas, provocaron cambios extensos en la actividad génica, mientras que otros tuvieron efectos más sutiles, sugiriendo diferentes niveles de control dentro de la red leucémica.
Un programa oculto que favorece la supervivencia del paciente
Mediante modelado computacional, el equipo destiló los datos complejos en 17 programas génicos, cada uno representando un patrón coordinado de actividad génica. Un programa destacó: un conjunto de genes vinculados a la diferenciación mieloide, el proceso por el cual las células inmaduras se convierten en glóbulos blancos plenamente funcionales. Los autores denominan esto el Programa Mieloide. Estuvo más activo en células de médula ósea normales cercanas a la maduración completa y mostró una relación inversa con genes que definen células madre leucémicas. Cuando los investigadores examinaron grandes conjuntos de datos de pacientes, una mayor actividad basal del Programa Mieloide se asoció de forma consistente con mejor supervivencia global, especialmente en pacientes cuya leucemia tiende a responder bien al tratamiento estándar. Esto sugiere que incluso dentro de un cáncer agresivo, algunas células están más cerca de un estado “listas para madurar” que se relaciona con mejores resultados.
Un centro de control de tres partes y sus puntos débiles
El análisis reveló que tres reguladores —Menin, DOT1L y KAT6A— forman un centro funcional que conjuntamente mantiene reprimido el Programa Mieloide. Cuando cualquiera de estos genes fue interrumpido, el programa de diferenciación se activó más, pero solo de forma parcial. El equipo probó entonces fármacos que inhiben a cada socio y descubrió una sinergia notable. Combinar un inhibidor de Menin con uno de KAT6A, o un inhibidor de DOT1L con uno de KAT6A, redujo drásticamente el crecimiento de células leucémicas y aumentó con fuerza la expresión de genes del Programa Mieloide en comparación con fármacos individuales. Al mismo tiempo, identificaron una influencia opuesta de otro complejo que contiene PCGF1. La pérdida de PCGF1 volvió a las células leucémicas menos sensibles a la inhibición de DOT1L, lo que destaca cómo algunos factores epigenéticos pueden mitigar el efecto de fármacos dirigidos y contribuir a la resistencia.
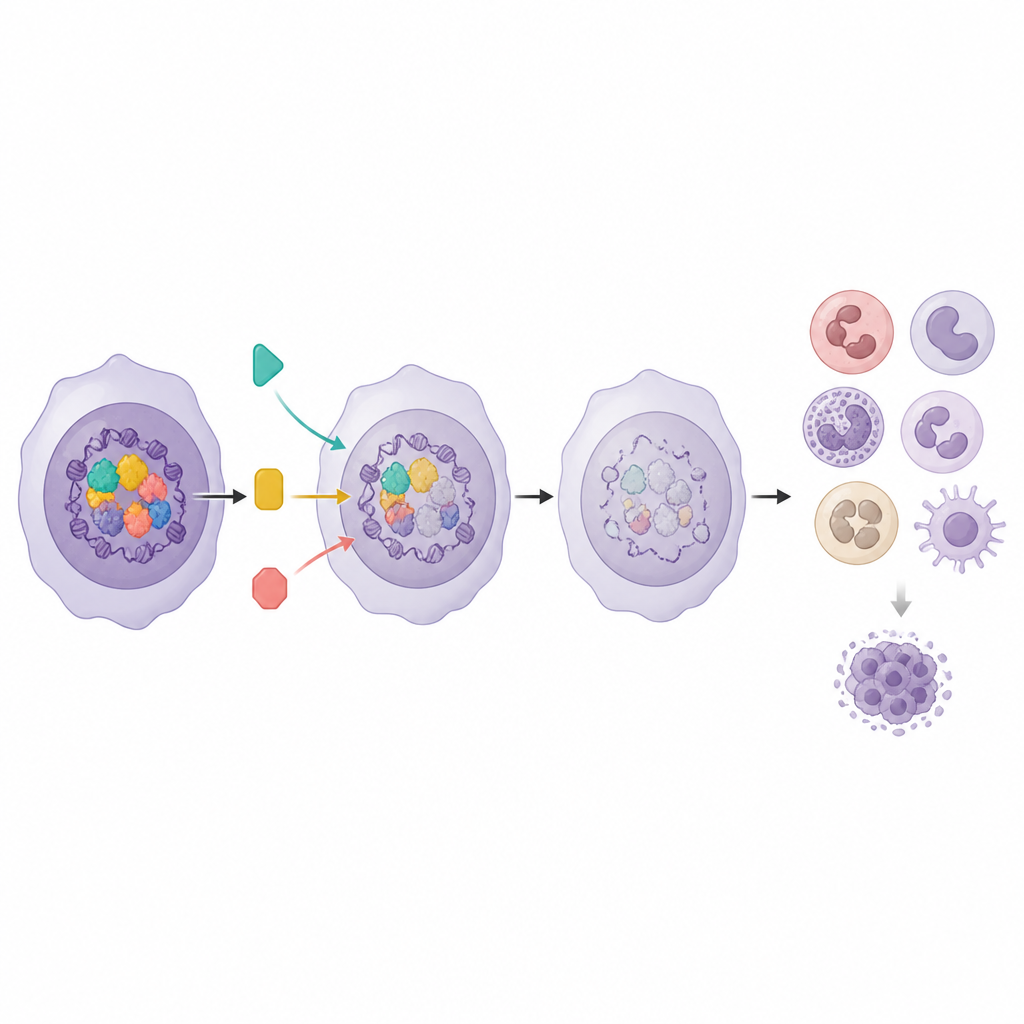
Usar la actividad génica para guiar combinaciones inteligentes
Dado que el Programa Mieloide se vincula tanto con la maduración celular como con la supervivencia del paciente, los investigadores preguntaron si su actividad también podría predecir qué fármacos funcionarían mejor. En muestras de pacientes, las leucemias con puntuaciones más altas del Programa Mieloide fueron más sensibles a varios inhibidores de vías de señalización, en particular los que apuntan a MEK, AKT y mTOR. Cuando el equipo combinó un inhibidor de Menin, que incrementa el Programa Mieloide, con estos inhibidores de vías en modelos celulares, las parejas de fármacos mostraron sinergia clara y redujeron las dosis necesarias para frenar el crecimiento de células leucémicas. El mismo programa génico también ayudó a distinguir combinaciones que realmente cooperan de aquellas que simplemente empujan a las células hacia un estado diferenciado genérico.
Qué significa esto para la atención futura de la leucemia
Para un lector no especializado, el mensaje clave es que este estudio va más allá de la búsqueda de una sola “bala mágica” y en su lugar cartografía cómo grupos de reguladores epigenéticos mantienen conjuntamente a las células leucémicas en un estado inmaduro y perjudicial. Al identificar un Programa Mieloide central que predice tanto mejor supervivencia como mayor sensibilidad a fármacos, y al señalar un centro triple Menin‑KAT6A‑DOT1L que suprime este programa, el trabajo ofrece un plano para terapias combinadas racionales. A largo plazo, medir la actividad del Programa Mieloide en pacientes podría ayudar a los médicos a elegir pares de fármacos que tanto liberen el bloqueo de maduración como exploten nuevas vulnerabilidades del cáncer, lo que potencialmente conduciría a tratamientos más duraderos y personalizados para la leucemia mieloide aguda.
Cita: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Palabras clave: leucemia mieloide aguda, terapia epigenética, diferenciación celular, sinergia farmacológica, genómica de célula única