Clear Sky Science · ru
Карта Perturb-seq дифференцировочного узла выявляет синергетические уязвимости при остром миелоидном лейкозе с перестройкой KMT2A
Почему это исследование лейкемии важно
Острый миелоидный лейкоз — быстро прогрессирующий рак крови, который часто сопротивляется современным таргетным препаратам. Многие новые подходы пытаются выключить отдельные драйверы рака, но заболевание адаптируется и возвращается. В этом исследовании задают важный вопрос для пациентов и их семей: вместо того чтобы поочерёдно нажимать отдельные переключатели, можно ли составить карту всей панели управления, которая удерживает лейкемические клетки в незрелом состоянии, и найти уязвимые места, где комбинированная терапия действует значительно лучше любой отдельной молекулы?
Раковые клетки, которые отказываются взрослеть
В этой работе учёные сосредоточились на высокорискованной форме острого миелоидного лейкоза, связанной с перестройками гена KMT2A. В таких опухолях стволовые клетки крови застревают в незрелой фазе вместо того, чтобы дифференцироваться в функциональные лейкоциты. Ранее разработанные препараты, нацеленные на отдельные эпигенетические регуляторы — химические метки на упаковке ДНК — показывали обнадёживающие результаты, но редко приводили к устойчивой ремиссии. Исследователи предположили, что лейкемические клетки выживают потому, что несколько эпигенетических систем сотрудничают, и блокировка одной из них оставляет другие, чтобы компенсировать утрату. Чтобы по-настоящему понять это взаимодействие, им нужен был способ наблюдать, что происходит внутри тысяч отдельных клеток, когда ключевые регуляторы поочерёдно выводят из строя.
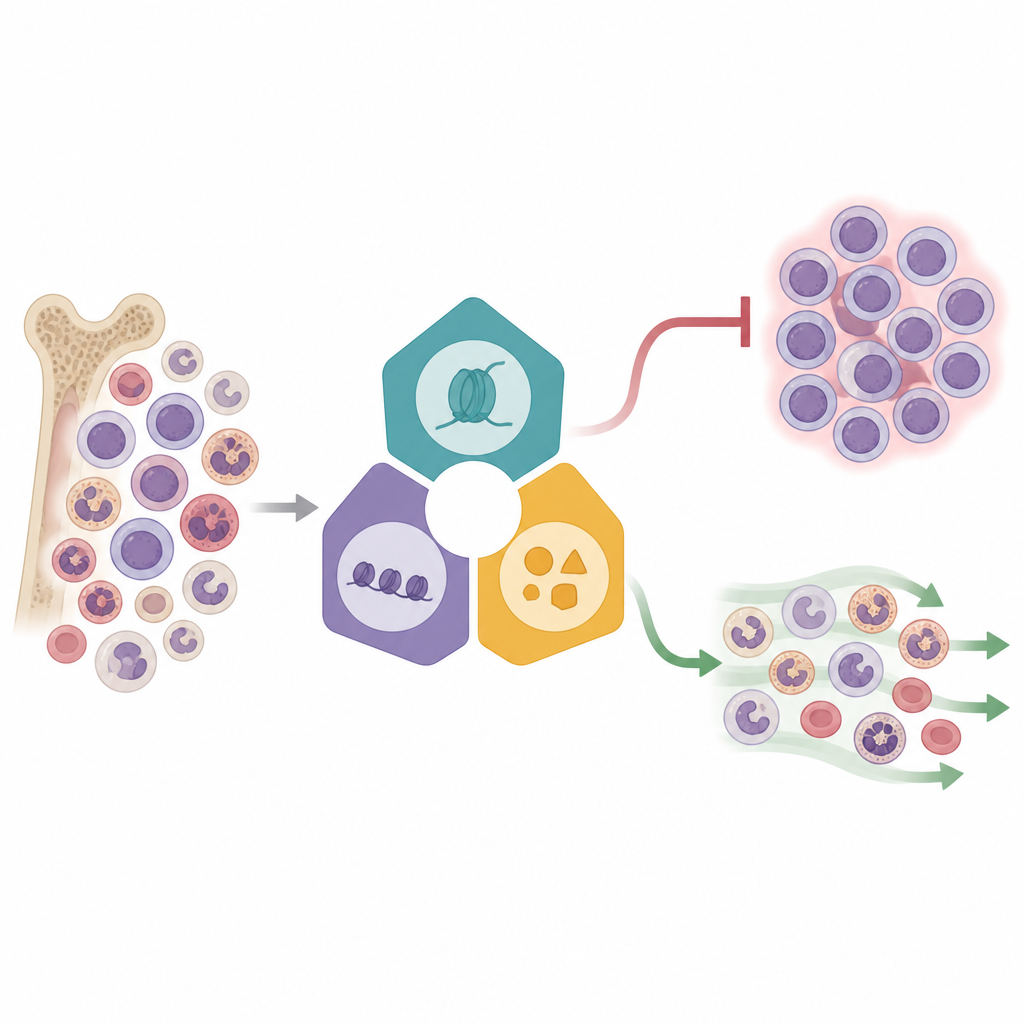
Чтение тысяч клеток одновременно
Исследователи использовали мощный метод Perturb-seq, который сочетает редактирование генов с секвенированием РНК одиночных клеток. В клеточной линии лейкемии с перестройкой KMT2A они нарушили работу 16 выбранных эпигенетических регуляторов из трёх крупных комплексов, контролирующих включение или выключение генов. Каждая отредактированная клетка несла генетический штрихкод, что позволяло связать конкретную правку с профилем геновой активности этой клетки. Отобразив более 31 000 клеток в сниженной двумерной проекции, они увидели, что клетки группируются в зависимости от того, какой комплекс был поражён, — выявились разные паттерны ответа. Некоторые факторы, особенно связанные с слиянием Menin–KMT2A и связанными ферментами, вызывали масштабные сдвиги в активности генов, тогда как другие давали более тонкие эффекты, указывая на разные уровни контроля внутри сети лейкемии.
Скрытая программа, благоприятствующая выживаемости пациентов
С помощью вычислительного моделирования команда свела сложные данные к 17 генным программам, каждая из которых представляет координированный паттерн активности генов. Выделилась одна программа: набор генов, связанных с миелоидной дифференцировкой — процессом, в котором незрелые клетки становятся полностью функциональными лейкоцитами. Авторы называют её Миелоидной программой. Она была наиболее активна в нормальном костном мозге в клетках, близких к полной зрелости, и демонстрировала обратную связь с генами, определяющими лейкемические стволовые клетки. При анализе больших когорт пациентов более высокая исходная активность Миелоидной программы стабильно ассоциировалась с лучшей общей выживаемостью, особенно у пациентов, чья лейкемия лучше отвечает на стандартную терапию. Это указывает на то, что даже в агрессивном раке часть клеток находится ближе к состоянию «готовности к созреванию», что связано с лучшими исходами.
Трёхчастный контрольный узел и его слабые места
Анализ показал, что три регулятора — Menin, DOT1L и KAT6A — образуют функциональный узел, который совместно подавляет Миелоидную программу. При нарушении любого из этих генов программа дифференцировки становилась более активной, но лишь частично. Затем команда протестировала препараты-ингибиторы каждого из партнёров и обнаружила поразительный синергизм. Сочетание ингибитора Menin с ингибитором KAT6A или ингибитора DOT1L с ингибитором KAT6A резко снижало рост лейкемических клеток и значительно усиливало экспрессию генов Миелоидной программы по сравнению с отдельными препаратами. Одновременно они выявили противоположное влияние другого комплекса, содержащего PCGF1. Потеря PCGF1 делала клетки лейкемии менее чувствительными к ингибированию DOT1L, что подчёркивает, как некоторые эпигенетические факторы могут ослаблять эффект целевых препаратов и способствовать резистентности.
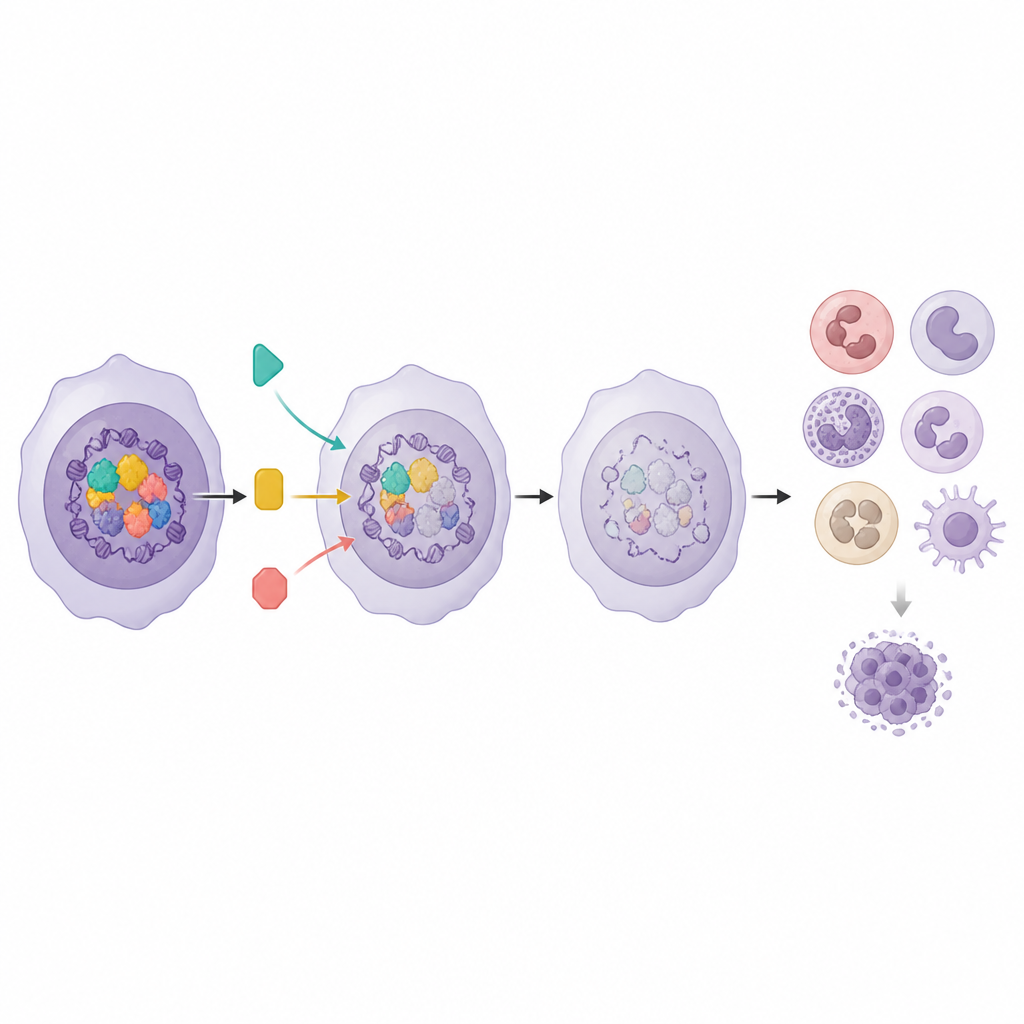
Использование активности генов для разумного подбора комбинаций
Поскольку Миелоидная программа связана и с созреванием клеток, и с выживаемостью пациентов, исследователи поинтересовались, может ли её активность прогнозировать, какие препараты будут наиболее эффективны. В образцах пациентов лейкемии с более высокими оценками Миелоидной программы были более чувствительны к нескольким ингибиторам сигнальных путей, в частности направленным против MEK, AKT и mTOR. Когда команда сочетала ингибитор Menin, который повышает активность Миелоидной программы, с этими ингибиторами путей в клеточных моделях, пары препаратов демонстрировали явный синергизм и снижали требуемые дозы для подавления роста лейкемических клеток. Та же генная программа помогала отличать комбинации, которые действительно сотрудничают, от тех, которые лишь толкают клетки в общее дифференцированное состояние.
Что это значит для будущей терапии лейкемии
Для неспециалиста главный вывод таков: это исследование уходит дальше поиска единственной «волшебной пули» и вместо этого картирует, как группы эпигенетических регуляторов совместно удерживают лейкемические клетки в незрелом, вредоносном состоянии. Выявив ключевую Миелоидную программу, которая предсказывает как лучшую выживаемость, так и повышенную чувствительность к препаратам, а также определив трёхчастный узел Menin–KAT6A–DOT1L, подавляющий эту программу, исследование даёт план рациональной разработки комбинированных терапий. В перспективе измерение активности Миелоидной программы у пациентов могло бы помочь врачам выбирать пары препаратов, которые одновременно снимают блок созревания и эксплуатируют новые слабые места рака, что потенциально приведёт к более стойким и персонализированным методам лечения острого миелоидного лейкоза.
Цитирование: Aryal, S., Curtiss, B.M., Zhou, X. et al. A Perturb-seq map of a differentiation hub reveals synergistic vulnerabilities in KMT2A-rearranged acute myeloid leukemia. Leukemia 40, 996–1008 (2026). https://doi.org/10.1038/s41375-026-02917-2
Ключевые слова: острый миелоидный лейкоз, эпигенетическая терапия, клеточная дифференцировка, лекарственный синергизм, геномика одиночных клеток